
【題目】NA表示阿伏加德羅常數,下列敘述錯誤的是( )
A.2 g D![]() O中含有的質子數、中子數、電子數均為NA
O中含有的質子數、中子數、電子數均為NA
B.含有NA個“Cu”微粒的CuO和Cu2S混合物質量為80 g
C.標準狀況下,5.6 L氧氣作氧化劑時轉移電子數一定為NA
D.58.5 g NaCl晶體中含有NA個Na+
【答案】C
【解析】
A.2gD![]() O的物質的量為0.1mol,1個D
O的物質的量為0.1mol,1個D![]() O分子中含有10個質子、10個中子、10個電子,含有的質子數、中子數、電子數均為NA,故A正確;
O分子中含有10個質子、10個中子、10個電子,含有的質子數、中子數、電子數均為NA,故A正確;
B.CuO、Cu2S中銅的質量分數均為80%,故當混合物中含有1 mol“Cu”時,即64gCu,則混合物質量為![]() =80 g,故B正確;
=80 g,故B正確;
C.標準狀況下,5.6 L O2的物質的量n=![]() =
=![]() =0.25 mol,0.25mol氧氣作氧化劑時轉移電子數不一定為NA,如在反應2Na+O2
=0.25 mol,0.25mol氧氣作氧化劑時轉移電子數不一定為NA,如在反應2Na+O2![]() Na2O2中,0.25mol氧氣與金屬鈉反應生成0.25mol過氧化鈉,反應轉移了0.5mol電子,轉移的電子數為0.5NA,故C錯誤;
Na2O2中,0.25mol氧氣與金屬鈉反應生成0.25mol過氧化鈉,反應轉移了0.5mol電子,轉移的電子數為0.5NA,故C錯誤;
D.58.5 g氯化鈉的物質的量為1mol,1mol氯化鈉由1mol鈉離子和1mol氯離子構成,故1mol氯化鈉中含NA個Na+,故D正確;
答案選C。


 開心練習課課練與單元檢測系列答案
開心練習課課練與單元檢測系列答案 開心試卷期末沖刺100分系列答案
開心試卷期末沖刺100分系列答案科目:高中化學 來源: 題型:
【題目】下列實驗中,儀器的下端必須插入液面下的有( )
①制備氫氣的簡易裝置中加入稀硫酸的長頸漏斗;
②制備氯氣裝置中的分液漏斗;
③用新制的FeSO4溶液和NaOH溶液制備Fe(OH)2操作中的膠頭滴管;
④將 氯氣溶于水時制取氯水的導氣管;
⑤蒸餾石油時的溫度計;
A.2個B.3個C.4個D.5個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[化學——選修3:物質結構與性質]碳及其化合物廣泛存在于自然界中,回答下列問題:
(1)處于一定空間運動狀態的電子在原子核外出現的概率密度分布可用___________形象化描述。在基態原子中,核外存在______對自旋相反的電子。
(2)碳在形成化合物時,其鍵型以共價鍵為主,原因是_____________。
(3)CS2分子中,共價鍵的類型有_____________,C原子的雜化軌道類型是_______,寫出兩個與CS2具有相同空間構型和鍵合形式的分子或離子_______________。
(4)CO能與金屬Fe形成Fe(CO)5,該化合物的熔點為253K,沸點為376K,其固體屬于_____晶體。
碳有多種同素異形體,其中石墨烯與金剛石的晶體結構如圖所示:
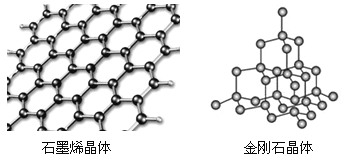
①在石墨烯晶體中,每個C原子連接_____個六元環,每個六元環占有___個C原子。
②在金剛石晶體中,C原子所連接的最小環也為六元環,每個C原子連接________個六元環,六元環中最多有________個C原子在同一平面。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物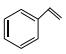 (甲)、
(甲)、![]() (乙)、
(乙)、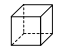 (丙)的分子式均為
(丙)的分子式均為![]() ,下列說法正確的是( )
,下列說法正確的是( )
A. 甲的同分異構體只有乙和丙兩種
B. 甲、乙、丙的一氯代物種數最少的是丙
C. 甲、乙、丙均可與溴的四氯化碳溶液反應
D. 甲中所有原子可能處于同一平面
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:pAg=-lgc(Ag+),Ksp(AgCl)=1×10-12,Ksp (AgI)=1×10-16。如圖是向10mLAgNO3溶液中逐滴滴入0.1mo1·L-1的NaCl溶液時,pAg隨著加入NaCl溶液的體積變化的圖像(實線)。下列敘述正確的是
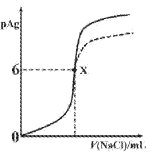
A. 原AgNO3溶液的物質的量濃度為0.1mol·L-1
B. 圖中x點表示溶液中Ag+恰好完全沉淀
C. 圖中x點的坐標為(10,6)
D. 若把NaCl溶液換成0.1mol·L-1NaI溶液,則圖像在終點后變為虛線部分
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】弱電解質的電離平衡、鹽類的水解平衡和難溶物的溶解平衡均屬于化學平衡.根據要求回答問題
(1)生活中明礬常作凈水劑,其凈水的原理是___________(用離子方程式表示).
(2)物質的量濃度相同的CH3COOH 溶液和NaOH 溶液混合后,溶液中c(CH3COO)=c(Na+),則CH3COOH 溶液的體積_____NaOH 溶液的體積.(填“大于”、“小于”或“等于”.)
(3)常溫下,取0.2molL﹣1 HCl溶液與0.2molL﹣1 MOH溶液等體積混合,測得混合溶液后的pH=5.寫出MOH的電離方程式:_______________________.
(4)含![]() 的廢水毒性較大,某工廠廢水中含5.0×10﹣3 molL﹣1的
的廢水毒性較大,某工廠廢水中含5.0×10﹣3 molL﹣1的![]() .為了使廢水的排放達標,進行如下處理:
.為了使廢水的排放達標,進行如下處理:
![]()
①綠礬為FeSO47H2O.反應(I)中Cr2O72﹣與FeSO4的物質的量之比為_____.
②常溫下若處理后的廢水中c(Cr3+)=6.0×10﹣7 molL﹣1,則處理后的廢水的pH=_____(Ksp[Cr(OH)3]=6.0×10﹣31)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液中濃度關系正確的是( )
A. 小蘇打溶液中:c(Na+)+c(H+)=c(HCO)+c(CO![]() )+c(OH-)
)+c(OH-)
B. CH3COONa溶液中:c(CH3COO-)>c(Na+)
C. 物質的量濃度相等的CH3COOH溶液和CH3COONa溶液等體積混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
D. 0.1 mol/L的NaHA溶液,其pH=4,則c(HA-)>c(H+)>c(H2A)>c(A2-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A.MnO2能加速H2O2的分解,是因為MnO2可以降低反應所需的活化能
B.向橙色的K2Cr2O7溶液中滴加NaOH溶液,溶液顏色變黃,說明化學平衡發生了移動
C.將盛有NO2氣體的密閉容器浸泡在熱水中,容器內氣體顏色變深,這一事實可以用勒夏特列原理解釋
D.FeCl3溶液和Fe2(SO4)3溶液加熱蒸干、灼燒都得到Fe2O3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定量的某磁黃鐵礦(主要成分FexS,S為-2價)與100mL鹽酸恰好完全反應(礦石中其他成分不與鹽酸反應),生成3.2g硫單質、0.4molFeCl2和一定量H2S氣體,且溶液中無Fe3+。則下列說法正確的是( )
A.該鹽酸的物質的量濃度為4.0mol·L-1
B.該磁黃鐵礦FexS中,Fe2+與Fe3+的物質的量之比為2:1
C.生成的H2S氣體在標準狀況下的體積為8.96L
D.該磁黃鐵礦中FexS的x=0.85
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com