
【題目】某興趣小組探究SO2氣體還原Fe3+的反應,他們使用的藥品和裝置如下圖所示,下列說法不合理的是( )

A. 能表明I-的還原性弱于SO2的現象是B中藍色溶液褪色
B. 裝置C的作用是吸收多余的SO2,防止污染空氣
C. 為了驗證A中發生了氧化還原反應,加入用稀鹽酸酸化的BaCl2,產生白色沉淀
D. 為了驗證A中發生了氧化還原反應,加入酸性KMnO4溶液,紫紅色褪去
科目:高中化學 來源: 題型:
【題目】甲、乙、丙、丁均為中學化學中常見的單質或化合物,它們之間的轉化關系如圖所示(部分產物已略去),下列各組物質中不能按圖示關系轉化的是( )

選項 | 甲 | 乙 | 丙 | 丁 |
A | NaOH | NaHSO3 | Na2SO3 | SO2 |
B | AlCl3 | Na[Al(OH)4] | Al(OH)3 | NaOH |
C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 |
D | C | CO | CO2 | O2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】冬天使用的熱敷袋里面有鐵粉、氯化鈉、碳粉,利用鐵被氧化放出的熱量取暖.某同學拆開一袋后取里面的固體粉末進行實驗:
①將粉末投入盛有足量稀鹽酸的燒杯中,觀察到有大量氣泡產生,底部有黑色粉末.則發生反應的離子方程式為 .
②為分離出反應后的溶液,可將上述燒杯中混合物進行操作,該操作需要的玻璃儀器為 .
③在②得到的溶液中通入氯氣,發生如下離子反應:2Fe2++Cl2=2Fe3++2Cl─;在該離子方程式中,當有ag氧化產物生成時,需通入標準狀況下的氯氣體積為L(用含a的代數式表示).
④該同學將少量銅片投入制得的含FeCl3的溶液中,發現銅片慢慢溶解消失,溶液由黃色變為青綠色.則發生反應的離子方程式為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在三個密閉容器中分別充入氦氣、氧氣、氮氣,當它們的溫度和密度都相同時,這三種氣體的壓強(P)從大到小的順序是
A. 氦氣>氧氣>氮氣 B. 氧氣>氮氣>氦氣
C. 氧氣>氦氣>氮氣 D. 氦氣>氮氣>氧氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數值。下列有關敘述正確的是( )
A. 14 g乙烯和丙烯混合氣體中的氫原子數為2NA
B. 1 mol N2與4 mol H2反應生成的NH3分子數為2NA
C. 1 mol Fe溶于過量硝酸,電子轉移數為2NA
D. 標準狀況下,2.24 L CCl4含有的共價鍵數為0.4NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘化亞銅(CuI)是陽極射線管復蓋物、也是重要的有機反應催化劑,不溶于水和乙醇。下圖是用廢銅電纜(雜質中含有少量鐵)制取無水碘化亞銅的流程。
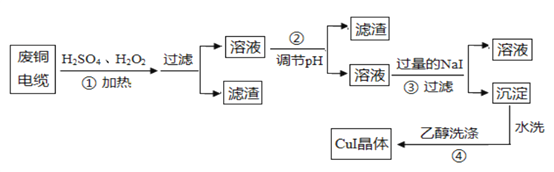
(1)過程①得到的溶液呈藍色,其原因是_______________________(用化學方程式表示),當溫度高于40℃時,反應的速度下降,原因是 _____________________ 。
(2)已知:Cu(OH)2的Ksp=2.2×10-20,Fe(OH)3的Ksp=2.16×10-39,lg6=0.78,過程②中用_____________調節溶液的pH值,
A.NaOH B.NH3·H2O C.CuO D.CuCO3
得到的濾渣成分是 __________ 。
(3)過程③的氧化產物能使淀粉變藍,對應的離子方程式為 ________________ 。
(4)過程④用乙醇洗滌的目的為 _____________________________ 。
(5)準確稱取m gCuI樣品,加入足量的Fe2(SO4)3溶液中,寫出該該反應的離子方程式____________________________________待樣品完全反應后,用a mol/L酸性KMnO4溶液滴定,達到終點時,消耗的體積平均值為Vml,則樣品中CuI的質量分數為 ____________ 。
(已知:5Fe2++MnO4- + 8H+ = 5Fe3+ + Mn2+ +4H2O)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高氯酸、硫酸、硝酸和鹽酸都是強酸,其酸性在水溶液中差別不大。以下是某溫度下這四種酸在冰醋酸中的電離常數:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
從以上表格中判斷以下說明中不正確的是( )
A. 在冰醋酸中這四種酸都沒有完全電離
B. 在冰醋酸中高氯酸是這四種酸中最強的酸
C. 在冰醋酸中硫酸的電離方程式為H2SO4===2H++SO42-
D. 水對于這四種酸的強弱沒有區分能力,但醋酸可以區分這四種酸的強弱
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com