
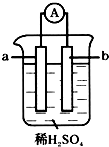
 已知在金屬活動性順序表中,a為排在氫前面的金屬.在如圖所示的裝置中,b為碳棒,關于此裝置的各種敘述中,不正確的是( )
已知在金屬活動性順序表中,a為排在氫前面的金屬.在如圖所示的裝置中,b為碳棒,關于此裝置的各種敘述中,不正確的是( )| A. | 碳棒上有氣體放出,溶液酸性變弱 | B. | a是正極,b是負極 | ||
| C. | 導線中有電子從a極到b極 | D. | a極上發生了氧化反應 |
分析 a的活動性比氫要強,b為碳棒,該裝置能自發的發生氧化還原反應而構成原電池,a作負極,碳棒作正極,負極上金屬失電子發生氧化反應,碳棒上氫離子得電子發生還原反應,電子從負極沿導線流向正極.
解答 解:A.該原電池中金屬作負極,碳棒b作正極,負極上金屬失電子發生氧化反應,正極碳上氫離子得電子發生還原反應,所以溶液中氫離子濃度減小,溶液的PH增大,故A正確;
B.該原電池中,金屬的金屬性大于氫元素,所以金屬a作負極,碳棒b作正極,故B錯誤;符合題意.
C.該裝置能構成原電池,所以有電流產生,電子從負極a沿導線流向正極b,故C正確;
D.a作負極,負極上失電子發生氧化反應,故D正確;
故選:B.
點評 本題考查了原電池工作原理.原電池中正負極的判斷不能僅憑金屬的活潑性判斷,要根據電極反應的反應類型、電子的流向等方面判斷.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:選擇題
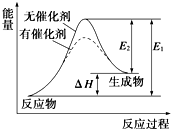 某反應的反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能).下列有關敘述正確的是( )
某反應的反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能).下列有關敘述正確的是( )| A. | 該反應為放熱反應 | |
| B. | 該反應的反應熱等于E1-E2 | |
| C. | 催化劑能改變該反應的焓變 | |
| D. | 逆反應的活化能大于正反應的活化能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
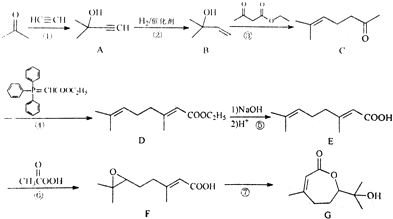
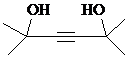 .
.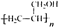 ,寫出合成流程圖(無機試劑任用).合成流程圖示例如下:
,寫出合成流程圖(無機試劑任用).合成流程圖示例如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該合金中銅與鎂的物質的量之比是2:1 | |
| B. | 可得到2.54 g沉淀 | |
| C. | 如果是銅鋁合金,則產生的NO2 的體積不會是1344mL | |
| D. | 恰好全部沉淀時,加入NaOH溶液的體積是600 mL |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將純水加熱到950C時,Kw變大,pH不變,水仍呈中性 | |
| B. | 向純水中加入稀氨水,平衡逆向移動,c(OH-)增大,Kw變小 | |
| C. | 向水中加入少量固體硫酸氫鈉,c(H+)增大,平衡逆向移動,KW不變 | |
| D. | 向水中通入HCl氣體,平衡逆向移動,溶液導電能力減弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,NaA溶液的pH=8,則c(Na+)-c(A-)=9.9×10-7 | |
| B. | pH=5.6的CH3COOH與CH3COONa混合溶液中,c(Na+)>(CH3COO-) | |
| C. | 0.1mol•L-1的NaHSO3的溶液中C(Na+)>C(HSO3-)>C(H+)>C(SO32-)>C(OH-) | |
| D. | 濃度均為0.1mol/L的 CH3COOH和CH3COONa溶液等體積混合:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “冰十六”的密度比液態水小 | B. | “冰十六”與干冰由不同分子構成 | ||
| C. | “冰十六”可以包合氣體分子 | D. | 液態水轉變成“冰十六”是化學變化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com