
��8�֣�ij�о��ԌW(xu��)��(x��)С�M����̽���������x��r���M(j��n)��������(sh��)�(y��n)��
��(sh��)�(y��n)һ ����һ�����|(zh��)������ȵĴ�����Һ
ȡ����������250mL 0.2000mol/L�Ĵ�����Һ����Ҫ�õ��IJ����x������Ͳ���������������� �� ��
��(sh��)�(y��n)�� ̽����Ȍ�(du��)������x�̶ȵ�Ӱ�
��0.2000mol/L�Ĵ�����Һϡጳ������ȵ���Һ������pHӋ(j��)�y��25��r(sh��)��ͬ��ȵĴ����pH,�Y(ji��)�����£�
|
������(mol/L) |
0.0010 |
0.0100 |
0.0200 |
0.1000 |
0.2000 |
|
pH |
3.88 |
3.38 |
3.23 |
2.88 |
2.73 |
�ش����І��}��
��1������(j��)���Д�(sh��)��(j��)�����Եó���������늽��|(zh��)�ĽY(ji��)Փ�����J(r��n)��ó��˽Y(ji��)Փ������(j��)��
��
��2���ı��еĔ�(sh��)��(j��)��߀���Եó���һ�Y(ji��)Փ���S�������ȵĜpС���������x�̶�
����������pС����׃����
��(sh��)�(y��n)һ �z�^�ιܣ�2�֣���250mL����ƿ��2�֣�
��(sh��)�(y��n)�� (1)0.0100mo1/L�����pH����2�����ϡ�10���r(sh��)��pH��׃��ֵС��l��2�֣�
(2)����2�֣�
����������(sh��)�(y��n)һ������һ�����|(zh��)���������Һ�����ƣ�����(j��)�����^�̿�֪��߀ȱ�� �z�^�ιܡ�250mL����ƿ��
��(sh��)�(y��n)�� (1)����(j��)��(sh��)��(j��)��֪��0.0100mo1/L�����pH����2���f����Һ�К��x�ӵĝ��С��0.0100mo1/L����������xƽ�⡣
��2������(j��)��(sh��)��(j��)��֪������ϡ�10���r(sh��)��pH��׃��ֵС��l���@�f���S�������ȵĜpС���������x�̶�������ġ�


 ���}���ϵ�д�
���}���ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���x����
| ||
| ||
| ||
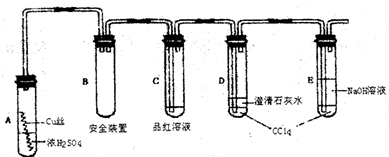
 Cu��OH��2+2H+
Cu��OH��2+2H+ Cu��OH��2+2H+
Cu��OH��2+2H+�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���x����
 �����FƤ�������^��(qi��ng)�����g�ԣ������a(ch��n)�г��õĽ��ٲ���֮һ����\�Ӫq���FƤ�ı��o(h��)�ӣ��@��Ĥ�ĺ�ȼ������Ҳ�����Д�僌��|(zh��)������Ҫָ��(bi��o)��ij�о��ԌW(xu��)��(x��)С�M���˜y����\�FƤ�ĺ�ȣ��O(sh��)Ӌ(j��)������Č�(sh��)�(y��n)������
�����FƤ�������^��(qi��ng)�����g�ԣ������a(ch��n)�г��õĽ��ٲ���֮һ����\�Ӫq���FƤ�ı��o(h��)�ӣ��@��Ĥ�ĺ�ȼ������Ҳ�����Д�僌��|(zh��)������Ҫָ��(bi��o)��ij�о��ԌW(xu��)��(x��)С�M���˜y����\�FƤ�ĺ�ȣ��O(sh��)Ӌ(j��)������Č�(sh��)�(y��n)������
| ||
| 2S��7.14 |
| ||
| 2S��7.14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
| A���Vֻ�cFeCl3��Һ�е�Fe3+ֱ�ӷ���(y��ng) | B���������V�cFeCl3��Һ�е�ˮֱ�ӷ���(y��ng)�a(ch��n)���� | C���t��ɫ�������V�cˮ����(y��ng)���ɵ�Mg��OH��2�cFe3+����(y��ng)���� | D���������V�cFeCl3ˮ�����ɵ��}�ᷴ��(y��ng)�a(ch��n)���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
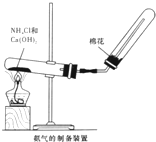 ij�о��ԌW(xu��)��(x��)С�M������ȡ�����̽����������P(gu��n)���|(zh��)���M(j��n)�������Ќ�(sh��)�(y��n)��
ij�о��ԌW(xu��)��(x��)С�M������ȡ�����̽����������P(gu��n)���|(zh��)���M(j��n)�������Ќ�(sh��)�(y��n)���鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com