

D
解析:溶液的導電能力的強弱與溶液中所含有的能自由移動的離子的濃度大小有關。
(NH4)2SO4和Ba(OH)2都是強電解質,在溶液中雖完全電離,但它們相互反應生成難電離的NH3·H2O和難溶的BaSO4,故滴加過程中,原溶液中的c(![]() )和c(
)和c(![]() )均逐漸減小;當滴加Ba(OH)2溶液20 mL時,反應完全,離子濃度最小,溶液導電能力最弱;再繼續滴加Ba(OH)2溶液,不再發生反應,隨著Ba2+和OH-兩種離子濃度的增大,溶液的導電能力逐漸增加。但由于后加入Ba(OH)2與原(NH4)2SO4的物質的量濃度相等(準確來說,應是電荷濃度相等),且受到恰好反應時所得40 mL稀氨水溶液的稀釋,故最后得到溶液的導電能力應該比最初的20 mL 0.5 mol·L-1 (NH4)2SO4溶液的導電能力差。
)均逐漸減小;當滴加Ba(OH)2溶液20 mL時,反應完全,離子濃度最小,溶液導電能力最弱;再繼續滴加Ba(OH)2溶液,不再發生反應,隨著Ba2+和OH-兩種離子濃度的增大,溶液的導電能力逐漸增加。但由于后加入Ba(OH)2與原(NH4)2SO4的物質的量濃度相等(準確來說,應是電荷濃度相等),且受到恰好反應時所得40 mL稀氨水溶液的稀釋,故最后得到溶液的導電能力應該比最初的20 mL 0.5 mol·L-1 (NH4)2SO4溶液的導電能力差。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
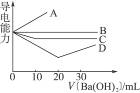
向20 mL 0.5 mol·L-1(NH4)2SO4溶液中逐滴加入0.5 mol·L-1 Ba(OH)2溶液,整個滴加過程中混合溶液的導電能力的變化基本符合下圖中的( )
查看答案和解析>>
科目:高中化學 來源:2012-2013學年遼寧省五校協作體高三(上)期中化學試卷(解析版) 題型:選擇題
查看答案和解析>>
科目:高中化學 來源: 題型:
下列離子方程式與所述事實相符且正確的是
A.0.5 mol/L NaHSO4與0.5 mol/L Ba(OH)2混合至溶液呈中性:
Ba2++OH—+SO42—+H+=BaSO4↓+H2O
B.向2 mol/L Fe(NO3)2(aq)中滴加少量氫碘酸:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O
C.向20 mL 0.5 mol/L FeBr2(aq)中通入224 mL Cl2(標準狀況):
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl—
D.向30 mL 0.5 mol/L NaOH(aq)中通入224 mL CO2(標準狀況):
3OH—+2CO2=CO32—+HCO3—+H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com