
(1)寫出下列物質的化學式:
A_______________________________________,E____________________________________。

(2)寫出下列反應的化學方程式:
反應①__________________________________________。
反應⑤__________________________________________。
(3)寫出下列反應的離子方程式:
反應②__________________________________________。
反應④__________________________________________。
科目:高中化學 來源:安徽省模擬題 題型:填空題
 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1 2SO2+O2 在550 ℃時的平衡常數K=_________。 A、B表示不同壓強下的平衡轉化率,通常工業生產中采用常壓的原因是:__________________,并比較不同壓強下的平衡常數:K(0.10 MPa) _________K(1.0 MPa)(填 “<”或“>”或“=”)。
2SO2+O2 在550 ℃時的平衡常數K=_________。 A、B表示不同壓強下的平衡轉化率,通常工業生產中采用常壓的原因是:__________________,并比較不同壓強下的平衡常數:K(0.10 MPa) _________K(1.0 MPa)(填 “<”或“>”或“=”)。 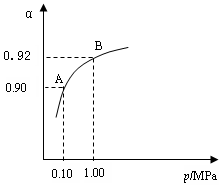
查看答案和解析>>
科目:高中化學 來源:浙江省模擬題 題型:填空題
 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1 2SO2+O2 在550 ℃時的平衡常數K=_________。 A、B表示不同壓強下的平衡轉化率,通常工業生產中采用常壓的原因是:__________________,并比較不同壓強下的平衡常數:K(0.10 MPa) _________K(1.0 MPa)(填 “<”或“>”或“=”)。
2SO2+O2 在550 ℃時的平衡常數K=_________。 A、B表示不同壓強下的平衡轉化率,通常工業生產中采用常壓的原因是:__________________,并比較不同壓強下的平衡常數:K(0.10 MPa) _________K(1.0 MPa)(填 “<”或“>”或“=”)。 

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com