
氮元素可以形成多種化合物。回答以下問題:
(1)基態氮原子的價電子排布式是 。
(2)C、N、O三種元素第一電離能從大到小的順序是 。
(3)(N2H4)分子可視為NH3分子中的一個氫原子被—NH2(氨基)取代形成的另一種氮的氫化物。
①N2H4分子中氮原子軌道的雜化類型是 。
②肼可用作火箭燃料,燃燒時發生的反應是:N2O4(1)+2N2H4(l) 3N2(g)+4H2O(g)△H= —103 8.7kJ.mol—1,若該反應中有4mol
N—H鍵斷裂,則形成的
3N2(g)+4H2O(g)△H= —103 8.7kJ.mol—1,若該反應中有4mol
N—H鍵斷裂,則形成的 鍵有 mol。
鍵有 mol。
③肼能與硫酸反應生成N2H6SO4,N2H6SO4晶體類型與硫酸銨相同,則N2H6SO4的晶體內不存在 (填標號)
a.離子鍵 b.共價鍵 c.配位鍵 d.范德華力
(4)氮化硼(BN)是一種重要的功能陶瓷材料,在與石墨結構相似的六方氮化硼晶缽中,層內B原子與N原子之間的化學鍵為___ 。
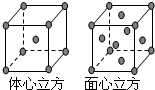
(5)六方氮化硼在高溫高壓下,可以轉化為立方氮化硼,其結構與金剛石相似,硬度與金剛石相當,晶胞邊長為3.615×l0—10m,立方氮化硼晶胞中含有 個氮原子、 個硼原子,立方氮化硼的密度是 g.cm一3(只要求列算式,不必計算出數值,阿伏伽德羅常數為NA)
(1)2s22p3 (2分)
(2)N>O>C(2分)
(3)①sp3 (2分) ②3 (2分) ③d(2分)
(4)共價鍵(1分)
(5)4(1分) 4(1分)  (2分)
(2分)
【解析】
試題分析:(2)C、N、O三種元素中氮原子最外層電子處于半滿的相對穩定狀態,第一電離能較大大于相鄰的元素原子,故第一電離能從大到小的順序N>O>C;(3)①N2H4分子中氮原子形成3個公用電子對,故為sp3 雜化;②若該反應中有4mol N—H鍵斷裂,則生成1。5mol氮氣,共含有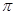 鍵有 3mol;③硫酸銨含有離子鍵、共價鍵、配位鍵,N2H6SO4的晶體內也應含有;(5)立方氮化硼晶胞結構與金剛石相似,故含有4氮原子,4個硼原子,立方體的質量為(14+11)×4÷NA,
鍵有 3mol;③硫酸銨含有離子鍵、共價鍵、配位鍵,N2H6SO4的晶體內也應含有;(5)立方氮化硼晶胞結構與金剛石相似,故含有4氮原子,4個硼原子,立方體的質量為(14+11)×4÷NA,
密度為(14+11)×4/(3.615×l0—10)3NA
考點:考查物質結構與性質有關問題。


科目:高中化學 來源: 題型:
 氮元素可以形成多種化合物.
氮元素可以形成多種化合物.+ 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 I:氮元素可以形成多種化合物.回答以下問題:
I:氮元素可以形成多種化合物.回答以下問題:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com