
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素原子個數比 | A和C 1:1 | B和A 1:X | D和E 1:3 | B和E 1:4 |
 ;
;分析 原子序數依次增大的A、B、C、D、E五種短周期主族元素,B原子最外層電子數比其次外層電子數多2個,原子只能有2個電子層,最外層電子數為4,則B為碳元素;A、B兩種原子的核電荷數之差等于它們的原子最外層電子數之和,二者不可能同周期,A的原子序數小于碳,只能處于第一周期,可推知A為H元素;D和E的原子序數之和為30,二者只能處于第三周期,為Al與Cl或Si與S,且D、E形成的化合物丙中D:E=1:3,則D為Al、E為Cl;C是E的鄰族元素,C的原子序數小于鋁,則C為氧元素,可推知甲為H2O2,丙為AlCl3,丁為CCl4,若有機物乙的分子為平面結構,碳氫鍵鍵角為120°,當X=2時,乙為C2H4,當X=1時,乙為苯.
解答 解:原子序數依次增大的A、B、C、D、E五種短周期主族元素,B原子最外層電子數比其次外層電子數多2個,原子只能有2個電子層,最外層電子數為4,則B為碳元素;A、B兩種原子的核電荷數之差等于它們的原子最外層電子數之和,二者不可能同周期,A的原子序數小于碳,只能處于第一周期,可推知A為H元素;D和E的原子序數之和為30,二者只能處于第三周期,為Al與Cl或Si與S,且D、E形成的化合物丙中D:E=1:3,則D為Al、E為Cl;C是E的鄰族元素,C的原子序數小于鋁,則C為氧元素,可推知甲為H2O2,乙為C2H4,丙為AlCl3,丁為CCl4.
(1)化合物甲為H2O2,電子式為 ,故答案為:
,故答案為: ;
;
(2)若有機物乙的分子為平面結構,碳氫鍵鍵角為120°,當X=2時,乙為C2H4,結構簡式為CH2=CH2,當X=1時,乙為苯,乙的二氯代物結構有鄰、間、對3種,故答案為:CH2=CH2;3.
點評 本題考查元素化合物推斷,充分利用短周期元素、核外電子排布特點、化合物中原子數目之比進行推斷,難度中等.


 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:選擇題
| 實驗序號 | 甲 | 乙 | 丙 |
| 合金質量/mg | 510 | 770 | 918 |
| 氣體體積/mL | 560 | 672 | 672 |
| A. | 甲組和乙組的實驗中,鹽酸均是過量的 | |
| B. | 鹽酸的物質的量濃度為0.8 mol/L | |
| C. | 合金中鎂鋁的物質的量之比為1:1 | |
| D. | 丙組中鋁的物質的量為0.009 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 溶液中溶質的質量分數 | B. | 溶液中陽離子數目 | ||
| C. | 溶液的質量 | D. | 濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5:4 | B. | 4:5 | C. | 5:12 | D. | 12:5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
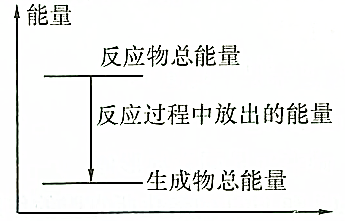
| A. | 反應過程中的能量關系可用如圖表示 | |
| B. | 1mol鋅所含的能量高于1mol H2 所含的能量 | |
| C. | 若將其設計為原電池,則鋅為正極 | |
| D. | 若將其設計為原電池,當有32.5g鋅溶解時,正極放出氣體一定為11.2L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化碳氣體通入氨水中 | B. | 二氧化硫氣體通入澄清石灰水中 | ||
| C. | 五氧化二磷投入堿溶液中 | D. | 二氧化硅投入燒堿溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將機動車尾氣排放標準從國家Ⅱ號標準提高到國家Ⅲ號標準 | |
| B. | 采用強氧化劑將SO2氧化為SO3再排放到大氣中 | |
| C. | 采用原煤脫硫技術,降低燃煤中硫的含量 | |
| D. | 向燃煤中加入適量石灰石,減少燃燒產物中SO2的量 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com