
把19.2 g 的Cu放入足量的稀硝酸中,微熱至Cu完全反應。
已知:3Cu + 8HNO3(稀) = 3Cu(NO3)2 +2NO↑+ 4H2O求:
(1)參加反應的硝酸的物質的量;
(2)被還原的硝酸的質量;
(3)生成的NO在標準狀況下的體積。
(1)0.8mol (2)12.6g (3)4.48L
解析試題分析:19.2g 的Cu的物質的量為 =0.3mol,
=0.3mol,
(1)設參加反應的硝酸的物質的量為x
3Cu+8HNO3(稀)=3Cu(NO3)2 +2NO↑+4H2O
3mol 8mol
0.3mol x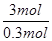 =
=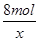
x=0.8mol,
答案:參加反應的硝酸的物質的量為0.8mol.
(2)由方程式可以看出,硝酸沒有全部被還原,當有8mol硝酸反應時,有2mol被還原,
則0.8mol硝酸參加反應,被還原的硝酸的物質的量為0.2mol,質量為:0.2mol×63g·mol-1=12.6g.答案:12.6g;
(3)設產生的NO在標準狀況下的體積為V,則
3Cu+8HNO3(稀)=3Cu(NO3)2 +2NO↑+4H2O
3mol 44.8L
0.3mol V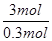 =
=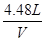
V=4.48L,
答案:產生的NO在標準狀況下的體積為4.48L
考點:化學方程式的有關計算


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源: 題型:填空題
水是組成生命體的重要物質,有關水的反應實例有很多。
(1)有人設想將太陽能轉化為電能,進而將水電解生成氫氣,氫氣是一種清潔能源。請分析電解水的過程中,水是_____________(填僅被氧化,僅被還原,既被氧化又被還原,既不被氧化又不被還原)
(2)野營愛好者攜帶氫化鈣固體作為生氫劑,方程式為CaH2+2H2O=Ca(OH)2+2H2↑,其中水是_____________(填僅被氧化,僅被還原,既被氧化又被還原,既不被氧化又不被還原)
(3)在下列反應中水只被還原的是_____________(填序號)
| A.C+H2O=CO+H2 | B.CaO+H2O=Ca(OH)2 |
| C.3Fe+4H2O=Fe3O4+4H2 | D.3NO2+H2O=2HNO3+NO |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某高溫還原法制備新型陶瓷氮化鋁(AlN)的反應體系中的物質有:Al2O3.C.N2.AlN.CO
(1)請將AlN之外的反應物與生成物分別填入以下空格內,配平,并標出電子轉移的方向和數目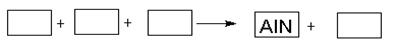
(2)若反應中共轉移3.01 ×1023個電子,則該反應產生氣體的體積為: (標準狀況下)
(3)氮化鋁也能由氯化鋁與氨氣經氣相反應制得:AlCl3+NH3  AlN+3HCl反應中,該方法比前者在生產上更具優勢。下列說法中,正確的是 。
AlN+3HCl反應中,該方法比前者在生產上更具優勢。下列說法中,正確的是 。
A.前一方法中的 Al2O3.C.N2結構穩定,反應時破壞化學鍵需要消耗更多的能量
B.前一方法中的Al2O3和C容易殘留在氮化鋁中
C.兩種方法中氮化鋁均為還原產物
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2013年初,霧霾天氣多次肆虐我國中東部,該地區PM2.5嚴重超標。研究表明,PM2.5約60%來源于某些氣體污染物在空氣中轉變而成的二次顆粒物。這些氣體污染物主要有二氧化硫、氮氧化物、氨氣、揮發性有機物。因此,控制、治理PM2.5污染源成為環保的重要課題。
(1)研究表明,TiO2在紫外線照射下會使空氣中的某些分子產生活性基團OH,如圖所示,OH與NO2的反應為NO2+OH HNO3。寫出OH與NO反應的化學方程式:_____________,該反應中被氧化的元素是 。
HNO3。寫出OH與NO反應的化學方程式:_____________,該反應中被氧化的元素是 。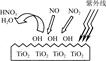
(2)如圖所示的電解裝置能吸收和轉化NO2、NO和SO2。陰極排出的溶液中含S2O42-離子,能吸收NOx氣體,生成的SO32-可在陰極區再生。請將S2O42-吸收NO2的離子方程式配平,并標明電子轉移的方向和數目。
____S2O42-+____NO2+____OH- SO32-+____N2+____
SO32-+____N2+____
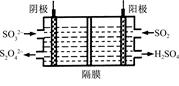
(3)已知上述電解裝置陽極反應為:SO2-2e-+2H2O SO42-+4H+,陰極生成的吸收液每吸收標準狀況下7.84 L的氣體,陽極區新生成質量分數為49%的硫酸100 g,則被吸收氣體中NO2和NO的物質的量之比為 。
SO42-+4H+,陰極生成的吸收液每吸收標準狀況下7.84 L的氣體,陽極區新生成質量分數為49%的硫酸100 g,則被吸收氣體中NO2和NO的物質的量之比為 。
(4)PM2.5產生的主要來源是日常發電、工業生產、汽車尾氣排放等過程中經過燃燒而排放的殘留物,大多含有重金屬等有毒物質。一般而言,粒徑2.5微米至10微米的粗顆粒物主要來自揚塵等;2.5微米以下的細顆粒物(PM2.5)則主要來自化石燃料的燃燒(如機動車尾氣、燃煤)、揮發性有機物的排放等。請你結合信息,給出降低PM2.5排放的對策(至少兩條): ______ 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
鐵及其化合物之間的相互轉化可用下式表示:
回答下列有關問題:
(1)鐵元素位于元素周期表的第四周期第Ⅷ族,原子序數是26,最外層有2個電子。元素鐵的原子結構示意圖是 。
(2)檢驗硫酸鐵溶液中是否存在Fe2+的方法是
(3)
(4)高鐵酸鈉(Na2FeO4)是水處理過程中使用的一種新型凈水劑,它的氧化性比高錳酸鉀強,其本身在反應中被還原為Fe3+。Na2FeO4之所以能凈水,除了能消毒殺菌外,另一個原因是(結合離子方程式說明) 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
將25.6g銅與含0.3molH2SO4的濃硫酸充分反應,(1)若在反應過程中消耗了0.2mol的H2SO4,則生成的氣體標況下體積為多少?(2)若以上反應產生的氣體全部逸出后,繼續在剩余物質中加入2mol/L的稀硝酸100ml,充分反應后產生NO的物質的量為多少?
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
將高碘酸H5IO6加入MnSO4溶液中可使溶液呈紫紅色,已知H5IO6在反應中發生如下過程:H5IO6→HIO3。完成下列填空:
(1)將該反應的氧化劑、還原劑及配平后的系數填入正確位置。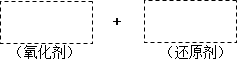
(2)在上圖中標明電子轉移的方向和數目。
(3)若向H5IO6溶液中加入足量的下列物質,能將碘元素還原成碘離子的是____(選填序號)。
a. 鹽酸 b. 硫化氫 c. 溴化鈉 d. 硫酸亞鐵
(4)若向含1mol H5IO6的溶液中加入過量的過氧化氫溶液,再加入淀粉溶液,溶液變藍,同時有大量氣體產生。請寫出此反應的化學方程式:________________________________,此過程中至少可得到氣體_________L(標準狀態下)。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
為驗證鹵素單質氧化性的相對強弱,某小組用下圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗)。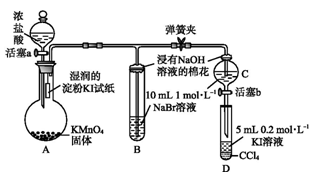
實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ.當B中溶液由黃色變為棕紅色時,關閉活塞a。
Ⅳ.……
(1)A中產生黃綠色氣體,其化學方程式是 。
(2)驗證氯氣的氧化性強于碘的實驗現象是 。
(3)B中溶液發生反應的離子方程式是 。
(4)為驗證溴的氧化性強于碘,過程Ⅳ的操作和現象是 。
(5)過程Ⅲ實驗的目的是 。
(6)氯、溴、碘單質的氧化性逐漸減弱的原因:同主族元素從上到下 ,得電子能力逐漸減弱。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
25℃、101kPa下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s) △H2=-511kJ·mol-1
下列說法正確的是( )
| A.①和②產物的陰陽離子個數比不相等 |
| B.①和②生成等物質的量的產物,轉移電子數不同 |
| C.常溫下Na與足量O2反應生成Na2O,隨溫度升高生成Na2O的速率逐漸加快 |
| D.25℃、101kPa下,Na2O2(s)+2Na(s)=2Na2O(s) △H=-317kJ·mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com