
下列各組離子能在水溶液中大量共存的是
A.Ca2+、SO42-、H+、HCO3- B.H+、NO3-、Cl-、SiO32-
C.K+、Fe2+、H+、NO3- D.K+、Na+、CO32-、SiO32-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2017屆貴州省高三模擬四化學卷(解析版) 題型:實驗題
用軟錳礦(MnO2)、黃鐵礦(FeS2)酸浸生產硫酸錳(MnSO4),并進一步電解制取二氧化錳(EMD)的工藝流程如下:
I. 將軟錳礦、黃鐵礦和硫酸按一定比例放入反應釜中,攪拌,加熱保溫反應一定時間。
II. 向反應釜中加入MnO2、CaCO3試劑,再加入Na2S溶液除掉浸出液中的重金屬。
III. 過濾,向濾液中加入凈化劑進一步凈化,再過濾,得到精制MnSO4溶液。
IV. 將精制MnSO4溶液送入電解槽,電解制得EMD。
請回答下列問題:
(1)步驟I中攪拌、加熱的目的是 。完成酸浸過程中反應的離子方程式:
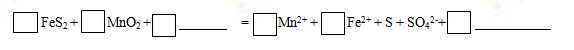
(2) 加入CaCO3將浸出液pH調至pH=5,從而除掉鐵,請解釋用CaCO3除鐵的原理: 。(結合離子方程式解釋)
(3)步驟IV中用如圖所示的電解裝置電解精制的MnSO4溶液,生成EMD的是
極(填“a”或“b”),生成EMD的電極反應式是 。
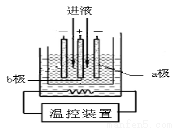
(4)EMD可用作堿性鋅錳電池的材料。已知堿性鋅錳電池的反應式為:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。
下列關于堿性鋅錳電池的說法正確的是 (填字母序號)。[來源
A.堿性鋅錳電池是二次電池
B.堿性鋅錳電池將化學能轉化為電能
C.正極反應為:2MnO2+2H2O+2e-=2MnOOH+2OH-
D.堿性鋅錳電池工作時,電子由MnO2經外電路流向Zn極
查看答案和解析>>
科目:高中化學 來源:2017屆天津市高三上月考三化學試卷(解析版) 題型:選擇題
類比推理的方法在化學學習與研究中有廣泛的應用,但有時會得出錯誤的結論。以下幾種類比推理結論中正確的是
A. H2SO4為強酸,推出HC1O4為強酸
B. Fe3Cl8可以改寫為FeCl2·2FeCl3,推出 Fe3I8 可以改寫為 FeI2·2FeI3
C. NH3 的沸點高于PH3,推出CH4 沸點高于SiH4
D. CO2通入Ba(NO3)2 溶液中無沉淀生成,推出SO2通入Ba(NO3)2 溶液中無沉淀生成
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考二化學卷(解析版) 題型:實驗題
CuCl晶體呈白色,熔點為430℃,沸點為1490℃,見光分解,露置于潮濕空氣中易被氧化,難溶于水、稀鹽酸、乙醇,易溶于濃鹽酸生成H3CuCl4,反應的化學方程式為CuCl(s)+3HCl(aq)  H3CuCl4(aq)。
H3CuCl4(aq)。
(1)實驗室用下圖所示裝置制取CuCl,反應原理為:
2Cu2++SO2+8Cl-+2H2O=2CuCl43-+SO42-+4H+
CuCl43-(aq) CuCl(s)+3Cl-(aq)
CuCl(s)+3Cl-(aq)
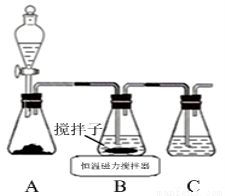
①裝置C的作用是 。
②裝置B中反應結束后,取出混合物進行如下圖所示操作,得到CuCl晶體。

操作ⅱ的主要目的是 ;操作ⅳ中宜選用的試劑是 。
③實驗室保存新制CuCl晶體的方法是 。
④欲提純某混有銅粉的CuCl晶體,請簡述實驗方案: 。
(2)某同學利用如下圖所示裝置,測定高爐煤氣中CO、CO2、N2和O2的百分組成。
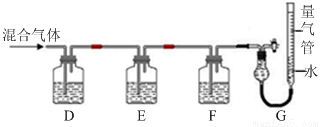
已知:i.CuCl的鹽酸溶液能吸收CO形成Cu(CO)Cl·H2O。
ii.保險粉(Na2S2O4)和KOH的混合溶液能吸收氧氣。
D、F洗氣瓶中宜盛放的試劑分別是 、 。
②寫出保險粉和KOH的混合溶液吸收O2的離子方程式: 。
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考二化學卷(解析版) 題型:選擇題
向27.2gCu和Cu2O的混合物中加入某濃度的稀硝酸0.5L,固體物質完全反應,生成NO和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此時溶液呈中性,金屬離子已完全沉淀,沉淀質量為39.2g。下列有關說法不正確的是
A.Cu與Cu2O 的物質的量之比為2:1
B.硝酸的物質的量濃度為2.6mol/L
C.產生的NO在標準狀況下的體積為4.48L
D.Cu、Cu2O與硝酸反應后剩余HNO3為0.2mol
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上適應性訓練四化學卷(解析版) 題型:實驗題
【化學—選修5:有機化學基礎】
污染物的有效去除和資源的充分利用是化學造福人類的重要研究課題。某研究小組利用軟錳礦(主要成分為MnO2,另含有少量鐵、鋁、銅、鎳等金屬化合物)作脫硫劑,通過如下簡化流程既脫除燃煤尾氣中的SO2,又制得電池材料MnO2(反應條件已省略)。
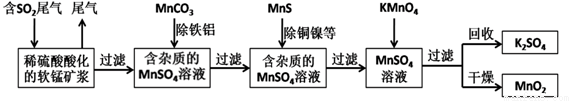
請回答下列問題:
(1)上述流程中多次設計到過濾操作,實驗室進行過濾操作時需要用到的硅酸鹽儀器有玻璃棒、燒杯,_______________;其中玻璃棒的作用是___________________。
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是_____________(只用文字表述)
(3)工業上采用電解K2MnO4水溶液的方法來生產KMnO4,其中惰性電極作陽極,鐵作陰極,請寫出陽極的電極反應式__________________。
(4)下列各組試劑中,能準確測定一定體積燃煤尾氣中SO2含量的是__________。(填編號)
a.NaOH溶液、酚酞試液 b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液 d.氨水、酚酞試液
(5)廢氣中SO2與稀硫酸酸化的軟錳礦反應的化學方程式為_______________;已知廢氣中SO2濃度為6.4g/m3,軟錳礦漿對SO2的吸收率可達90%,則處理1000m3燃煤尾氣,可得到硫酸錳晶體(MnSO4·H2O,相對分子質量為169)質量為_________________kg(結果保留3 位有效致字)。
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上適應性訓練四化學卷(解析版) 題型:選擇題
向Na2CO3、NaHCO3混合溶液中逐滴加入稀鹽酸,生成氣體的量隨鹽酸加入量的變化關系如圖所示。則下列離子組在對應的溶液中,一定能大量共存的是
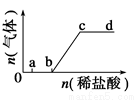
A.a點對應的溶液中:Na+、OH-、SO42-、NO3-
B.b點對應的溶液中:Al3+、Fe3+、NO3-、Cl-
C.c點對應的溶被中:Na+、Ca2+、NO3-、Cl-
D.d點對應的溶液中:Fe2+、Na+、Cl- 、 NO3-
查看答案和解析>>
科目:高中化學 來源:2016-2017學年吉林長春外國語學校高一上期末文化學卷(解析版) 題型:填空題
不能用帶磨口玻璃塞試劑瓶存放堿(如NaOH)溶液和Na2SiO3溶液,應用橡皮塞原因:
查看答案和解析>>
科目:高中化學 來源:2016-2017學年吉林長春外國語學校高一上期末理化學卷(解析版) 題型:選擇題
下列關于液氯和氯水的敘述中正確的是( )
A.液氯較氯水的漂白作用更強 B.液氯與氯水均有酸性
C.液氯是純凈物,氯水是混合物 D.液氯是無色的,氯水呈黃綠色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com