
【題目】下列反應的離子方程式書寫正確的是
A. 金屬鋁溶于稀硫酸中:Al+2H+=Al3++H2↑
B. 銅片溶于稀硝酸產生無色氣體:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
C. 向NaClO溶液中通入過量的SO2:ClO-+SO2+H2O=HClO+HSO3-
D. 用惰性電極電解CuSO4溶液:2Cu2++2H2O![]() 2Cu+4H++O2↑
2Cu+4H++O2↑
科目:高中化學 來源: 題型:
【題目】過氧化尿素是一種新型漂泊、消毒劑,廣泛應用與農業、醫藥、日用化工等領域。用低濃度的雙氧水和飽和尿素溶液在一定條件下可以合成過氧化尿素。反應的方程式為:
CO(NH2)2+H2O2![]() CO(NH2)2·H2O2。過氧化尿素的部分性質如下:
CO(NH2)2·H2O2。過氧化尿素的部分性質如下:
分子式 | 外觀 | 熱分解溫度 | 熔點 | 溶解性 |
CO(NH2)2·H2O2 | 白色晶體 | 45℃ | 75~85℃ | 易溶于水、有機溶劑 |
合成過氧化尿素的流程及反應裝置圖如圖:

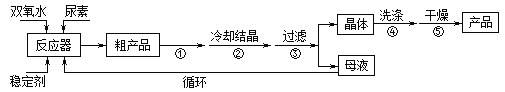
請回答下列問題:
(1)儀器X的名稱是__________;冷凝管中冷卻水從____(填“a”或“b”)口出來;
(2)該反應的溫度控制30℃而不能過高的原因是_______________________。
(3)步驟①宜采用的操作是_____________。
A.加熱蒸發 B.常壓蒸發 C.減壓蒸發
(4)若實驗室制得少量該晶體,過濾后需要用冷水洗滌,具體的洗滌操作是_________________。
(5)準確稱取1.000g產品于250mL錐形瓶中,加適量蒸餾水溶解,再加2mL6mol·L﹣1H2SO4,用0.2000mol·L﹣1KMnO4標準溶液滴定至終點時消耗18.00mL(尿素與KMnO4溶液不反應),則產品中CO(NH2)2·H2O2的質量分數為_____________;若滴定后俯視讀數,則測得的過氧化尿素含量________(填“偏高”、“偏低”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關物質性質、用途的說法都正確的是
A. 硅晶體是良好的半導體,可用于制造光導纖維
B. 高壓鈉燈發出的黃光透霧能力強,可用于道路和廣場照明
C. 生石灰能與水反應,可用于除去CO2氣體中少量的水蒸氣
D. 碳酸鈉具有堿性,可用于治胃酸中和劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組物質中,第一種是電解質,第二種是分散系,第三種是合金的是 ( )
A. 硫酸、CuSO4·5H2O、生鐵 B. 酒精、空氣、銅綠
C. 二氧化碳、明礬、熟石灰 D. 硝酸鉀、食鹽水、黃銅
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“神舟七號”的燃料是氫化鋰三兄弟:LiH、LiD、LiT。其中Li的質量數為7,則對相同物質的量的這三種物質的下列說法正確的是( )
A. 質子數之比為1:2:3 B. 中子數之比為1:1:1
C. 摩爾質量之比為8:9:10 D. 化學性質不相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水合肼(N2H4·H2O)又稱水合聯氨,其純凈物為無色透明的油狀液體,具有強堿性和吸濕性。將水合肼通入CuO膠體中,可發生如圖所示的轉化。

(1)圖示的轉化中,②屬于_____________(填“非氧化還原反應”或“氧化還原反應”)。
(2)轉化①中,氧化劑與還原劑的物質的量之比為4: l ,則X的化學式為_____。
(3)轉化②中,反應一段時間后,溶液中n(OH-)____________(填“增大”“ 減小” 或“不變”)。
(4)若①中參加反應的CuO物質的量為0.4mol,按圖示轉化過程進行后,④中生成的CuO物質的量也等于0.4mol,則③中參加反應的O2的物質的量與④中今加反應的NaClO的物質的量之比為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于物質的用途不合理的是
A. SiO2可用于制造光導纖維 B. 活性炭可用作除味劑
C. 濃硫酸可用于干燥堿性物質 D. NH4Cl可用作氮肥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮是重要的非金屬元素,可以形成多種化合物。回答以下問題:
(1)基態氮原子的電子排布式是________________。C、N、O三種元素第一電離能從大到小的順序是____________________。
(2)肼(N2H4)分子可視為NH3分子中的一個氫原子被-NH2(氨基)取代形成的另一種氮的氫化物。
①NH3分子的空間構型是________________________;N2H4分子中氮原子軌道的雜化類型是____________________。
②肼可用作火箭燃料,燃燒時發生的反應是:
N2O4(1)+2N2H4(1)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若該反應中有4molN-H鍵斷裂,則形成的π鍵有_________mol。
③肼能與硫酸反應生成N2H6SO4。N2H6SO4晶體類型與硫酸銨相同,則N2H6SO4的晶體內不存在__________(填標號)
a.離子鍵 b.共價鍵 c.配位鍵 d.范德華力
(3)(CH3)3NH+和AlCl4-形成離子液體。離子液體由陰、陽離子組成,熔點低于100℃,其揮發性一般比有機溶劑___________(填“大”或“小”),可用作____________(填代號)。
a.助燃劑 b.“綠色”溶劑
c.復合材料 d.絕熱材料
(4)X+中所有電子正好充滿K、L、M三個電子層,它與N3-形成的晶體結構如圖所示。X的元素符號是___________,與同一個N3-相連的X+有_________個。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com