
| 污染指數 | 首要污染物 | 空氣質量等級 | 空氣質量狀況 |
| 55 | SO2 | Ⅱ | 良 |



科目:高中化學 來源: 題型:閱讀理解
| 城市 | 污染指數 | 首要污染物 | 空氣質量級別 | 空氣質量狀況 |
| 甲 | 55 | SO2 | II | 良 |

查看答案和解析>>
科目:高中化學 來源: 題型:
空氣質量越來越愛到人們的關注,下表是部分城市某日的空氣質量報告:
| 城市 | 污染指數 | 首要污染物 | 空氣質量級別 | 空氣質量狀況 |
| 北京 | 89 | NOx | Ⅱ | 良 |
| 上海 | 49 | — | Ⅰ | 優 |
| 寧波 | 55 | SO2 | Ⅱ | 良 |
| 克拉瑪依 | 106 | PM10 | Ⅲ1 | 輕微污染 |
(1)由上表可知,在上述城市中,容易出現酸雨的城市有: ;空氣質量最差的成都市是: 。
(2)可吸入顆粒(PM10)又稱為飄塵,它與空氣中的SO2、O2接觸時,使部分的SO2轉化為SO3,使空氣酸度增加,形成酸雨。飄塵所起的主要作用是( )。
A.氧化劑 B.還原劑 C.吸附劑 D.催化劑
(3) 汽車排放的尾氣、硝酸和化肥廠等工廠排出的廢氣中都含有氮氧化物,氮氧化物溶于水最終轉化為 ,這也是造成酸雨的另一個主要原因。
(4) 酸雨可導致下列哪種危害( )
A.腐蝕建筑物 B.導致樹木枯萎 C.造成洪澇災害 D.影響湖泊生態環境
(5) 根據上表,請你提出改善北京空氣質量的一項建議。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省蘇州五中高一第二學期期中考試化學試卷(帶解析) 題型:實驗題
(10分)下表是某城市某日的空氣質量報告:
| 污染指數 | 首要污染物 | 空氣質量級別 | 空氣質量狀況 |
| 55 | SO2 | II | 良 |
查看答案和解析>>
科目:高中化學 來源:2014屆江蘇省高一第二學期期中考試化學試卷(解析版) 題型:實驗題
(10分)下表是某城市某日的空氣質量報告:
|
污染指數 |
首要污染物 |
空氣質量級別 |
空氣質量狀況 |
|
55 |
SO2 |
II |
良 |
該市某校研究性學習小組對表中首要污染物SO2導致酸雨的成因進行了如下探究:
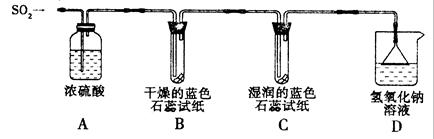
[探究實驗一]用下圖所示裝置進行實驗。
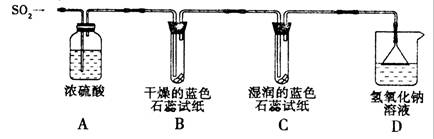
① A裝置的作用是 (填“干燥”或“氧化”)SO2氣體。
②實驗過程中,B裝置內石蕊試紙的顏色沒有發生變化,C裝置內濕潤的藍色石蕊試紙變 色,說明SO2與水反應生成一種酸。
③ D裝置的作用是 ,D中發生反應的化學方程式是 。
[探究實驗二]往盛有水的燒杯中通入SO2氣體,測得所得溶液的pH 7(填“>”“=”或“<”),然后每隔1 h測定其pH,發現pH逐漸 (填“變大”或“變小”),直至恒定。說明燒杯中的溶液被空氣中的氧氣氧化最終生成H2SO4。
[查閱資料]SO2形成酸雨的另一途徑為:SO2與空氣中的O2在飄塵的作用下反應生成SO3,SO3溶于降水生成H2SO4。則在此過程中的飄塵是作為 (填“催化劑”或“氧化劑”)。
[探究結論]SO2與空氣中的氧氣、水反應生成硫酸而形成酸雨。該市可能易出現酸雨。
[知識拓展]
(1)汽車排放的尾氣,硝酸、化肥等工業生產排出的廢氣中都含有氮的氧化物,氮的氧化物溶于水最終轉化為 ,是造成酸雨的另一主要原因。
(2)該市某工廠的燃料煤中硫的質量分數為0.16%,該工廠每天燃燒這種煤100噸。如果煤中的硫全部轉化為SO2,那么這些SO2在標準狀況下的體積約為 m3。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com