
【題目】已知X、Y、Z、W是元素周期表中短周期中的四種非金屬元素,它們的原子序數依次增大,X元素的原子形成的陽離子就是一個質子,Z、W在元素周期表中處于相鄰的位置,它們的單質在常溫下均為無色氣體,Y原子的最外層電子數是內層電子數的2倍。試回答:
(1)寫出下列元素的元素符號和電子排布式:
X____________________ Y___________________
Z____________________ W___________________
(2)X單質和Z單質在一定條件下反應生成化合物E,該反應的化學方程式為________________。E在催化劑存在的條件下可用于還原汽車尾氣中的______,以減少對大氣的污染。
【答案】H、1s1 C、1s22s22P2 N、1s22s22P3 O、1s22s22p4 ![]() 氮的氧化物
氮的氧化物
【解析】
X元素的原子形成的陽離子就是一個質子,故X為H元素;
Z、W在元素周期表中處于相鄰的位置,它們的單質在常溫下均為無色氣體,且為短周期非金屬元素,原子序數依次增大,Z為N,W為O;
Y原子的最外層電子數是內層電子數的2倍,所以Y為C元素,據此進行答題。
X元素的原子形成的陽離子就是一個質子,故X為H,Z、W在元素周期表中處于相鄰的位置,它們的單質在常溫下均為無色氣體,且為短周期非金屬元素,原子序數依次增大,Z為N,W為O,Y原子的最外層電子數是內層電子數的2倍,所以Y為C。
綜上所述:X為氫,Y為碳,Z為氮,W為氧,
(1)X為H,其核外只有一個電子,核外電子排布式為:1s1;Y為碳,碳元素為6號元素,原子核外有6個電子,其電子排布式為:1s22s22P2;Z為氮,氮元素為7號元素,原子核外有7個電子,其電子排布式為:1s22s22P3,W為氧,氧元素為8號元素,原子核外有8個電子,其電子排布式為:1s22s22P4;
故答案為:H、1s1;C、1s22s22P2;N、1s22s22P3;O、1s22s22p4
(2)氫氣和氮氣在一定條件下反應生成化合物氨氣,該反應的化學方程式為:![]() ;氨氣在催化劑存在的條件下可用于還原汽車尾氣中的氮的氧化物:一氧化氮、二氧化氮,以減少對大氣的污染
;氨氣在催化劑存在的條件下可用于還原汽車尾氣中的氮的氧化物:一氧化氮、二氧化氮,以減少對大氣的污染
故答案為:![]() ;氮的氧化物;
;氮的氧化物;


科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. ![]() C表示質子數為6、中子數為8的核素
C表示質子數為6、中子數為8的核素
B. 甲醇(CH3OH)和甘油(CH2OHCHOHCH2OH)互為同系物
C. C5H12的同分異構體有3種,其沸點各不相同
D. CH3CH2CH2CH(CH3)2的名稱是2甲基戊烷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通過資源化利用的方式將CO2轉化為具有工業應用價值的產品(如圖所示),是一種較為理想的減排方式,下列說法中正確的是( )
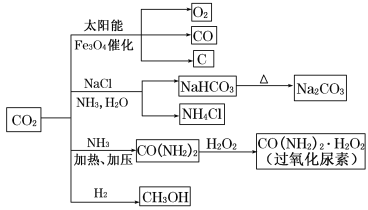
A.CO2經催化分解為C、CO、O2的反應為放熱反應
B.除去Na2CO3固體中少量NaHCO3可用熱分解的方法
C.過氧化尿素和SO2都能使品紅溶液褪色,其原理相同
D.由CO2和H2合成甲醇,原子利用率達100%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL-1的鹽酸,測得溶液中的CO32-、HCO3-、AlO2-、Al3+離子的物質的量與加入鹽酸溶液的體積變化關系如圖所示,則下列說法正確的是( )

A. 原混合溶液中的CO2-3與AlO-2的物質的量之比為1:2
B. V1:V2=1:5
C. M點時生成的CO2為0.05mol
D. a曲線表示的離子方程式為:AlO-2+H++H2O=Al(OH)3↓
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列各組離子在指定溶液中能大量共存的是
A. 澄清無色透明溶掖中:K+、Cu2+、ClO-、S2-
B. 含有大量Al3+的溶液:Na+、NH4+、SO42-、C1-
C. 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-
D. ![]() 的溶液中:Na+、HCO3-、SO42-、NH4+
的溶液中:Na+、HCO3-、SO42-、NH4+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硫酸鈉中有+4價的硫,它既有氧化性又有還原性,現有試劑:溴水、Na2S溶液、Na2SO3溶液、稀硫酸、NaOH溶液、氨水。
(1)要證明Na2SO3具有還原性,應選用的試劑有______,看到的現象是_______,反應的化學方程式為__________。
(2)要證明Na2SO3具有氧化性,應選用的試劑有_____,看到的現象是________,反應的化學方程式為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據如下能量關系示意圖,下列說法正確的是
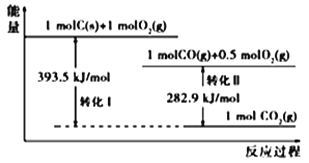
A. 1 molC(g)與1 mol O2(g)的能量之和為393.5 kJ
B. 反應2CO(g)+O2(g) ===2CO2(g)中,生成物的總能量大于反應物的總能量
C. 由C→CO的熱化學方程式為:2C(s)+O2(g) ===2CO(g) ΔH= 221.2 kJmol1
D. CO的燃燒熱ΔH=+282.9 kJmol1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)如圖是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式:_______________________________________________________。
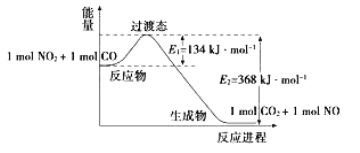
(2)總反應:Pb + PbO2 + 2H2SO4 = 2PbSO4 + 2H2O寫出下列的電極反應式
負極:_____________________________
正極:_____________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】原電池產生電流的本質原因是( )
A. 電解質溶液中有電離出的自由移動的離子
B. 有導線將兩個活潑性不同的電極連接
C. 在不同金屬的兩極間存在電勢差
D. 在原電池中發生了氧化還原反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com