
 $?_{暗處}^{光照}$
$?_{暗處}^{光照}$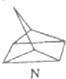 △H═88.6kJ•mol-1
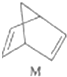
△H═88.6kJ•mol-1分析 (1)M轉化為N是吸熱反應,所以N的能量高,不穩定;
(2)甲醇燃燒生成CO2(g)和H2(g)屬于不完全燃燒,放出的熱量少,故a<238.6;
(3)有1mol Cl2參與反應時釋放出145kJ熱量,2mol氯氣反應放熱290kJ,注物質聚集狀態和對應反應焓變寫出熱化學方程式;
(4)所給反應中轉移12個電子,故每轉移1mol電子放出的熱量為1 176kJ÷12=98kJ;
(5)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H=+489.0kJ•mol-1
②CO(g)+1/2O2(g)=CO2(g)△H=-283.0kJ•mol-1111]
③C(石墨)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
則關鍵蓋斯定律可知(③×3-①-②×3)×2即得.
解答 解:(1)有機物M經過太陽光光照可轉化成N,:△H=+88.6kJ•mol-1,過程是吸熱反應,N暗處轉化為M,是放熱反應,能量越低越穩定,說明M穩定;
故答案為:M;
(2)燃燒熱是1mol物質完全燃燒生成穩定氧化物放出的熱量,甲醇燃燒生成CO2(g)和H2(g)屬于不完全燃燒,放出的熱量小于燃燒熱;
故答案為:<;
(3)有1mol Cl2參與反應時釋放出145kJ熱量,2mol氯氣反應放熱290kJ,反應的熱化學方程式為:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290kJ•mol-1 ;
故答案為:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290kJ•mol-1 ;
(4)4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1176kJ•mol-1,轉移12mol電子放熱1176KJ,則反應過程中,每轉移1mol電子放熱98kJ,
故答案為:98kJ;
(5)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H=+489.0kJ•mol-1
②CO(g)+1/2O2(g)=CO2(g)△H=-283.0kJ•mol-1111]
③C(石墨)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
則關鍵蓋斯定律可知(③×3-①-②×3)×2即得到4Fe(s)+3O2(g)=2Fe2O3(s)的△H=-1641.0kJ•mol-1,故答案為:-1641.0kJ•mol-1.
點評 本題考查了化學反應能量變化,燃燒熱概念分析判斷,氧化還原反應電子轉移的計算應用,掌握基礎是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,c(H+)/c(OH一)=1×10-12的溶液:K+、AlO2-、SiO32-、Na+ | |
| B. | 加入KSCN顯紅色的溶液:K+、NH4+、Cl-、I- | |
| C. | 加入石蕊顯藍色的溶液:Cu2+、Al3+、NO3-、SO42- | |
| D. | 加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 品名 | 濃縮菠蘿汁 |
| 配料 | 水、濃縮菠蘿汁、蔗糖、檸檬酸、甜蜜素、維生素C、菠蘿香精、檸檬黃、日落黃、山梨酸鉀等. |
| 性質 | 亞硝酸鈉 | 氯化鈉 |
| 1.酸性條件下的穩定性 | 微熱時分解為NO和NO2 | 微熱時不分解 |
| 2.熔點 | 271℃ | 801℃ |
| 3.室溫時的溶解度 | 約80g | 約35g |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 反應結束時溶液的pH=7 | |
| B. | 反應后溶液中存在的粒子只有Na+和Cl- | |
| C. | 該反應的實質是H+和OH-結合生成水 | |
| D. | 反應前后所有元素的化合價均無變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

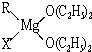 中的配位鍵
中的配位鍵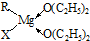
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com