
| A. | c(H+)•c(OH-)=KW | B. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)+c(OH-) | D. | c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
分析 等物質的量濃度、等體積的NaOH和醋酸溶液混合,二者恰好完全反應生成醋酸鈉,醋酸鈉是強堿弱酸鹽,醋酸根離子水解導致溶液呈堿性,溶液中存在電荷守恒和物料守恒,根據電荷守恒和物料守恒判斷.
解答 解:等物質的量濃度、等體積的NaOH和醋酸溶液混合,二者恰好完全反應生成醋酸鈉,醋酸鈉是強堿弱酸鹽,醋酸根離子水解導致溶液呈堿性,
A.離子積常數與溶液酸堿性及溶液中溶質成分無關,任何電解質水溶液中都存在c(H+)•c(OH-)=KW,所以該溶液中存在c(H+)•c(OH-)=KW,故A不選;
B.醋酸根離子水解導致溶液呈堿性,則溶液中存在c(OH-)>c(H+),醋酸根離子水解程度較小,且鈉離子不水解,則存在c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故B不選;
C.電解質溶液中存在電荷守恒,根據電荷守恒得c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以c(Na+)<c(CH3COO-)+c(OH-),故C選;
D.電解質溶液中存在電荷守恒,根據電荷守恒得c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故D不選;
故選C.
點評 本題考查酸堿混合溶液定性判斷,為高頻考點,明確混合溶液中溶質及其性質是解本題關鍵,側重考查學生分析判斷及電荷守恒和物料守恒的靈活運用能力,題目難度不大.


科目:高中化學 來源: 題型:解答題
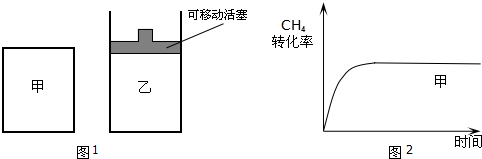
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
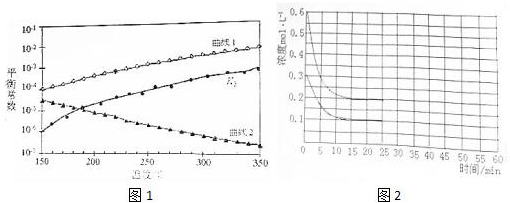
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
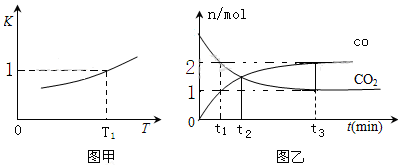
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CaOCl2 | B. | (NH4)2Fe(SO4)2 | C. | Na3A1F6 | D. | Cu2(OH)2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 反應中,每生成1molH2轉移的電子數均為2mol | |
| B. | 參加反應的金屬Na、Mg、Al的物質的量之比為1:2:3 | |
| C. | 鎂的物質的量為0.1mol | |
| D. | V=2.24 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com