
【題目】[化學—選修5:有機化學基礎]
高分子材料PET聚酯樹脂和PMMA的合成路線如下:

已知:Ⅰ.RCOOR′+ R′′18OH![]() RCO18O R′′+ R′OH(R、R′、R′′代表烴基);
RCO18O R′′+ R′OH(R、R′、R′′代表烴基);
Ⅱ. (R、R′代表烴基);
(R、R′代表烴基);
(1)①的反應類型是________。
(2)②的化學方程式為________。
(3)PMMA單體的官能團名稱是________、________。
(4)F的核磁共振氫譜顯示只有一組峰,⑤的化學方程式為________。
(5)G的結構簡式為________。
(6)下列說法正確的是________(填字母序號)。
a.⑦為酯化反應
b.B和D互為同系物
c.D的沸點比同碳原子數的烷烴高
d.1 mol 與足量NaOH溶液反應時,最多消耗4 mol NaOH
與足量NaOH溶液反應時,最多消耗4 mol NaOH
(7)J的某種同分異構體與J具有相同官能團,且為順式結構,其結構簡式是________。
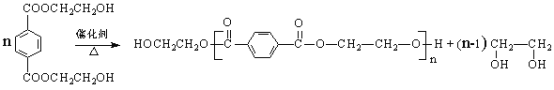
(8)寫出由PET單體制備PET聚酯(化學式為C10nH8nO4n 或C10n+2H8n+6O4n+2)并生成B的化學方程式________________________________________________。
【答案】加成反應 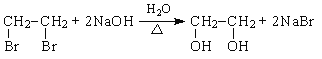 碳碳雙鍵 酯基
碳碳雙鍵 酯基 ![]()
 a、c
a、c 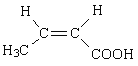
【解析】
(1)根據合成路線可知,①為乙烯與溴的加成反應生成A為1,2-二溴乙烷;
(2)②為1,2-二溴乙烷在氫氧化鈉水溶液中的水解反應生成乙二醇。化學方程式為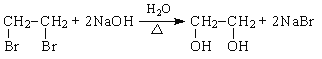 ;
;
(3)由PMMA的結構可知,PMMA為烯酯類加聚反應產物,故其單體的官能團名稱是碳碳雙鍵和酯基;
(4)F為醇催化氧化生成,其核磁共振氫譜顯示只有一組峰結構對稱,則E為2-丙醇,F為丙酮,故⑤的化學方程式為![]() ;
;
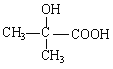
(5)G由丙酮在i:HCN/OH-,ii: H2O/H+作用下生成,由題目信息可知其結構簡式為 ;
;
(6)a.⑦為 與甲醇發生酯化反應生成PMMA單體,故a正確;
與甲醇發生酯化反應生成PMMA單體,故a正確;
b.B為乙二醇,D為甲醇,二者不是同系物,故b錯誤;
c.D為甲醇,分子間可產生氫鍵,所以其沸點比同碳原子數的烷烴高,故c正確;
d.1 mol![]() 中含2mol酯基,所以與足量NaOH溶液反應時,最多消耗2 mol NaOH,故d錯誤;答案選a、c;
中含2mol酯基,所以與足量NaOH溶液反應時,最多消耗2 mol NaOH,故d錯誤;答案選a、c;
(7)J為2-甲基丙烯酸,其同分異構體中具有碳碳雙鍵與羧基,且為順式結構,其結構簡式是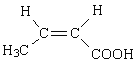 ;
;
(8)根據題干信息可知,由PET單體制備PET聚酯的化學方程式為: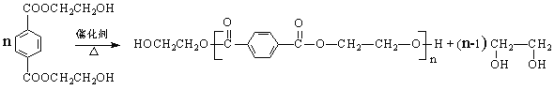 。
。


科目:高中化學 來源: 題型:
【題目】(1)2008年北京奧運會主體育場的外形好似“鳥巢”(The Bird Nest),有一類化學物質也好似鳥巢,如化學式是B5H9的五硼烷(如圖)。 請問1mol五硼烷的質量是________g。
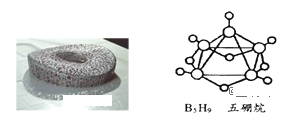
(2)14C相對原子質量為14,含有6個質子,8個中子和6個電子,NA為阿伏加德羅常數,1mol14CH4分子中所含中子數為_________,7g14C原子形成的石墨中所含質子數為___________,17g 14CH3+所含電子數為____________
(3)現有兩組混合物:①溴水 ②39%的乙醇溶液(乙醇的沸點為78.4℃),分離以上各混合物的正確實驗方法依次是_____________ 、____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】世界環保聯盟建議全面禁止使用氯氣用于飲用水的消毒,而建議采用高效“綠色”消毒劑二氧化氯。二氧化氯是一種極易爆炸的強氧化性氣體,易溶于水、不穩定、呈黃綠色,在生產和使用時必須盡量用稀有氣體進行稀釋,同時需要避免光照、震動或加熱。實驗室以電解法制備ClO2的流程如下:

(1) ClO2中所有原子_____________(填“是”或“不是”)都滿足8電子結構。上圖所示電解法制得的產物中雜質氣體B能使石蕊試液顯藍色,除去雜質氣體可選用_________
A.飽和食鹽水 B.堿石灰 C.濃硫酸 D.蒸餾水
(2) 穩定性二氧化氯是為推廣二氧化氯而開發的新型產品,下列說法正確的是_________
A.二氧化氯可廣泛用于工業和飲用水處理
B.穩定性二氧化氯的出現大大增加了二氧化氯的使用范圍
C.在工作區和成品儲藏室內,要有通風裝置和監測及警報裝置
(3) 歐洲國家主要采用氯酸鈉氧化濃鹽酸制備。化學反應方程式為______________________。
(4) 我國廣泛采用經干燥空氣稀釋的氯氣與固體亞氯酸鈉(NaClO2)反應制備,化學方程式是 __________________,此法相比歐洲方法的優點是______________________。
(5) 科學家又研究出了一種新的制備方法,利用硫酸酸化的草酸(H2C2O4)溶液還原氯酸鈉,化學反應方程式為_____________________________。此法提高了生產及儲存、運輸的安全性,原因是 _________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如果把![]() 的相對原子質量定義為24,以
的相對原子質量定義為24,以![]() 所含的C原子數為阿伏加德羅常數,則在標準狀況時下列數值肯定不變的是( )
所含的C原子數為阿伏加德羅常數,則在標準狀況時下列數值肯定不變的是( )
A.濃硫酸(![]() )的物質的量濃度
)的物質的量濃度
B.常溫下氯化鈉的溶解度
C.標準狀況下氣體摩爾體積.
D.1克拉鉆石所含的C原子的物質的量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】大地震過后,飲用水的消毒殺菌成為抑制大規模傳染性疾病爆發的有效方法之一,漂粉精是常用的消毒劑。
(1)工業上制取漂粉精的化學方程式為______________________,在使用漂粉精時,為了加速漂白作用,可以在漂粉精中加入少量________________.
(2)漂粉精暴露在空氣中易失效的主要原因是___________、_______________(用化學方程式表示)
(3)濃鹽酸和次氯酸鈣能發生如下反應Ca(ClO)2+4HCl(濃)=CaCl2+2Cl2↑+2H2O,用貯存很久的漂粉精和濃鹽酸反應制得的氯氣中,可能含有的雜質氣體是__________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Cl2在70℃的NaOH水溶液中,能發生氧化還原反應后可生成NaClO與NaClO3現有63.9g Cl2,將其通入到足量70℃的NaOH水溶液中,反應完全后測得溶液中NaClO與NaClO3的物質的量比為4:1,并得到500mL溶液。
(1)寫出Cl2在70℃的NaOH水溶液中發生上述反應的化學方程式______。
(2)計算完全反應后溶液中NaClO、NaClO3物質的量濃度____、______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用難溶于水的碳酸鍶(SrCO3)粉末為原料(含少量鋇和鐵的化合物)制備高純六水氯化鍶晶體(SrCl26H2O),其過程為:
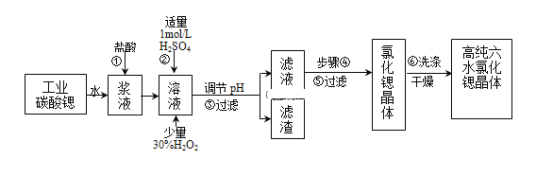
已知:Ⅰ.有關氫氧化物沉淀的pH:
氫氧化物 | Fe(OH)3 | Fe(OH)2 |
開始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
Ⅱ.SrCl26H2O晶體在61℃時開始失去結晶水,100℃時失去全部結晶水.
(1)操作①需要加快反應速率,措施有充分攪拌和______(寫一種).碳酸鍶與鹽酸反應的離子方程式______.
(2)在步驟②-③的過程中,將溶液的pH值由1調節至______;宜用的試劑為______.
A.1.5B.3.7C.9.7D.氨水E.氫氧化鍶粉末F.碳酸鈉晶體
(3)操作③中所得濾渣的主要成分是______(填化學式).
(4)工業上用熱風吹干六水氯化鍶,適宜的溫度是______
A.50~60℃B.80~100℃C.100℃以上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用苯甲醛(C6H5CHO)在NaOH溶液中可以制苯甲醇(C6H5CH2OH)和苯甲酸(C6H5COOH)。實驗流程如圖:
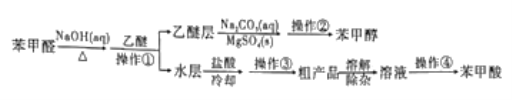
相關物質的性質如下表所示。回答下列問題:
物質 | 對水的相對密度 | 沸點 | 溶解性 |
苯甲醇 | 1.04 | 205.7 | 微溶于水,易溶于乙醚 |
苯甲酸 | 1.27 | 249 | 微溶于冷水,可溶于熱水,易溶于乙醚 |
乙醚 | 0.71 | 34.6 | 與水互不相溶 |
(1)操作①中,需要用到的玻璃儀器除燒杯外,還有____。操作①后,苯甲醇在容器中混合物的_____(填“上”或“下”)層。
(2)乙醚層用10%Na2CO3溶液洗滌的目的是_____。操作②前常需要加入MgSO4,作用是______。操作②的裝置如圖,指出該裝置圖中兩個錯誤:______。
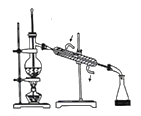
(3)操作③是______,操作④是______。
(4)取106.00g苯甲醛反應,若苯甲醛的轉化率為80%,乙醚的萃取率為100%,洗滌等過程損失率為10%,則最終可制得苯甲醇___g(結果保留小數點后兩位)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素A、B、C、D在元素周期表中的相對位置如表所示,已知A原子最外層電子數與次外層電子數之比為2:1。E和C、D同周期,它的原子序數比B多6。
回答下列問題:
A | B | ||
C | D |
(1)人的汗液中含有D的簡單離子,其離子結構示意圖為______,元素C在元素周期表中的位置是______。C的最高價氧化物的水化物的濃溶液稀釋的方法是______。
(2)A的最高價氧化物的化學式為_____,所含的化學鍵類型是______(填“離子鍵”或“共價鍵”)。
(3)E的最高價氧化物對應的水化物的化學式為____,它是______(填“酸性”或“兩性”或“堿性”)化合物。寫出該化合物與氫氧化鈉溶液反應的離子方程式______。
(4)加熱時,B的最高價氧化物對應水合物的濃溶液與單質A反應的化學方程式為(用具體的化學式表示)______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com