
【題目】用含有Al2O3、SiO2和少量FeO·xFe2O3的鋁灰制備Al2(SO4)3·18H2O,工藝流程如下(部分操作和條件略):
Ⅰ.向鋁灰中加入過量稀H2SO4,過濾;
Ⅱ.向濾液中加入過量KMnO4溶液,調節溶液的pH約為3;
Ⅲ.加熱,產生大量棕色沉淀,靜置,上層溶液呈紫紅色;
Ⅳ.加入MnSO4至紫紅色消失,過濾;
Ⅴ..再經過一系列操作,分離得到產品。
(1)步驟Ⅰ中過濾所得濾渣主要成分為:______________________,
H2SO4溶解Al2O3的離子方程式為:_____________________。
(2)步驟Ⅱ中加入KMnO4時發生反應的離子方程式為: 。
(3)已知:生成氫氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
開始沉淀時 | 3.4 | 6.3 | 1.5 |
完全沉淀時 | 4.7 | 8.3 | 2.8 |
注:金屬離子的起始濃度均為0.1 mol·L-1
①根據表中數據解釋步驟Ⅱ的目的:________________________,
②當Al3+開始沉淀時,Fe3+的濃度約為:_______________________。
(4)已知:一定條件下,MnO![]() 可與Mn2+反應生成MnO2。
可與Mn2+反應生成MnO2。
①向Ⅲ的沉淀中加入濃鹽酸并加熱,能說明沉淀中存在MnO2的現象是: 。
②步驟Ⅳ中加入MnSO4的目的是: 。
(5)步驟Ⅴ中“一系列操作”是__________________、_________________。
【答案】
(1)SiO2;Al2O3+6H+ =2Al3++3H2O
(2)MnO![]() +5 Fe2++8H+=Mn2++5 Fe3++4H2O
+5 Fe2++8H+=Mn2++5 Fe3++4H2O
(3)①pH約為3時,Fe2+和Al3+不能形成沉淀,將Fe2+氧化為Fe3+,可使鐵完全沉淀;②10-6.7或10-6.8
(4)①生成黃綠色氣體;②除去過量的MnO![]()
(5)蒸發濃縮、冷卻結晶;
【解析】
試題分析:(1)Al2O3、FeOxFe2O3能與硫酸反應,而SiO2不與硫酸反應,步驟Ⅰ過濾得到沉淀的主要成分為:SiO2,硫酸溶解氧化鋁生成硫酸鋁和水,反應的離子方程式為:Al2O3+6H+=2Al3++3H2O;故答案為:SiO2;Al2O3+6H+=2Al3++3H2O;
(2)高錳酸根離子在酸溶液中被還原為錳離子,亞鐵離子被氧化為鐵離子,反應的離子方程式為:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O,故答案為:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O;
(3)①鐵離子開始沉淀和沉淀完全的溶液pH為1.5~2.8,鋁離子開始沉淀pH為3.4,亞鐵離子開始沉淀的溶液pH大于鋁離子完全沉淀pH,向濾液中加入過量KMnO4溶液,目的是氧化亞鐵離子為三價鐵離子,依據圖表數據分析可知,所以調節溶液的pH約為3,可以使鐵離子全部沉淀,鋁離子不沉淀分離,步驟II的目的:pH約為3時,Fe2+和Al3+不能形成沉淀,將Fe2+氧化為Fe3+,可使鐵完全沉淀,故答案為:pH約為3時,Fe2+和Al3+不能形成沉淀,將Fe2+氧化為Fe3+,可使鐵完全沉淀;
②濃度為0.1molL-1的Fe3+開始沉淀時,溶液pH為1.5,所以Ksp[Fe(OH)3] = 0.1 × (10-14+1.5)3 = 1 × 10-38.5,當Al3+開始沉淀時,溶液pH為3.4,即溶液中氫氧根離子的濃度為1×10-14+3.4 molL-1=1×10-10.6 molL-1,所以Fe3+的濃度為![]() =10-6.7 molL-1,故答案為:10-6.7 molL-1;
=10-6.7 molL-1,故答案為:10-6.7 molL-1;
(4)①向Ⅲ的沉淀中加入濃HCl并加熱,二氧化錳和濃鹽酸在加熱條件下反應生成氯化錳、氯氣和水生成的氯氣是黃綠色氣體,能說明沉淀中存在MnO2,故答案為:生成黃綠色氣體;②MnO4-可與Mn2+反應生成MnO2,過濾除去,所以可以利用MnSO4的溶液和高錳酸鉀溶液反應生成二氧化錳,把過量高錳酸根離子除去,故答案為:除去過量的MnO4-;
(5)從溶液中獲得Al2(SO4)318H2O晶體,可以通過蒸發濃縮、冷卻結晶的方法,故答案為:蒸發濃縮、冷卻結晶。


 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:
【題目】工業上采用氨的催化氧化制備硝酸,起反應如下:
![]()
![]()
設空氣中氧氣的體積分數為0.20,氮氣的體積分數為0.80
(1)為使NH3恰好完全氧化為NO,氨-空氣混合物中氨的體積分數為 (用小數表示,保留2位小數)
(2)1mol NH3完全轉化HNO3,若在此過程中不補充水,則所得HNO3溶液的質量分數為 (用小數表示,保留2位小數)
(3)已知NH3完全轉化NO的轉化率為95%,由NO轉化HNO3的轉化率為92%.請計算用17噸NH3可制取質量分數為0.63的硝酸溶液為 噸
(4)硝酸工業生產中的尾氣可用純堿溶液吸收,有關的化學反應為:
![]() ①
①
![]() ②
②
若每生產1mol CO2,吸收溶液質量就增加40g。計算吸收液中NaNO2和NaNO3物質的量之比為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用燃燒法測定某種α- 氨基酸X (CxHyOzNp)的分子組成。取3.34 g X放在純氧中充分燃燒,生成CO2、H2O和N2。現用下圖所示裝置進行實驗(鐵架臺、鐵夾、酒精燈等未畫出),請回答有關問題:
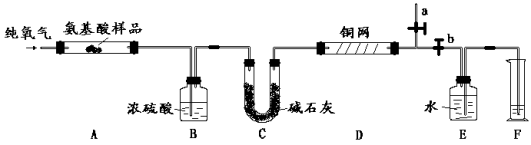
(1)實驗開始時,首先打開止水夾a,關閉止水夾b,通一段時間的純氧氣,這樣做的目的是 ;之后則需關閉止水夾a,打開止水夾b。
(2)上述裝置中A、D處都需要用酒精燈加熱,操作時應先點燃 處的酒精燈。
(3)裝置D的作用是 。
(4)實驗結果:
①B中濃硫酸增重1.62 g,C中堿石灰增重7.04 g,F中收集到224 mL氣體(標準狀況)。
②X的相對分子質量為167,它是通過 測定的(填一種現代化學儀器)
試通過計算確定該有機物X的分子式(寫出計算過程)。
(5)另取3.34 g X與0.2 mol/L 的NaOH溶液反應,最多能中和NaOH溶液200 mL,有機物X的13C-NMR(即核磁共振碳譜,其作用與核磁共振氫譜類似)如下圖所示。試確定有機物X的結構簡式為 。
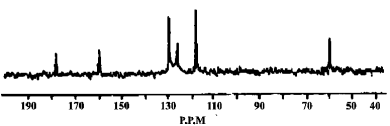
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫化亞銅(CuH)是一種不穩定的物質,能在氯氣中燃燒,也能與酸反應。用CuSO4溶液和“某物質”在40~50℃時反應可生成CuH。下列敘述中錯誤的是( )
A.“某物質”具有還原性
B.CuH與鹽酸反應可能產生H2
C.CuH與足量稀硝酸反應:CuH+3H++NO3-=Cu2++NO↑+2H2O
D.CuH在氯氣中燃燒:CuH+Cl2=CuCl+HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學采用工業大理石(含有少量SiO2、Al2O3、Fe2O3等雜質)制取CaCl2·6H2O,設計了如下流程:
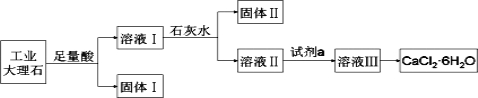
下列說法不正確的是( )
A.固體Ⅰ中含有SiO2,固體Ⅱ中含有Fe(OH)3
B.使用石灰水時,要控制pH,防止固體Ⅱ中Al(OH)3轉化為AlO2-
C.從溶液Ⅲ得到CaCl2·6H2O產品的過程中,須控制好條件防止產物分解
D.若改變實驗方案,在溶液Ⅰ中直接加氨水至沉淀完全,濾去沉淀,其溶液經蒸發濃縮、冷卻結晶也可得到純凈CaCl2·6H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E均是短周期元素,其原子序數依次增大,A和B同周期,A和D同主族,A原子最外層電子數是內層電子數的二倍,B元素族序數是周期數的三倍,B的陰離子與C的陽離子電子層結構相同,C的單質與B的單質在不同條件下反應,可生成C2B或C2B2,E是所在周期中原子半徑最小的元素。請回答:
(1)D在元素周期表中的位置是 。
(2)C2B的電子式是 ;AB2的結構式是 。
(3)B、C、E的離子半徑由大到小的順序為 (用化學式回答,下同);A、D、E元素最高價氧化物對應水化物的酸性由強到弱為 。
(4)B的氣態氫化物與H2S相比沸點高的是 (用化學式回答);原因是 。
(5)水中錳含量超標,容易使潔具和衣物染色,使水產生異味,EB2可以用來除去水中超標的Mn2+,生成黑色沉淀MnO2,當消耗13.50gEB2時,共轉移了1mol電子,則反應的離子方程式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤燃燒排放的煙氣中(主要含SO2、CO2)的SO2形成酸雨、污染大氣,對煙氣進行脫硫,回答下列問題:
(1)采用Ca(ClO)2煙氣脫硫可得到較好的效果。已知下列反應:
①SO2(g)+2OH (aq) =SO32 (aq)+H2O(l) ΔH1
②ClO (aq)+SO32 (aq) =SO42 (aq)+Cl (aq) ΔH2
③CaSO4(s) =Ca2+(aq)+SO42(aq) ΔH3
則反應SO2(g)+ Ca2+(aq)+ ClO (aq) +2OH (aq) = CaSO4(s) +H2O(l) +Cl (aq)的ΔH=_ 。
(2)采用氨水煙氣脫硫,最終可得到氮肥。將相同物質的量的SO2與NH3溶于水所得溶液中c(H+)﹣c(OH-)= (填字母編號).
A.c(SO32-)﹣c(H2SO3)
B.c(SO32-)+c(NH3·H2O)﹣c(H2SO3)
C.c(HSO3-)+c(SO32-)﹣c(NH4+)
D.c(HSO3-)+2c(SO32-)﹣c(NH4+)
(3)煙氣在較高溫度經下圖方法脫除SO2,并制得H2SO4。
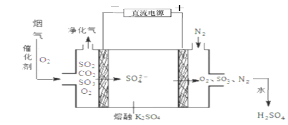
①在陰極放電的物質是 。
②在陽極生成SO3的電極反應式是 。
③已知室溫下,Ksp(BaSO4)=1.1×10-10。將脫除SO2后制得的H2SO4配成pH=4 的H2SO4溶液,與pH=9的 Ba(OH)2 溶液混合,若所得混合溶液的 pH=7,則 Ba(OH)2 溶液與 H2SO4 溶液的體積比為 。欲使溶液中c(SO42-) =2.0×10-4mol·L-1,則應保持溶液中 c(Ba2+) = mol·L-1。
(4)一定條件下,用Fe2O3、NiO或Cr2O3作催化劑,利用如下反應回收燃煤煙氣中的硫。反應為:2CO(g)+SO2(g)![]() 2CO2(g)+S(l) ΔH= - 270KJ·mol-1其他條件相同、催化劑不同時,SO2的轉化率隨反應溫度的變化如圖1,不考慮催化劑的價格因素,選擇_ 為該反應的催化劑較為合理(選填序號)。
2CO2(g)+S(l) ΔH= - 270KJ·mol-1其他條件相同、催化劑不同時,SO2的轉化率隨反應溫度的變化如圖1,不考慮催化劑的價格因素,選擇_ 為該反應的催化劑較為合理(選填序號)。

a. Cr2O3 b. NiO c. Fe2O3
選擇該催化劑的理由是:_ 。
某科研小組用選擇的催化劑,在380℃時,研究了n(CO) : n(SO2)分別為1:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述不相符合的是
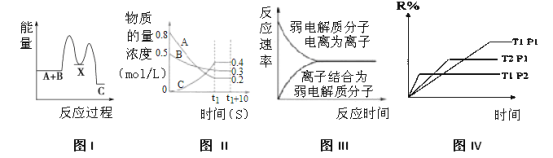
A.反應A+B→C(ΔH<0)分兩步進行:①A+B→X(ΔH>0),②X→C(ΔH<0),圖I表示總反應過程中能量變化
B.圖 II表示反應的化學方程式為3A+B=2C
C.圖III表示弱電解質在水中建立電離平衡的過程
D.圖IV表示反應M(g)+N(g) R(g)+2L(?)是放熱反應且L是氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學學習了化學反應速率后,聯想到曾用H2O2制備氧氣,于是設計了下面的實驗方案并進行實驗探究。
實驗編號 | 反 應 物 | 催 化 劑 |
甲 | 試管中加入3 mL 2﹪ H2O2溶液和3滴蒸餾水 | 無 |
乙 | 試管中加入3 mL 5﹪ H2O2溶液和3滴蒸餾水 | 無 |
丙 | 試管中加入3 mL 5﹪ H2O2溶液和3滴蒸餾水 | 1 mL 0.1 mol/L FeCl3溶液 |
丁 | 試管中加入3 mL 5﹪ H2O2溶液和3滴稀鹽酸溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
戊 | 試管中加入3 mL 5﹪ H2O2溶液和3滴NaOH溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
【查閱資料】過氧化氫(H2O2),其水溶液俗稱雙氧水,常溫下是一種無色液體,性質比較穩定。在加熱的條件下,它能分解生成氧氣。研究表明,將新制的5﹪的H2O2溶液加熱到65℃時就有氧氣放出,加熱到80℃時就有較多氧氣產生。
(1)上述實驗發生反應的化學方程式為 。
(2)實驗甲和實驗乙的實驗目的是 ;
實驗丙、實驗丁和實驗戊的實驗目的是 。
(3)請根據該同學查閱的資料分析H2O2的性質,解釋實驗甲和實驗乙能否達到實驗目的? 。
(4)實驗過程中該同學對實驗丙、丁、戊中產生的氣體進行收集,并在2分鐘內6個時間點對注射器內氣體進行讀數,記錄數據如下表。
時間/s | 20 | 40 | 60 | 80 | 100 | 120 | |
氣體體積/mL | 實驗丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
實驗丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
實驗戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
①對實驗戊,0~20 s的反應速率v1= mL/s,100~120 s的反應速率v2= mL/s。
不考慮實驗測量誤差,二者速率存在差異的主要原因是 。
②如右圖是根據實驗收集到最大體積的氣體時所用時間繪制的圖像。曲線c表示的是實驗 (填“丙”、“丁”或“戊”)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com