
【題目】下列變化不屬化學科學研究的范疇的是( )
A.電解水生成氫氣和氧氣
B.合成有機高分子材料
C.原子彈發生劇烈爆炸
D.生產合成纖維和合成橡膠
 期末1卷素質教育評估卷系列答案
期末1卷素質教育評估卷系列答案科目:高中化學 來源: 題型:
【題目】下列圖像分別表示有關反應的反應過程與能量變化的關系。
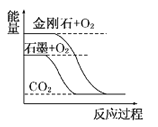

據此判斷下列說法中正確的是( )
A. 石墨轉變為金剛石是吸熱反應 B. 白磷比紅磷穩定
C. S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)=SO2(g) ΔH2 則ΔH1>ΔH2 D. CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A是分子式為C7H8的芳香烴,已知它存在以下一系列轉化關系,其中C是一種一元醇,D是A的對位一取代物,H與E、I與F分別互為同分異構體:
(1)化合物I的結構簡式是 ,
(2)反應B﹣→C的化學方程式是: , 反應E﹣→F的化學方程式是: .
(3)設計實驗證明H中含有溴原子,還需用到的試劑有 .
(4)為驗證E﹣→F的反應類型與E﹣→G不同,下列實驗方法切實可行的是 .
A.向E→F反應后的混合液中加入硝酸酸化,再加入AgNO3溶液得到淡黃色沉淀
B.向E→F反應后的混合液中加入溴水,發現溴水立即褪色
C.向E→F反應后的混合液中加入鹽酸酸化后,加入溴的CCl4溶液,使之褪色
D.向E→F反應后的混合液中加入酸性KMnO4溶液,混合液紅色變淺.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2O2是一種綠色試劑,在化學工業中用于生產過氧乙酸、亞氯酸鈉等的原料,醫藥工業用作殺菌劑、消毒劑。某化學小組為探究H2O2的性質做了如下實驗:
(1) 下表是該小組研究影響過氧化氫(H2O2)分解速率的因素時采集的一組數據。

研究小組在設計方案時,考慮了濃度、____、____因素對過氧化氫分解速率的影響。
(2) 另一研究小組擬在同濃度 Fe3+的催化下,探究H2O2濃度對H2O2分解反應速率的影響。限選試劑與儀器:30% H2O2、0.1 mol·L-1FeCl3、蒸餾水、錐形瓶、雙孔塞、水槽、膠管、玻璃導管、量筒、秒表、恒溫水浴槽、注射器。設計實驗裝置,完成圖1方框內的裝置示意圖(要求所測得的數據能直接體現反應速率大小)。________


圖1 圖2
(3) 對于H2O2分解反應,Cu2+也有一定的催化作用。為比較Fe3+和 Cu2+對H2O2分解的催化效果,研究小組的同學設計了如圖2所示的實驗。請回答相關問題:
①可通過觀察________,比較得出結論。
②有同學提出將0.1 mol·L-1FeCl3溶液改為0.05 mol·L-1Fe2(SO4)3更為合理,其理由是___。
(4) 已知 FeCl3溶液中主要含有H2O、Fe3+和 Cl-三種微粒,甲同學又做了兩種猜想。
猜想 1:真正催化分解H2O2的是FeCl3溶液中的 Fe3+。
猜想 2:真正催化分解H2O2的是____。
完成表格驗證猜想:
所需試劑 | 操作及現象 | 結論 |
_______ | _________ | Cl-對H2O2分解無催化作用 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數的值,則下列說法正確的是( )
A.1mol苯酚中“C═C”的個數為3 NA
B.常溫常壓下,22.4L丙烷所含有的共價鍵數目為10NA
C.標準狀況下,1L戊烷充分燃燒后生成的氣態產物的分子數為 ![]() NA
NA
D.2.8g乙烯和丙烯的混合氣體中所含碳原子數為0.2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將海水淡化與濃海水資源化結合起來是綜合利用海水的重要途徑之一。一般是先將海水淡化獲得淡水,再從剩余的濃海水中通過一系列工藝流程提取其他產品。
回答下列問題:
(1)采用“空氣吹出法”從濃海水中吹出Br2,并用純堿吸收。堿吸收溴的主要反應是Br2+Na2CO3+H2ONaBr+NaBrO3+NaHCO3,吸收1 mol Br2時,轉移的電子數為____mol。
(2)海水提鎂的一段工藝流程如下圖:

濃海水的主要成分如下:
離子 | Na+ | Mg2+ | Cl- | S |
濃度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
該工藝過程中,脫硫階段主要反應的離子方程式為______________,產品2的化學式為______,1 L濃海水最多可得到產品2的質量為___g。
(3)電解熔融的氯化鎂時發生反應的化學方程式為_____________;電解時,若有少量水存在會造成產品鎂的消耗,寫出有關反應的化學方程式__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨是重要的無機化工產品之一,在國民經濟中占有重要地位。我國采用鐵觸媒(以鐵為主的混合物)做催化劑合成氨。回答下列問題:
(1)Fe基態原子核外電子排布式為____。氮化鐵是一種重要的無機化合物,不溶于水,暴露在潮濕環境中可釋放出氨氣,元素Fe和N中,第一電離能較大的是_____,基態原子核外未成對電子數較多的是_______。
(2)N的氧化物有N2O等,N2O與CO2互為等電子體,N2O的空間構型為__________。
(3)N有多種氫化物,其中肼(N2H4)常用作火箭推進劑的燃料,N2H4中N原子的雜化形式為____。
(4)N、P、As為同族元素,NH3、PH3、AsH3三種物質的沸點由高到低的順序為_____。原因是____。
(5)K3[Fe(CN)6]常用于檢驗Fe2+,K3[Fe(CN)6]中存在的化學鍵類型有_______。
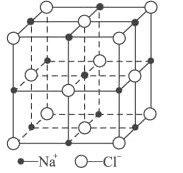
(6)FeO晶體的晶胞與NaCl的相似,NaCl的晶胞如圖所示。由于晶體缺陷,某氧化亞鐵晶體的實際組成為Fe0.9O,其中包含有Fe2+和Fe3+,晶胞邊長為428pm,則該晶體的密度為____g/cm3(列出計算式即可,用NA表示阿伏加德羅常數的值)。
 。
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com