
| A. | 實驗室用濃鹽酸與MnO2反應制Cl2,每生成22.4 LCl2,轉移的電子總數為2NA | |
| B. | 1 mol O2在反應中作氧化劑時,所得電子數一定為4NA | |
| C. | 1 mol Na2O2與足量H2O反應,轉移電子數為2NA | |
| D. | 0.1 mol金屬鈉在過量氧氣中充分燃燒,生成的化合物中離子總數為0.15NA |
分析 A、氯氣所處的狀態不明確;
B、氧氣反應后的價態不明確;
C、過氧化鈉和水反應時,1mol過氧化鈉轉移1mol電子;
D、鈉在氧氣中燃燒生成過氧化鈉,而在過氧化鈉中含2個鈉離子和1個過氧根.
解答 解:A、氯氣所處的狀態不明確,故氯氣的物質的量無法計算,則轉移的電子數無法計算,故A錯誤;
B、氧氣反應后的價態不明確,故氧氣得到的電子數無法計算,故B錯誤;
C、過氧化鈉和水反應時,1mol過氧化鈉轉移1mol電子,即轉移NA個電子,故C錯誤;
D、鈉在氧氣中燃燒生成過氧化鈉,0.1mol鈉反應生成0.05mol過氧化鈉,而在過氧化鈉中含2個鈉離子和1個過氧根,故0.05mol過氧化鈉中含0.15NA個離子,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,掌握物質的量的計算公式和物質結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,22.4 L CCl4、CO2含有的分子數為NA | |
| B. | 通常狀況下,NA個CO2分子占有的體積約為22.4 L | |
| C. | 常溫常壓下,1.06 g Na2CO3含有的Na+離子數為0.02NA | |
| D. | 物質的量濃度為0.5 mol/L的MgCl2溶液中,含有Cl-個數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸與氫氧化鈉溶液反應:H++OH-═H2O | |
| B. | 碳酸鈣與稀硝酸的反應:CO32-+2H+═CO2+H2O | |
| C. | 銅與稀硫酸反應:Cu+2H+═Cu2++H2↑ | |
| D. | 氯氣與氫氧化鈉溶液反應:Cl2+OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列問題:
用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 白醋中滴入石蕊試液呈紅色 | B. | 白醋加入熱水瓶中除去水垢 | ||
| C. | 蛋殼浸泡在白醋中有氣體放出 | D. | pH試紙顯示白醋的pH為2~3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 使用合適的催化劑可以加大反應速率 | |
| B. | 升高溫度可以增大反應速率 | |
| C. | 增大N2濃度可以使H2轉化率達到100% | |
| D. | 增大N2濃度可以減小反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
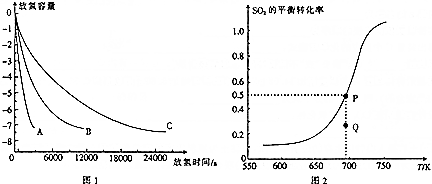
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
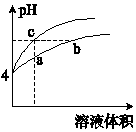 某溫度下,體積和pH都相同的鹽酸和氯化銨溶液加水稀釋時的pH變化曲線如圖所示.下列判斷正確的是( )
某溫度下,體積和pH都相同的鹽酸和氯化銨溶液加水稀釋時的pH變化曲線如圖所示.下列判斷正確的是( )| A. | a、c兩點溶液的導電能力相同 | |
| B. | a、b、c三點溶液中水的電離程度:a>b>c | |
| C. | b點溶液中:c(H+)+c(NH3•H2O)=c(OH-) | |
| D. | 用NaOH溶液和等體積b、c處溶液反應,消耗NaOH溶液的體積Vb=Vc |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com