
| A. | 使用催化劑能夠降低化學反應的反應熱(△H) | |
| B. | 金屬發生吸氧腐蝕時,被腐蝕的速率和氧氣濃度無關 | |
| C. | SO2的水溶液能夠導電,所以SO2是電解質 | |
| D. | 在同濃度的鹽酸中,ZnS可溶而CuS不溶,說明CuS的溶解度比ZnS的小 |
分析 A.催化劑能降低反應的活化能從而改變反應速率,但不改變化學平衡;
B.金屬發生吸氧腐蝕時,氧氣濃度越大,腐蝕的速率越快;
C.二氧化硫在溶液中不能電離,不屬于電解質;
D.相同條件下,溶解度越小越難溶.
解答 解:A.催化劑能降低反應的活化能從而改變反應速率,但不改變化學平衡,則不能改變反應的反應熱,故A錯誤;
B.金屬發生吸氧腐蝕時,氧氣濃度越大,腐蝕的速率越快,則被腐蝕的速率和氧氣濃度有關,故B錯誤;
C.SO2的水溶液能夠導電,導電離子是亞硫酸電離的,亞硫酸為電解質,而二氧化硫為非電解質,故C錯誤;
D.在同濃度的鹽酸中,ZnS可溶而CuS不溶,則說明CuS的溶解度比ZnS的小,故D正確;
故選D.
點評 本題考查較為綜合,涉及反應熱與焓變、電解質與非電解質、金屬腐蝕等知識,題目難度不大,注意掌握電解質與非電解質的判斷方法,A為易錯點,注意催化劑不影響反應熱,試題培養了學生的靈活應用能力.


科目:高中化學 來源: 題型:選擇題
| A. | 已知冰的熔化熱為6.0 kJ/mol,冰中氫鍵鍵能為20 kJ/mol,假設1 mol冰中有2 mol 氫鍵,且熔化熱完全用于破壞冰的氫鍵,則最多只能破壞冰中15%的氫鍵 | |
| B. | 同溫同壓下,H2(g)+Cl2=2HCl(g)在光照和點燃條件下的△H不同 | |
| C. | 實驗測得環己烷(l)、環己烯(l)和苯(l)的標準燃燒熱分別為-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以證明在苯分子中不存在獨立的碳碳雙鍵 | |
| D. | 反應A(g)?2B(g),若正反應的活化能為Ea kJ/mol,逆反應的活化能為Eb kJ/mol,則該反應的△H=(Ea-Eb) kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化學鍵 | N≡N | F-F | N-F |
| 鍵能:kJ/mol | 941.7 | 154.8 | 283.0 |
| A. | 過程F2(g)→2F(g)吸收能量 | |
| B. | 過程N(g)+3F(g)→NF3(g) 放出能量 | |
| C. | 反應N2(g)+3F2(g)=2NF3(g) 放出能量 | |
| D. | NF3吸收能量后如果沒有化學鍵的斷裂與生成,仍可能發生化學反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
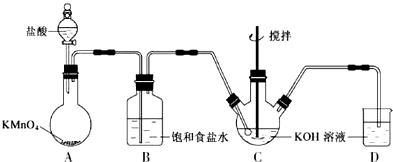
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
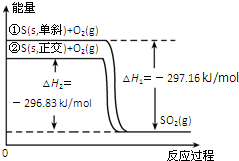
| A. | 單斜硫轉化為正交硫的反應是吸熱反應 | |
| B. | 正交硫比單斜硫穩定 | |
| C. | 相同物質的量的正交硫比單斜硫所含有的能量高 | |
| D. | ①表示斷裂1mol O2中的共價鍵所吸收的能量比形成lmolSO2中的共價鍵所放出的能量少297.16 kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷的燃燒熱△H=-890.3 kJ•mol-1,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+$\frac{3}{2}$O2(g)=CO(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 中和熱測定實驗中的終止溫度就是實驗過程中混合液的最高溫度 | |
| C. | 為了減少大氣中的霧霾,天然氣日漸成為一種備受關注的可再生的清潔能源 | |
| D. | 同溫同壓下,H2(g)+Cl2(g)=2HCl(g)在光照和點燃條件下的△H不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
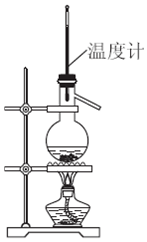
| A. | 制取乙烯 | |
| B. | 制取氯氣 | |
| C. | 分離乙醇和水 | |
| D. | 分離水和碘的四氯化碳(常壓下沸點76.8℃)溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com