
【題目】電化學原理在生產生活中應用十分廣泛.請回答下列問題: 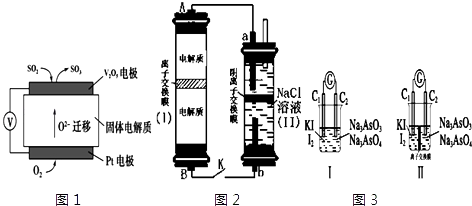
(1)通過SO2傳感器可監測大氣中SO2的含量,其工作原理如圖1所示. ①固體電解質中O2﹣向極移動(填“正”或“負”).
②寫出V2O5電極的電極反應式: .
(2)如圖2所示裝置I是一種可充電電池,裝置Ⅱ是一種以石墨為電極的家用環保型消毒液發生器.裝置I中離子交換膜只允許Na+通過,充放電的化學方程式為:2Na2S2+NaBr3 ![]() Na2S4+3NaBr ①負極區電解質為:(用化學式表示)
Na2S4+3NaBr ①負極區電解質為:(用化學式表示)
②家用環保型消毒液發生器發生反應的離子方程為 .
③閉合開關K,當有0.04mol Na+通過離子交換膜時,a電極上析出的氣體在標準狀況下體積為mL.
(3)如圖3Ⅰ、Ⅱ分別是甲、乙兩組同學將反應“AsO43﹣+2I﹣+2H+AsO33﹣+I2+H2O”設計成的原電池裝置,其中C1、C2均為碳棒.甲組向圖Ⅰ燒杯中逐滴加入適量濃鹽酸或40%NaOH溶液,電流表指針都不發生偏轉;乙組經思考后先添加了一種離子交換膜,然后向圖Ⅱ燒杯右側中逐滴加入適量濃鹽酸或適量40%NaOH溶液,發現電流表指針都發生偏轉. ①甲組電流表指針都不發生偏轉的原因是 .
②乙組添加的是(填“陰”或“陽”)離子交換膜.
【答案】
(1)負; SO2﹣2e﹣+O2﹣=SO3
(2)Na2S2、Na2S4; Cl﹣+H2O ![]() ClO﹣+H2↑;448
ClO﹣+H2↑;448
(3)氧化還原反應在電解質溶液中直接進行,沒有電子沿導線通過;陽
【解析】解:(1)①原電池中陰離子移向負極,故答案為:負;
②在V2O5電極上,SO2失電子發生氧化反應生成SO3,電極方程式為:SO2﹣2e﹣+O2﹣=SO3,故答案為:SO2﹣2e﹣+O2﹣=SO3;(2)①原電池的負極發生氧化反應,所含元素化合價升高,所以負極區電解質為:Na2S2、Na2S4,故答案為:Na2S2、Na2S4;
②電解氯化鈉溶液生成NaOH、氯氣和氫氣,氯氣與氫氧化鈉反應生成次氯酸鈉和氯化鈉,總反應的離子方程式為Cl﹣+H2O ![]() ClO﹣+H2↑,故答案為:Cl﹣+H2O
ClO﹣+H2↑,故答案為:Cl﹣+H2O ![]() ClO﹣+H2↑;
ClO﹣+H2↑;
③a極生成氯氣,b極生成氫氣,當有0.04mol Na+通過離子交換膜時,有0.04mol氫離子放電,生成氫氣0.02mol,標準狀況下體積為:0.02mol×22.4L/mol=0.448L=448mL,故答案為:448;(3)①甲組操作時,兩個電極均為碳棒,不發生原電池反應,則微安表(G)指針不發生偏轉,故答案為:氧化還原反應在電解質溶液中直接進行,沒有電子沿導線通過;
②乙組向圖ⅡB燒杯中逐滴加入適量濃鹽酸或40%NaOH溶液,發生原電池反應,A中發生I2+2e﹣═2I﹣,為正極反應,而B中As化合價升高,發生氧化反應,添加了陽離子交換膜,故答案為:陽.
(1)①原電池中陰離子移向負極;
②在V2O5電極上,SO2失電子發生氧化反應生成SO3;(2)①原電池的負極發生氧化反應;
②電解氯化鈉溶液生成NaOH、氯氣和氫氣,氯氣與氫氧化鈉反應生成次氯酸鈉和氯化鈉;
③a極生成氯氣,b極生成氫氣,當有0.04mol Na+通過離子交換膜時,有0.04mol氫離子放電;(3)①甲組向圖Ⅰ燒杯中逐滴加入適量濃鹽酸,發生氧化還原反應,不發生原電池反應;
②乙組向圖ⅡB燒杯中逐滴加入適量濃鹽酸或40%NaOH溶液,發生原電池反應,A中發生I2+2e﹣═2I﹣,為正極反應,而B中As化合價升高,發生氧化反應,以此分析.


科目:高中化學 來源: 題型:
【題目】科學家利用石墨烯和具有粘彈性的聚硅樹脂(俗稱橡皮泥)制備出一種具有極高 靈敏度的電力學傳感材料,能夠檢測輕微的變形和沖擊,其靈敏程度甚至能探測到蜘蛛的運動。該材料可用于制作檢測人體脈搏、血壓的傳感器等。實驗室模擬工業合成方法,制備聚硅樹脂的中間體氯甲基三乙氧基硅烷ClCH2Si(OEt)3 。量取20mL甲基三氯硅烷(CH3SiCl3)注入三口燒瓶中,開啟電磁攪拌加熱器升溫至66℃,從a中加入濃鹽酸,加熱A一段時間,待溫度升至110℃,停止加熱,在三口燒瓶中加入30mL無水乙醇(EtOH),迅速反應生成氯甲基三乙氧基硅烷ClCH2Si(OEt)3,待溫度降至室溫后,將三口燒瓶中液體轉移到蒸餾燒瓶中蒸餾,收集得到174.5℃餾分12mL。
物質 | C2H5OH | CH3SiCl3 | ClCH2SiCl3 | ClCH2Si(OEt)3 |
相對分子質量 | 46 | 149.5 | 184 | 212.5 |
熔點/℃ | -114.1 | -77.8 | — | — |
沸點/℃ | 78.3 | 66.4 | 116.5 | 174 |
密度/g·mL | 0.79 | 1.30 | 1.47 | 1.02 |
已知:甲基三氯硅烷為無色液體,具有刺鼻惡臭,易潮解;氯甲基三乙氧基硅烷易水解,能與堿金屬氫氧化物生成堿金屬硅醇鹽。

(1)連接好裝置后,檢驗裝置氣密性的操作是:_________________________________;
(2)A裝置中發生反應的離子方程式是:_______________________________________;
裝置C的作用是:_____________________ ;E中所裝液體是:______________;
(3)裝置D中發生反應的化學方程式為:① CH3SiCl3 + Cl2 → ClCH2SiCl3 + HCl
②__________________________________________________________________ ;
球形冷凝管的作用是:________________________;
(4)有同學發現該裝置有一處不足可能會導致實驗失敗,應該__________________________________________________;
(5) 該方法制備氯甲基三乙氧基硅烷的產率是:_______________(保留兩位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.1gH2和4gO2反應放出71.45kJ熱量,則氫氣的燃燒熱為142.9 kJmol﹣1
B.在稀溶液中,H+(aq)+OH﹣(aq)═H2O(1)△H=﹣57.3 kJmol﹣1 , 若將含0.5molH2SO4的濃硫酸與含1molNaOH的氫氧化鈉溶液混合,放出的熱量大于57.3kJ
C.HCl和NaOH反應的中和熱△H=﹣57.3 kJmol﹣1 , 則H2SO4和Ca(OH)2反應的中和熱△H=2×(﹣57.3)kJmol﹣1
D.1mol甲烷燃燒生成氣態水和二氧化碳所放出的熱量是甲烷燃燒熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應屬于吸熱反應的是( )
A. 炭燃燒生成一氧化碳 B. 中和反應
C. Ba(OH)2·8H2O與NH4Cl反應 D. 鋅粒與稀H2SO4反應制取H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D都是中學化學常見的物質,其中A、B、C均含有同一種元素。在一定條件下相互轉化的關系如下圖所示。

請回答下列問題。
(1)若通常情況下A、B、C、D都是氣體,且B和D為空氣的主要成分,寫出反應(Ⅲ)的化學方程式:_______________________。
(2)若D為氯堿工業的重要產品,A、B、C 為均含有同一種金屬元素的無機化合物,反應(Ⅲ)的離子方程式為________________________。
(3)若B為非金屬單質,且B 所含元素的原子最外層電子數與內層電子數之和的比值為3: 5,則反應(Ⅲ)中氧化產物與還原產物的物質的量之比為______,0.1mol A與含0.15molNaOH 的溶液充分反應后,溶液中所含離子濃度的大小關系為______。(已知: 常溫下H2S 的電離平衡常數Ka1= 1.3×10-7 Ka2=7.1×10-15)
(4)若A、B、C 的溶液均顯堿性,C 為焙制糕點的發酵粉的主要成分之一。
①A中所含化學鍵類型為________,D的電子式為_________
②25℃時,濃度均為0.1mol/L 的B、C 溶液,pH 較大的是______(填溶質的化學式)溶液,寫出B 溶液中顯電中性的原因:__________________(用B 溶液中有關粒子的濃度關系表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸亞鐵銨是一種淺藍綠色晶體,俗稱摩爾鹽,其化學式為:FeSO4·(NH4)2SO4·6H2O。硫酸亞鐵在空氣中易被氧化,而形成摩爾鹽后就穩定了。硫酸亞鐵銨可由硫酸亞鐵與硫酸銨等物質的量混合制得。下圖是模擬工業制備硫酸亞鐵銨晶體的實驗裝置。回答下列問題:

I.(1)先用30%的氫氧化鈉溶液煮沸廢鐵屑(含少量油污、鐵銹、FeS 等),再用清水洗凈。用氫氧化鈉溶液煮沸的目的是__________________。
(2)將處理好的鐵屑放入錐形瓶中,加入稀硫酸。錐形瓶中發生反應的離子方程式可能為________(填序號)。
A.Fe+2H+==Fe2++H2↑ B.Fe2O3+5H+===2Fe3++3H2O
C.2Fe3++S2-==2Fe2++S↓ D.2Fe3++Fe==3Fe2+
(3)利用容器②的反應,向容器①中通入氫氣,應關閉活塞_______,打開活塞______(填字母)。容器③中NaOH溶液的作用是___________;向容器①中通入氫氣的目的是___________。
I.待錐形瓶中的鐵屑快反應完時,關閉活塞B、C,打開活塞A,繼續產生的氫氣會將錐形瓶中的硫酸亞鐵(含極少部分未反應的稀硫酸)壓到飽和硫酸銨溶液的底部。在常溫下放置一段時間,試劑瓶底部將結晶出硫酸亞鐵銨。制得的硫酸亞鐵銨晶體中往往含有極少量的Fe2+。為測定晶體中Fe2+的含量,稱取一份質量為20.0g 的硫酸亞鐵銨晶體樣品,制成溶液。用0.5 mol/LKMnO4溶液滴定,當溶液中Fe2+全部被氧化,MnO4- 被還原成Mn2+時,耗KMnO4 溶液體積20.00mL。
滴定時,將KMnO4 溶液裝在____(酸式或堿式) 滴定管中,判斷反應到達滴定終點的現象為____;晶體中FeSO4的質量分數為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.酸雨是指pH小于7的降水
B.水泥、玻璃、水晶飾物和珍珠都是硅酸鹽制品
C.城市空氣質量報告中包括PM2.5、SO2、NO2、CO2等污染物
D.鋼是用量最大、用途最廣的合金,青銅是我國歷史上最早使用的合金
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是電解飽和食鹽水的裝置,通電一段時間后下列說法不正確的是

A. 陰極附近溶液的pH增大
B. 陽極產生的氣體可用濕潤的淀粉碘化鉀試紙檢驗
C. 若陽極最終收集到氣體4.48L,則反應中轉移電子的物質的量為0.4 mol
D. 完全電解后充分混合U型管中物質,所得溶液會含有NaClO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度不同壓強(P1<P2)下,可逆反應2X(g)2Y(g)+Z(g)中,生成物Z在反應混合物中的體積分數(ψ)與反應時間(t)的關系有以下圖示,正確的是( )
A.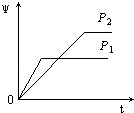
B.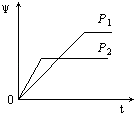
C.
D.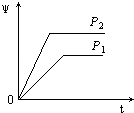
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com