
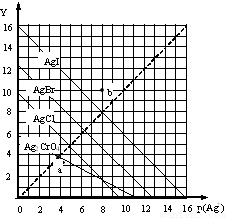
 鹵化銀AgX的沉淀溶解平衡曲線如圖所示,已知橫坐標p(Ag+)=-lgc(Ag+),縱坐標Y=-lgc(X-).下列說法正確的是( )
鹵化銀AgX的沉淀溶解平衡曲線如圖所示,已知橫坐標p(Ag+)=-lgc(Ag+),縱坐標Y=-lgc(X-).下列說法正確的是( )| A. | 該溫度下AgCl的Ksp約為1×10-15 | |
| B. | a點時c(Ag+)=c(I-),AgI處于平衡狀態 | |
| C. | b點可表示AgBr的不飽和溶液 | |
| D. | 該溫度下AgCl、AgBr飽和溶液中:c(Cl-)<c(Br-) |
分析 橫坐標p(Ag+)=-lgc(Ag+),縱坐標Y=-lgc(X-),p(Ag+)、Y越大,說明c(Ag+)、c(X-)越小,如生成沉淀,應滿足Qc>Ksp,以此解答該題.
解答 解:A.由圖象可知p(Ag+)=5,Y=5時AgCl溶液達到飽和,則Ksp=1×10-10,故A錯誤;
B.a點不在AgI的平衡曲線上,則沒有達到平衡狀態,故B錯誤;
C.b點在AgBr的平衡曲線右上側,說明p(Ag+)、Y較大,則c(Ag+)、c(X-)較小,沒有達到平衡狀態,為不飽和溶液,故C正確;
D.由圖象可知Ksp(AgBr)較小,則該溫度下AgCl、AgBr飽和溶液中:c(Cl-)>c(Br-),故D錯誤.
故選C.
點評 本題主要考查了沉淀溶解平衡曲線,為高頻考點,側重于學生的分析能力的考查,注意掌握圖線中c(Ag+)、c(X-)數值越大,實際濃度越小是解題的關鍵,難度中等.


 互動英語系列答案
互動英語系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 燒堿、液態氧、碘酒 | B. | 干冰、鐵、冰水混合物 | ||
| C. | 生石灰、白磷、熟石灰 | D. | 堿石灰、氮氣、膽礬 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ③④ | C. | ④ | D. | ①②⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A. | 氯化銀、溴化銀和碘化銀的溶解度依次增大 | |
| B. | 將硫酸銀溶解于水后,向其中加入少量硫化鈉固體,不能得到黑色沉淀 | |
| C. | 在5mL1.5×10-5 mol•L-1的NaCl溶液中,加入1滴(1mL約20滴)1.0×10-3mol•L-1的AgNO3溶液,不能觀察到白色沉淀 | |
| D. | 在燒杯中放入6.24 g 硫酸銀固體,加200 g 水,經充分溶解后,所得飽和溶液的體積為200 mL,溶液中Ag+ 的物質的量濃度為0.2 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶液顏色保持不變,說明上述可逆反應達到平衡狀態 | |
| B. | 若用綠礬(FeSO4•7H2O)作還原劑,處理1L廢水,至少需要917.4 g | |
| C. | 常溫下轉化反應的平衡常數K=l×1014.則轉化后所得溶液的pH=6 | |
| D. | 常溫下Ksp[Cr(OH)3]=1×10-32,要使處理后廢水中的c(Cr3+ )降至1×10-5mol/L,應調溶液的pH=5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
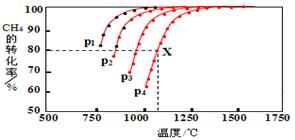 能源、環境與生產生活和社會發展密切相關.
能源、環境與生產生活和社會發展密切相關.| 容 器 | 甲 | 乙 |
| 反應物投入量 | 1molCO 2(g)和3molH2(g) | 1molCH3OH(g)和1molH2O(g) |
| 平衡時c(CH3OH) | c1 | c2 |
| 平衡時能量變化 | 放出29.4kJ | 吸收akJ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com