
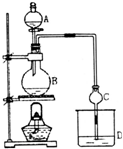
 某課外小組設計的實驗室制取乙酸乙酯的裝置如圖所示,A中放有濃硫酸,B中放有乙醇、無水醋酸鈉,D中盛有飽和碳酸鈉溶液.
某課外小組設計的實驗室制取乙酸乙酯的裝置如圖所示,A中放有濃硫酸,B中放有乙醇、無水醋酸鈉,D中盛有飽和碳酸鈉溶液.| 試劑 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸點(℃) | 34.7 | 78.5 | 118 | 77.1 |
分析 (1)酯化反應為可逆反應,且濃硫酸具有吸水性;
(2)乙醇、乙酸易溶于水,球形干燥管C中的球形結構可防止液體倒吸;飽和碳酸鈉溶液可吸收乙醇、除去乙酸,降低乙酸乙酯的溶解度;碳酸鈉溶液水解顯堿性,碳酸鈉溶液與乙酸乙酯分層;
(3)用氯化鈣除去少量乙醇,用無水硫酸鈉除去少量的水,無水硫酸鈉吸水形成硫酸鈉結晶水合物;不能選擇P2O5、堿石灰和NaOH等固體干燥劑,以防乙酸乙酯在酸性(P2O5遇水生成酸)或堿性條件下水解.
解答 解:(1)濃硫酸能與醋酸鈉反應生成乙酸,乙酸與乙醇在加熱、濃硫酸作催化劑的條件下發生酯化反應生成乙酸乙酯,該反應為可逆反應,濃硫酸吸水利于平衡向生成乙酸乙酯方向移動;乙酸酸與乙醇發生的酯化反應,反應的方程式為CH3CO18OH+C2H5OH$?_{△}^{濃H_{2}SO_{4}}$CH3COOCH2CH3+H218O,
故答案為:制乙酸、催化劑、吸水劑;CH3CO18OH+C2H5OH$?_{△}^{濃H_{2}SO_{4}}$CH3COOCH2CH3+H218O;
(2)圓底燒瓶受熱不均,球形干燥管的管口伸入液面下可以防止倒吸,同時起冷凝的作用;D中選用飽和碳酸鈉溶液的原因是乙酸乙酯與飽和Na2CO3溶液不互溶、且密度有較大差異,有利于分層,飽和Na2CO3溶液還可以吸收揮發出來的乙酸和乙醇,碳酸根離子發生水解CO32-+H2O?HCO3-+OH-,溶液呈堿性,加入幾滴酚酞,溶液呈紅色;碳酸鈉水解呈堿性,乙酸乙酯不溶于飽和碳酸鈉溶液,密度比水小,溶液分層,上層無色油體液體,乙酸和碳酸鈉反應,堿性減弱而使溶液紅色變淺;
故答案為:防止倒吸、冷凝;乙酸乙酯與飽和Na2CO3溶液不互溶、且密度有較大差異,有利于分層,飽和Na2CO3溶液還可以吸收揮發出來的乙酸和乙醇;CO32-+H2O?HCO3-+OH-;溶液分層,上層無色油體液體,下層溶液顏色變淺;
(3)用氯化鈣除去少量乙醇,用無水硫酸鈉除去少量的水,無水硫酸鈉吸水形成硫酸鈉結晶水合物,不能選擇P2O5、堿石灰和NaOH等固體干燥劑,以防乙酸乙酯在酸性(P2O5遇水生成酸)或堿性條件下水解;
故答案為:乙醇;C.
點評 本題考查有機物的制備實驗,為高頻考點,把握反應原理、實驗裝置的作用、混合物分離為解答的關鍵,側重分析與實驗能力的考查,注意吸水劑的選擇,題目難度不大.


 仁愛英語同步練習冊系列答案
仁愛英語同步練習冊系列答案 學習實踐園地系列答案
學習實踐園地系列答案科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L水中所含的分子數約為6.02×1023 | |
| B. | 標準狀況下,aL的氧氣和氮氣的混合物含有的分子數約為$\frac{a}{22.4}$×6.02×1023 | |
| C. | 常溫常壓下,48g O3氣體含有的氧原子數為6.02×1023 | |
| D. | 1mol FeCl3完全水解轉化為氫氧化鐵膠體后能生成NA個膠粒 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 組成苯的12個原子在同一平面上 | |
| B. | 苯環中6個碳碳鍵鍵長完全相同 | |
| C. | 苯的密度比水的小 | |
| D. | 苯只能發生取代反應,不能發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:2 | B. | 2:1 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 澄清的石灰水與稀鹽酸反應 Ca(OH)2+2H+=Ca2++2H2O | |
| B. | 向硝酸銀溶液中加鹽酸:Ag++C1-═AgCl↓ | |
| C. | 銅片插入硝酸銀溶液中 Cu+Ag+=Cu2++Ag | |
| D. | 氫氧化鋇溶液與硫酸的反應 OH-+H+=H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com