
【題目】NA代表阿伏加德羅常數的值,下列有關敘述錯誤的是
A. 56 g鐵粉在1mol氯氣中充分燃燒,失去的電子數為3NA
B. 標準狀況下22.4L CH4和C2H4的混合氣體所含氫原子數為4NA
C. 常溫常壓下,3.4gNH3中含N—H鍵數目為0.6NA
D. 1mol 固體NaHSO4含有的陰陽離子總數為2NA
科目:高中化學 來源: 題型:
【題目】某小組研究了銅片與![]() 反應的速率,實現現象記錄如下表。
反應的速率,實現現象記錄如下表。
實驗 | 時間段 | 現象 |
|
| 銅片表面出現極少氣泡 |
| 銅片表面產生較多氣泡,溶液呈很淺的藍色 | |
| 銅片表面均勻冒出大量氣泡 | |
| 銅片表面產生較少氣泡,溶液藍色明顯變深,液面上方呈淺棕色 |
為探究影響該反應速率的主要因素,小組進行如下實驗。
實驗I:監測上述反應過程中溶液溫度的變化,所得曲線如下圖。
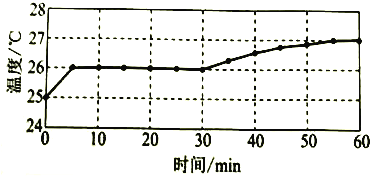
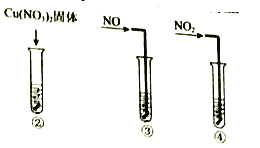
實驗II:②-④試管中加入大小、形狀相同的銅片和相同體積、 ![]() 。結果顯示:
。結果顯示:![]() 對
對![]() 和
和![]() 反應速率的影響均不明顯,
反應速率的影響均不明顯,![]() 能明顯加快該反應的速率。
能明顯加快該反應的速率。
實驗III:在試管中加入銅片和![]() ,當產生氣泡較快時,取少量反應液于試管中,檢驗后發現其中含有
,當產生氣泡較快時,取少量反應液于試管中,檢驗后發現其中含有![]() 。
。
(1)根據表格中的現象,描述該反應的速率隨時間的變化情況:____________。
(2)實驗![]() 的結論:溫度升高___________(填“是”或“不是”)反應速率加快的主要原因。
的結論:溫度升高___________(填“是”或“不是”)反應速率加快的主要原因。
(3)實驗II的目的是:__________
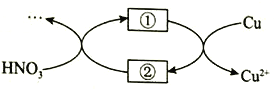
(4)小組同學查閱資料后推測:該反應由于生成某中間產物而加快了反應速率。請結合實驗II、III,在下圖方框內填入相應的微粒符號①____②_____,以補全催化機理。
(5)為驗證(4)中猜想,還需補充一個實驗:__________(請寫出操作和現象)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通常情況下,pH<7 的溶液顯酸性,pH=7 的溶液顯中性,pH>7 的溶液顯堿性。以 FeCl3 溶液為實驗對象,探究其與堿性物質之間反應的復雜多樣性。實驗如下:
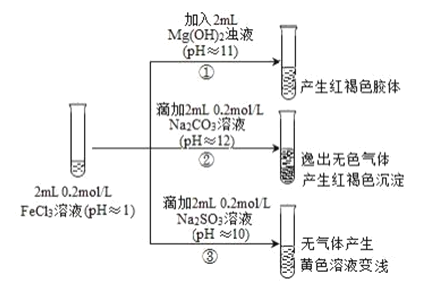
已知:含 Fe2+的溶液中加入 K3Fe(CN)6 溶液生成藍色沉淀。K3Fe(CN)6 = 3K++Fe(CN)6 3-
(1)①中反應的離子方程式是______。
(2)寫出②中發生反應的化學方程式______。
(3)對于③中的實驗現象,同學們有諸多猜測,繼續進行實驗:
甲組:取③中反應后溶液少許,滴入稀鹽酸酸化,再滴加 BaCl2 溶液,產生白色沉淀。得出結論:FeCl3 與 Na2SO3 發生了氧化還原反應,其中SO32-被氧化生成了______(填離子的化學式)。
乙組:認為甲組的實驗不嚴謹,重新設計并進行實驗,證實了甲組的結論是正確的。其實驗方案是取③中反應后的溶液,加入 K3Fe(CN)6 溶液,生成______(填藍色沉淀的化學式,沉淀中不含鉀元素),說明生成了 Fe2+。請寫出 FeCl3 與 Na2SO3 溶液反應的離子方程式:______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在一個2L的密閉容器中,加入4molA和2molB進行如下反應:3A(g)+2B(g)![]() 4C(s)+2D(g),反應一段時間后達到平衡,測得生成1.6mol C,則下列說法正確的是( )
4C(s)+2D(g),反應一段時間后達到平衡,測得生成1.6mol C,則下列說法正確的是( )
A. 該反應的化學平衡常數表達式是K=![]()
B. 此時,B的平衡轉化率是40%
C. 增大該體系的壓強,平衡向右移動,化學平衡常數增大
D. 增大B,平衡向右移動B的平衡轉化率不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA代表阿伏加德羅常數的值,下列有關敘述正確的是
A. 標準狀況下,5.6L 一氧化氮和5.6L 氧氣混合后的分子總數為0.5NA
B. 等體積、濃度均為1mol/L的磷酸和鹽酸,電離出的氫離子數之比為3:1
C. 一定溫度下,1L 0.50 mol/L NH4Cl溶液與2L 0.25 mol/L NH4Cl溶液含NH4+的物質的量不同
D. 標準狀況下,等體積的N2和CO所含的原子數均為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列化合物:①NaOH,②H2SO4,③CH3COOH,④NaCl,⑤CH3COONa,⑥NH4Cl,⑦CH3COONH4,⑧NH4HSO4,⑨NH3H2O,請回答下列問題:
(1)NH4Cl溶液中離子濃度大小順序為______________________。
(2)常溫下,pH=11的CH3COONa溶液中,水電離出來的c(OH﹣)=_____;在pH=3的CH3COOH溶液中,水電離出來的c(H+)=_____。
(3)已知水存在如下平衡:H2O+H2O![]() H3O++OH﹣△H>0,現欲使平衡向右移動,且所得溶液顯酸性,選擇的下列方法是_____。
H3O++OH﹣△H>0,現欲使平衡向右移動,且所得溶液顯酸性,選擇的下列方法是_____。
A.向水中加入NaHSO4固體 B.向水中加NaHCO3固體
C.加熱至100℃[其中c(H+)=1×10﹣6mol/L] D.向水中加入NH4Cl固體
(4)若濃度均為0.1mol/L、等體積的NaOH和NH3H2O分別加水稀釋m倍、n倍,稀釋后兩種溶液的pH都變成9,則 m_____n(填“<”、“>”或“=”)。
(5)物質的量濃度相同的⑥、⑦、⑧、⑨四種稀溶液中,NH4+濃度由大到小的順序是(填序號)_____。
(6)已知t℃時,Kw=1×10-12,在該溫度時將pH=9的NaOH溶液aL與pH=2的H2SO4溶液bL混合(忽略混合后溶液體積的變化),若所得混合溶液的pH=3,則a:b=_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電浮選凝聚法是工業上采用的一種污水處理方法:保持污水的pH在5.0~6.0之間,通過電解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉積下來,具有凈化水的作用。陰極產生的氣泡把污水中懸浮物帶到水面形成浮渣層,刮去(或撇掉)浮渣層,即起到了浮選凈化的作用。某科研小組用電浮選凝聚法處理污水,設計裝置示意圖,如圖所示。
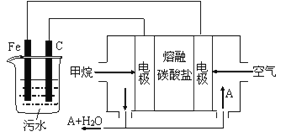
(1)實驗時若污水中離子濃度較小,導電能力較差,產生氣泡速率緩慢,無法使懸浮物形成浮渣。此時,應向污水中加入適量的__________。
a.H2SO4 b.BaSO4 c.Na2SO4 d.NaOH
(2)電解池陽極發生了兩個電極反應,電極反應式分別是
Ⅰ.___________________; Ⅱ._________________;
(3)電極反應Ⅰ和Ⅱ的生成物反應得到Fe(OH)3沉淀的離子方程式是__________________;
(4)該燃料電池是以熔融碳酸鹽為電解質,CH4為燃料,空氣為氧化劑,稀土金屬材料做電極。
①負極的電極反應是____________________;
②為了使該燃料電池長時間穩定運行,電池的電解質組成應保持穩定,電池工作時必須有部分A物質參加循環(見上圖)。A物質的化學式是_________________;
(5)實驗過程中,若在陰極產生了44.8 L(標準狀況)氣體,則熔融鹽燃料電池消耗CH4(標準狀況)____L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寫出如下化學反應方程式,如果是離子反應,則寫離子反應方程式:
(1)氯氣通入石灰乳中制取漂白粉:_________________________________
(2)漂白粉生效:_________________________________
(3)飽和的碳酸鈉溶液中通入二氧化碳:_________________________________
(4)過氧化鈉與二氧化碳反應:_________________________________
(5)次氯酸見光分解:_________________________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com