




科目:高中化學 來源: 題型:閱讀理解
 (2010?浙江)已知:
(2010?浙江)已知:
| c(H+)?c(F-) |
| c(HF) |
| c(H+)?c(F-) |
| c(HF) |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2012-2013學年福建省晉江市養正中學高二下學期第一次月考化學試卷(帶解析) 題型:填空題
(14分)已知:①25℃時弱電解質電離平衡數:Ka(CH3COOH)= ,Ka(HSCN)=0.13;難溶電解質的溶度積常數:Kap(CaF2)=
,Ka(HSCN)=0.13;難溶電解質的溶度積常數:Kap(CaF2)=
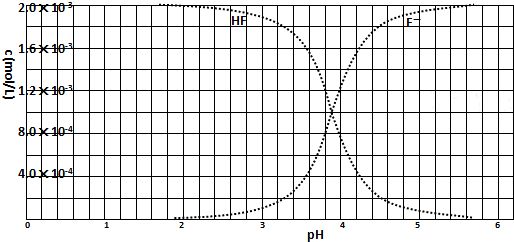
②25℃時,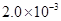 mol·L-1氫氟酸水溶液中,調節溶液pH(忽略體積變化),得到c(HF)、c(F-)與溶液pH的變化關系,如下圖所示:
mol·L-1氫氟酸水溶液中,調節溶液pH(忽略體積變化),得到c(HF)、c(F-)與溶液pH的變化關系,如下圖所示:

請根據以下信息回答下列問題:
(1)25℃時,HF電離平衡常數的數值Ka= 。
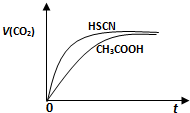
(2)25℃時,將20mL 0.10 mol·L-1 CH3COOH溶液和20mL 0.10 mol·L-1HSCN溶液分別與20mL 0.10 mol·L-1NaHCO3溶液混合,實驗測得產生的氣體體積(V)隨時間(t)變化的示意圖為圖2所示:
反應初始階段,兩種溶液產生CO2氣體的速率存在明顯差異的原因是 ,反應結束后所得兩溶液中,c(CH3COO-) c(SCN-)(填“>”、“<”或“=”)
(3) mol·L-1HF溶液與
mol·L-1HF溶液與 mol·L-1 CaCl2溶液等體積混合,調節混合液pH為4.0(忽略調節混合液體積的變化), (填“有”或“無”)沉淀產生。
mol·L-1 CaCl2溶液等體積混合,調節混合液pH為4.0(忽略調節混合液體積的變化), (填“有”或“無”)沉淀產生。
(4)已知CH3COONH4溶液為中性,又知CH3COOH溶液加到Na2CO3溶液中有氣體放出,試推斷NH4HCO3溶液的pH 7(填“>”、“<”或“=”);
將同溫度下等濃度的四種鹽溶液:?
| A.NH4Cl | B.NH4SCN? | C.CH3COONH4 | D.NH4HCO3 |
查看答案和解析>>
科目:高中化學 來源:2014屆福建省晉江市高二下學期第一次月考化學試卷(解析版) 題型:填空題
(14分)已知:①25℃時弱電解質電離平衡數:Ka(CH3COOH)= ,Ka(HSCN)=0.13;難溶電解質的溶度積常數:Kap(CaF2)=
,Ka(HSCN)=0.13;難溶電解質的溶度積常數:Kap(CaF2)=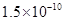
②25℃時, mol·L-1氫氟酸水溶液中,調節溶液pH(忽略體積變化),得到c(HF)、c(F-)與溶液pH的變化關系,如下圖所示:
mol·L-1氫氟酸水溶液中,調節溶液pH(忽略體積變化),得到c(HF)、c(F-)與溶液pH的變化關系,如下圖所示:


請根據以下信息回答下列問題:
(1)25℃時,HF電離平衡常數的數值Ka= 。
(2)25℃時,將20mL 0.10 mol·L-1 CH3COOH溶液和20mL 0.10 mol·L-1HSCN溶液分別與20mL 0.10 mol·L-1NaHCO3溶液混合,實驗測得產生的氣體體積(V)隨時間(t)變化的示意圖為圖2所示:
反應初始階段,兩種溶液產生CO2氣體的速率存在明顯差異的原因是 ,反應結束后所得兩溶液中,c(CH3COO-) c(SCN-)(填“>”、“<”或“=”)
(3) mol·L-1HF溶液與
mol·L-1HF溶液與 mol·L-1
CaCl2溶液等體積混合,調節混合液pH為4.0(忽略調節混合液體積的變化), (填“有”或“無”)沉淀產生。
mol·L-1
CaCl2溶液等體積混合,調節混合液pH為4.0(忽略調節混合液體積的變化), (填“有”或“無”)沉淀產生。
(4)已知CH3COONH4溶液為中性,又知CH3COOH溶液加到Na2CO3溶液中有氣體放出,試推斷NH4HCO3溶液的pH 7(填“>”、“<”或“=”);
將同溫度下等濃度的四種鹽溶液:?
A.NH4Cl B.NH4SCN? C.CH3COONH4 D.NH4HCO3
按(NH4+)由大到小的順序排列是: (填序號)。
按pH由大到小的順序排列是: (填序號)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com