
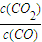 ,由數(shù)據(jù)可知,溫度越大,K越小,則升高溫度,平衡逆向移動;
,由數(shù)據(jù)可知,溫度越大,K越小,則升高溫度,平衡逆向移動;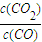 =1<K,平衡向正反應方向移動,則
=1<K,平衡向正反應方向移動,則 =4,解得x=0.6,以此計算反應速率及轉化率;
=4,解得x=0.6,以此計算反應速率及轉化率; ,由數(shù)據(jù)可知,溫度越大,K越小,則升高溫度,平衡逆向移動,說明正反應為放熱反應,所以△H<0,故答案為:<;
,由數(shù)據(jù)可知,溫度越大,K越小,則升高溫度,平衡逆向移動,說明正反應為放熱反應,所以△H<0,故答案為:<;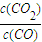 =1<K,平衡向正反應方向移動,則
=1<K,平衡向正反應方向移動,則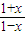 =4,解得x=0.6,
=4,解得x=0.6, =0.006mol/(Lmin),CO的轉化率為
=0.006mol/(Lmin),CO的轉化率為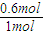 ×100%=60%,
×100%=60%,

科目:高中化學 來源: 題型:
| 溫度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常數(shù) | 4.0 | 3.7 | 3.5 |
| c(CO2) |
| c(CO) |
| c(CO2) |
| c(CO) |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2012-2013學年安徽省舒城曉天中學高二上學期第二次月考化學試卷(帶解析) 題型:填空題
高溫下CuO和CO中發(fā)生如下反應:CuO(s)+CO(g) Cu(s)+CO2(g)。
Cu(s)+CO2(g)。
已知該反應在不同溫度下的平衡常數(shù)如下:
| 溫度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常數(shù) | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化學 來源:2014屆江西省高二第一次月考化學試卷(解析版) 題型:填空題
高溫下CuO和CO中發(fā)生如下反應:CuO(s)+CO(g) Cu(s)+CO2(g)。已知該反應在不同溫度下的平衡常數(shù)如下:
Cu(s)+CO2(g)。已知該反應在不同溫度下的平衡常數(shù)如下:
|
溫度/℃ |
1 000 |
1 150 |
1 300 |
|
平衡常數(shù) |
4.0 |
3.7 |
3.5 |
請回答下列問題:
(1) 該反應的平衡常數(shù)表達式K=________,ΔH________0(填“>”“<”或“=”);
(2) 在一個容積為10 L的密閉容器中,1 000 ℃時加入Cu、CuO、CO、CO2各1.0 mol,反應經過10 min后達到平衡。求該時間范圍內反應的平均反應速率v(CO2)=________、CO的平衡轉化率=________;
(3) 欲提高(2)中CO的平衡轉化率,可采取的措施是__ __。
A.減少Cu的量 B.增加CuO的量 C.移出部分CO2 D.提高反應溫度
E.減小容器的容積 F.加入合適的催化劑
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com