
【題目】維生素C的結構簡式是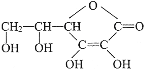 ,它的分子式是______________。由于它能防治壞血病,又稱為_______。在維生素C溶液中滴入紫色石蕊試液,溶液顏色變紅,說明維生素C溶液具有__________性;在維生素C溶液中滴入少量藍色的含有淀粉的碘水,可觀察到的現象是___________,說明維生素C具有____________性。
,它的分子式是______________。由于它能防治壞血病,又稱為_______。在維生素C溶液中滴入紫色石蕊試液,溶液顏色變紅,說明維生素C溶液具有__________性;在維生素C溶液中滴入少量藍色的含有淀粉的碘水,可觀察到的現象是___________,說明維生素C具有____________性。
 舉一反三同步巧講精練系列答案
舉一反三同步巧講精練系列答案 口算與應用題卡系列答案
口算與應用題卡系列答案 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:
【題目】A是化學實驗室中最常見的有機物,它易溶于水并有特殊香味,能進行如圖所示的多種反應。
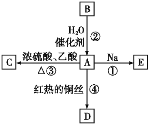
(1)A的官能團名稱是_______________________,B的結構簡式是________。
(2)反應②的反應類型為______________。
(3)寫出反應③的化學方程式:_____________________。
(4)寫出反應④的化學方程式:_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,某二元堿X(OH)2水溶液中相關組分的物質的量分數隨溶液pH變化的曲線如圖所示,下列說法錯誤的是
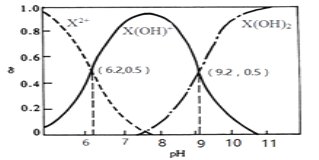
A.Kb2的數量級為10-8
B.X(OH)NO3水溶液顯酸性
C.等物質的量的X(NO3)2和X(OH)NO3混合溶液中 c(X2+)>c[X(OH)+]
D.在X(OH)NO3水溶液中,c[X(OH)2]+c(OH-)= c(X2+)+ c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米Fe2O3在常壓電化學法合成氨過程中起催化作用。該電解裝置如圖所示。已知熔融NaOH-KOH為電解液,Fe2O3在陰極發生反應生成中間體Fe。下列說法不正確的是
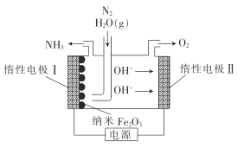
A.惰性電極II是電解池的陽極,發生氧化反應
B.生成氨氣的反應:2Fe+N2+3H2O=Fe2O3+2NH3
C.惰性電極I的電極反應:Fe2O3+3H2O+6e -=2Fe+ 6OH-
D.產生2.24LO2時,轉移的電子數為0.4NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化亞硝酰(NOC1,沸點為-5.5 °C )是有機合成中的重要試劑,為黃色氣體,具有刺鼻惡臭味,遇水反應,有多種方法制備氯化亞硝酰。已知:HNO2既有氧化性又有還原性,AgNO2微溶于水,溶于硝酸:AgNO2 + HNO3 =AgNO3+ HNO2。
(1)將5g在300°C下干燥了3h并研細的KCl粉末裝入50mL帶有接頭及抽真空用活塞的玻璃容器內。將容器盡量減壓,在減壓條件下通入0.002 mol NO2。反應12~36 min即可完成,紅棕色的NO2消失,出現黃色的氯化亞硝酰,同時還得到一種鹽,該鹽的化學式為____________, 氯化鉀需要“干燥”的原因是_____________。
(2)實驗室可由氯氣與一氧化氮在常溫常壓下合成氯化亞硝酰,裝置如圖所示。
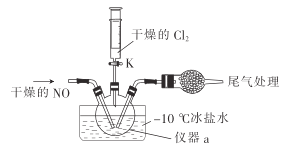
①儀器a的名稱為__________。
②干燥管中盛放的試劑為____________。
③生成NOCl的化學方程式為________________。
(3)為驗證NOCl與H2O反應后的溶液中存在Cl-和HNO2,設計如下實驗步驟,完成下列表格。
步驟 | 實驗現象或反應的化學方程式 |
①取5ml三頸燒瓶中產品,加入盛有水的燒杯中,充分反應 | NOCl與H2O發應的化學方程式_______ |
②向燒杯中滴加足量AgNO3溶液,有白色沉淀生成,再加入足量稀硝酸 | 加入稀硝酸后,實驗現象為___________ |
③向步驟②燒杯中滴加酸性KMnO4溶液 | 實驗現象為___________ |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,運用電離理論做出的預測正確的是
A.測定某二元弱酸鈉鹽溶液的pH,可能小于7
B.稀釋0.1mol/LCH3COOH(aq),![]() 可能變大也可能變小
可能變大也可能變小
C.在20.00mL濃度均為0.100 mol/L的HCl與CH3COOH混合溶液中滴加0.200mol/LNaOH溶液至pH=7,NaOH溶液體積一定小于20.00mL
D.pH=8的堿性溶液中一定沒有CH3COOH分子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖中A~J均為中學化學中常見的物質,它們之間有如下轉化關系。其中A、D為金屬單質。(反應過程中生成的水及其他產物已略去)
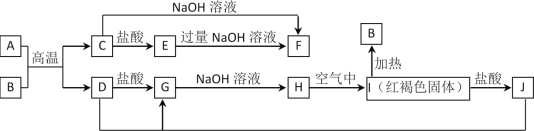
請回答以下問題:
(1)B是__________,H是_______________。(填化學式)
(2)寫出J與D反應轉化為G的離子方程式_________________________________。
(3)A在常溫下也可與NaOH溶液反應生成F,寫出此反應的化學方程式_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國某科研機構研究表明,利用K2Cr2O7可實現含苯酚廢水的有效處理,其工作原理如下圖所示。下列說法正確的是
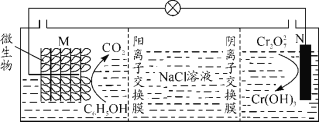
A.N為該電池的負極
B.該電池可以在高溫下使用
C.一段時間后,中間室中NaCl溶液的濃度減小
D.M的電極反應式為:C6H5OH+28e-+11H2O=6CO2↑+28H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一瓶不純的K2CO3粉末,所含雜質可能是KNO3、Ca(NO3)2、KCl、CuCl2、Na2SO4中的一種或幾種。為確定其成分,進行如下實驗:
(1)取少量該粉末于燒杯中,加入適量蒸餾水,充分攪拌,得無色澄清溶液。
(2)在上述無色溶液中加入足量的BaCl2溶液,有白色沉淀生成,過濾,得無色溶液。
(3)取少許(2)中過濾后的無色溶液于試管中,滴加AgNO3溶液有白色沉淀生成。
下列說法正確的是( )
A.雜質中可能含有KNO3、CuCl2
B.雜質中肯定不含有Ca(NO3)2、CuCl2
C.雜質中肯定含有KCl、Na2SO4
D.雜質中肯定含有KCl,可能含有KNO3、Na2SO4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com