


 ��У�n��ϵ�д�
��У�n��ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
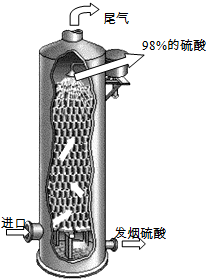 ��2011?̩�ݶ�ģ�������ڇ�(gu��)��(j��ng)��(j��)��ռ�ИO����Ҫ�ĵ�λ���҇�(gu��)�����S�F�V����Ҫ�ɷ�FeS2����ԭ�����a(ch��n)���ᣮ
��2011?̩�ݶ�ģ�������ڇ�(gu��)��(j��ng)��(j��)��ռ�ИO����Ҫ�ĵ�λ���҇�(gu��)�����S�F�V����Ҫ�ɷ�FeS2����ԭ�����a(ch��n)���ᣮ| �ɷ� | ������ǰ | �������� |
| O2 | 11% | δ�y(c��)�� |
| SO2 | 7% | δ�y(c��)�� |
| N2 | 82% | 84.8% |
| SO3 | -- | 6.9% |
| 800Q |
| a |
| 800Q |
| a |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�
| 3bmM |
| 1000a |
| 3bmM |
| 1000a |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ��2012�W(xu��)��ɽ�|ʡ�H���и߶��������I(y��)���W(xu��)ԇ�����壩 �}�ͣ�����}
���Ȼ��~��CuCl2��2H2O���к���FeCl2�s�|(zh��)�����Ƶü����Ȼ��~���w�����Ȍ����Ƴ�ˮ��Һ��Ȼ���D��ʾ�IJ������E�M(j��n)���ἃ����֪��pH�飴�����ĭh(hu��n)���У�Cu2+��Fe2+ �����ɳ�������Fe3+����ȫ����
�����ɳ�������Fe3+����ȫ����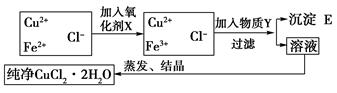
��1����ʲô����������X���ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ�
��2���������|(zh��)�������������������������m���ڱ���(sh��)�(y��n)����
| A��H2O2 ������������ | B��KMnO4 ������������ | C��NaClO������������ | D��K2Cr2O7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ��2012�W(xu��)��ɽ�|ʡ�H���и߶��������I(y��)���W(xu��)ԇ�����壩 �}�ͣ�����}
���Ȼ��~��CuCl2��2H2O���к���FeCl2�s�|(zh��)�����Ƶü����Ȼ��~���w�����Ȍ����Ƴ�ˮ��Һ��Ȼ���D��ʾ�IJ������E�M(j��n)���ἃ����֪��pH�飴�����ĭh(hu��n)���У�Cu2+��Fe2+�����ɳ�������Fe3+����ȫ����
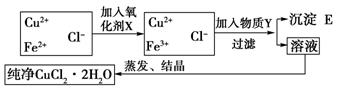
��1����ʲô����������X���ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ�
��2���������|(zh��)�������������������������m���ڱ���(sh��)�(y��n)����
A��H2O2 �������� ���� B��KMnO4 ���������� �� C��NaClO ������������ D��K2Cr2O7
��3�����|(zh��)Y�� ������E�� ��
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com