
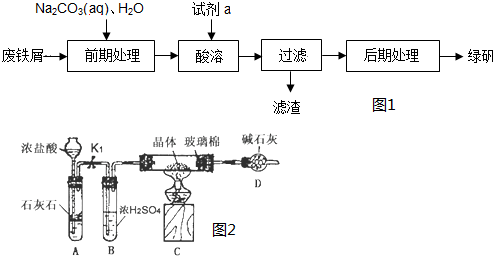
分析 廢鐵屑加入碳酸鈉溶液除去油污,加入硫酸酸溶后,為了防止亞鐵離子被氧化,加入的硫酸應適量保證鐵少量剩余,過濾時濾渣中一定含有Fe,濾液通過蒸發濃縮,冷卻結晶,過濾洗滌得到綠礬晶體;
(1)要制備硫酸亞鐵,所以要用稀硫酸溶解鐵屑,為了防止亞鐵離子被氧化,Fe不能全部消耗;
(2)酸溶時是鐵和硫酸反應生成硫酸亞鐵和氫氣;
(3)依據過濾裝置和步驟分析選擇玻璃儀器;
(4)根據已知數據求出水的質量和晶體的質量,通過以上數據得出,晶體質量為93g-80g=13g,加熱完全分解后剩余固體的質量為87.6g-80g=7.6g,根據二者的物質的量關系求出n.
解答 解:(1)要制備硫酸亞鐵,所以要用稀硫酸溶解鐵屑,為了防止亞鐵離子被氧化,Fe不能全部消耗,則加入稀硫酸時當溶液中氣泡較少時即停止加硫酸,防止Fe被耗盡;
故答案為:稀H2SO4;
(2)酸溶時發生的主要反應是鐵和硫酸反應生成硫酸亞鐵和氫氣,反應的化學方程式為:Fe+H2SO4=H2↑+FeSO4;
故答案為:Fe+H2SO4=H2↑+FeSO4;
(3)利用漏斗、玻璃棒、燒杯組裝過濾裝置進行過濾操作,所用的主要玻璃儀器有玻璃棒、漏斗、燒杯;
故答案為:漏斗;
(4)通過以上數據得出,晶體質量為93g-80g=13g,加熱完全分解后剩余固體的質量為87.6g-80g=7.6g,所以 $\frac{18n}{152}$=$\frac{13g-7.6g}{7.6g}$,解得n=6,
故答案為:6.
點評 本題考查較為綜合,涉及化學實驗方案的評價以及相關計算等知識,側重于學生的分析能力、實驗能力、計算能力的考查,注意相關基礎知識的積累,難度中等.


科目:高中化學 來源: 題型:多選題
| A. | CH2═CHCH3 | B. | CH3CH═CHCH3 | C. | (CH3)2C═C(CH3)2 | D. | CH3CH2CH═CH2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
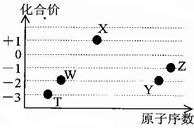 如圖是五種短周期元素的原子序數與其在氫化物中化合價的關系圖,則下列說法不正確的是( )
如圖是五種短周期元素的原子序數與其在氫化物中化合價的關系圖,則下列說法不正確的是( )| A. | X的氫化物具有很強的還原性 | |
| B. | YW2、ZW2、X2W2都能使品紅溶液褪色,且褪色原理相同 | |
| C. | Y、Z元素的最高價氧化物對應的水化物都呈酸性,而且酸性:HZO4>H2YO4 | |
| D. | 元素W、T的氫化物的沸點比同主族中相鄰的氫化物高,是因為這兩種氫化物分子間存在氫鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物 質 | 雜 質 | 試劑 | 提 純 方 法 | |
| A | BaSO4 | BaCO3 | 水 | 溶解、過濾、洗滌 |
| B | CO2 | SO2 | 飽和Na2CO3溶液 | 洗氣 |
| C | 乙酸乙酯 | 乙酸 | 稀NaOH溶液 | 混合振蕩、靜置分液 |
| D | 蛋白質 | 葡萄糖 | 濃(NH4)2SO4溶液 | 溶解、過濾、洗滌 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 (對苯醌)═N2H4+
(對苯醌)═N2H4+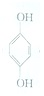 (對苯酚),N2H4的結構式為
(對苯酚),N2H4的結構式為 ,該電池正極的電極反應式為
,該電池正極的電極反應式為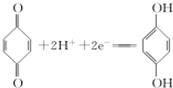 .
.| 溫度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2NO2((g)+O3(g)?N2O5(g)+O2(g)中N2O5既是氧化產物又是還原產物 | |
| B. | aA(s)+bB(g)=cC(g),若將容器體積增至原來2倍,C濃度降至原來的0.5倍,則a+b=c | |
| C. | 對于2SO2(g)+O2(g)?2SO3(g)的平衡體系,在溫度、壓強保持不變時充入少量SO3,則正反應速率減小、逆反應速率增大,平衡向逆反應方向移動 | |
| D. | 對于N2(g)+3H2(g)?2NH3(g)△H的平衡體系,僅將所有物質濃度加倍,平衡將向正反應方向移動,但△H不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
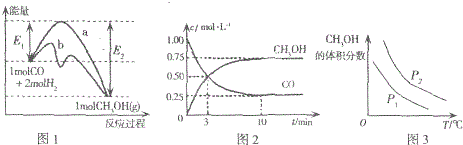
| A. | 圖1中曲線b表示使用了催化劑;該反應屬于放熱反應 | |
| B. | 當壓強不同(P1<P2)時,平衡時甲醇的體積分數隨溫度變化的曲線如圖3 | |
| C. | 一定溫度下,容器中壓強恒定時該反應已達平衡狀態 | |
| D. | 該溫度下CO(g)+2H2(g)?CH3OH(g)的化學平衡常數為10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸 | H2CO3 | 水楊酸(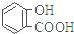 ) ) |
| 電離平衡常數(25℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-13 |
| A. | 常溫下,等濃度、等體積的NaHCO3 溶液pH小于 溶液pH 溶液pH | |
| B. | 常溫下,等濃度、等體積的Na2 CO3 溶液和 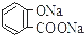 溶液中所含離子總數前者小于后者 溶液中所含離子總數前者小于后者 | |
| C. | 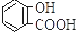 +2NaHCO3→ +2NaHCO3→ +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. | 水楊酸的第二級電離 Ka2 遠小于第一級電離Ka1 的原因之一是 能形成分子內氫鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 淀粉、纖維素和油脂都是天然高分子化合物 | |
| B. | 乙酸乙酯在堿性條件下的水解反應稱為皂化反應 | |
| C. | 乙醇能使酸性高錳酸鉀溶液褪色,發生的是氧化反應 | |
| D. | 乙烯可以與氫氣發生加成反應,苯不能與氫氣加成 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com