
為提純下列物質(括號內的物質為雜質),所選用的除雜試劑和分離方法都正確的是
A | B | C | D | |
被提純物質 | 酒精(水) | 乙醇(乙酸) | 乙烷(乙烯) | 溴苯(溴) |
除雜試劑 | 生石灰 | 氫氧化鈉溶液 | 酸性高錳酸鉀溶液 | KI溶液 |
分離方法 | 蒸餾 | 分液 | 洗氣 | 分液 |
科目:高中化學 來源:2016-2017學年遼寧省高一上開學考化學卷(解析版) 題型:推斷題
現有A、B、C、D、E、F、G七種物質,C、F是最常見的金屬,B是氣體單質,D為FeSO4溶液,G為CuSO4溶液,它們之間存在如圖所示關系:
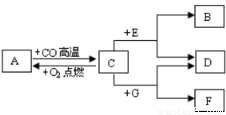
(1)推測下列物質的化學式A ,B ,F 。
(2)寫出A→C轉化的化學方程式 。
(3)寫出C+G→D+F轉化的離子方程式 。
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省高三上學期第一次月考化學試卷(解析版) 題型:選擇題
常溫下,濃度均為0.10mol/L、體積均為V0的HA和HB溶液,分別加水稀釋至體積V,pH隨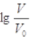 的變化如圖所示,下列敘述正確的是
的變化如圖所示,下列敘述正確的是
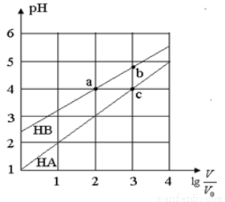
A.該溫度下HB的電離平衡常數約等于1.11×10-5
B.相同條件下NaA溶液的pH大于NaB溶液的pH
C.溶液中水的電離程度:a=c>b
D.當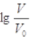 =3時,若兩溶液同時升高溫度,則
=3時,若兩溶液同時升高溫度,則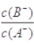 減小
減小
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二上開學考化學試卷(解析版) 題型:選擇題
海洋中有豐富的食品、礦產、能源、藥物和水產資源,下圖為海水利用的部分過程。
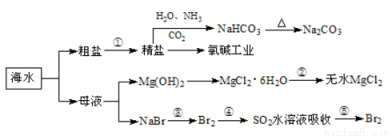
下列有關說法正確的是
A.在第③、④、⑤步驟中,溴元素均被氧化
B.制取NaHCO3的反應是利用其在此反應所涉及物質中溶解度最小
C.用澄清的石灰水可鑒別NaHCO3和Na2CO3
D.工業上通過電解飽和MgCl2溶液制取金屬鎂
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二上開學考化學試卷(解析版) 題型:選擇題
從海帶中提取碘單質,成熟的工藝流程如下,下列關于海水制碘的說法,不正確的是

A.實驗室在蒸發皿中灼燒干海帶,并且用玻璃棒攪拌
B.含I—的濾液中加入稀硫酸和雙氧水后,碘元素發生氧化反應
C.在碘水中加入幾滴淀粉溶液,溶液變藍色
D.碘水加入CCl4得到I2的CCl4溶液,該操作為“萃取”
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二上開學考化學試卷(解析版) 題型:選擇題
W、X、Y、Z均為短周期元素,W的最外層電子數與核外電子數之比為7:17;X與W同主族;Y的原子序數是W和X的原子序數之和的一半:含Z元素物質的焰色反應為黃色。下列判斷正確的是
A. 金屬性:Y>Z B. 氫化物的沸點:X>W
C. 離子的還原性:X>W D. 原子及離子半徑:Z>Y>X
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省高三上8月開學考化學試卷(解析版) 題型:填空題
某反應中反應物與生成物有:FeCl2、FeCl3、CuCl2、Cu。
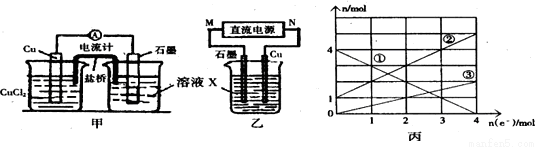
(1)將上述反應設計成的原電池如圖甲所示,請回答下列問題:
①圖中X溶液是 ;②Cu電極上發生的電極反應式為 ;
③原電池工作時,鹽橋中的 離子(填“K+”或“Cl—”)不斷進入X溶液中。
(2)將上述反應設計成的電解池如圖乙所示,乙燒杯中金屬陽離子的物質的量與電子轉移的物質的量的變化關系如圖丙,請回答下列問題:
①M是 極;②圖丙中的②線是 離子的變化。
③當電子轉移為2mol時,向乙燒杯中加入 L 5mol·L-1NaOH溶液才能使所有的金屬陽離子沉淀完全。
(3)鐵的重要化合物高鐵酸鈉(Na2FeO4)是一種新型飲用水消毒劑,具有很多優點。
①高鐵酸鈉生產方法之一是電解法,其原理為Fe+2NaOH+2H2O Na2FeO4+3H2↑,則電解時陽極的電極反應式是 。
Na2FeO4+3H2↑,則電解時陽極的電極反應式是 。
②高鐵酸鈉生產方法之二是在強堿性介質中用NaClO氧化Fe(OH)3生成高鐵酸鈉、氯化鈉和水,該反應的離子方程式為 。
③Na2FeO4能消毒、凈水的原因 。
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省高三上8月開學考化學試卷(解析版) 題型:選擇題
下列實驗“操作和現象”與“結論”對應關系正確的是( )

A.a圖,滴加乙醇,試管中橙色溶液變為綠色,乙醇發生取代反應生成乙酸
B.b圖,右邊試管中產生氣泡迅速,說明氯化鐵的催化效果比二氧化錳好
C.c圖,根據試管中收集到無色氣體,不能驗證銅與稀硝酸的反應產物是NO
D.d圖,試管中先有白色沉淀、后有黑色沉淀生成,能確定Ksp(AgCl)>Ksp(Ag2S)
查看答案和解析>>
科目:高中化學 來源:2017屆重慶市高三上學期開學考試化學試卷(解析版) 題型:填空題
W、X、Y、Z(W、X、Y、Z分別代表元素符號)均為元素周期表中前四周期的元素,其原子序數依次增大,其中W、X、Y、Z為短周期元素,它們的單質在通常情況下均為無色氣體。X元素的基態原子在同周期元素基態原子中含有的未成對電子數最多,Y元素的基態原子中s能級上的電子數等于p能級上的電子數,Z為金屬元素,其基態原子是具有4s1結構的基態原子中質子數最多的原子,試回答下列問題:
(1)寫出X的基態原子的價電子排布式_________________;
(2)比較X、Y兩元素基態原子的第一電離能大小:X__________Y(填“>”、“<”或“=”),理由是________;
(3)W、X兩元素能寫出一種常見氣體M,每個M分子中含有10個電子,M分子中心原子的雜化方式為_________;WX兩種元素還能寫出一種常見陽離子N,每個N中也含有10個電子,但在N與M中所含化學鍵的鍵角大小不同,其原因是__________;
(4)Z2+可與M分子在誰溶液中形成[Z(M)4]2+,其中M分子和Z2+通過__________-結合;
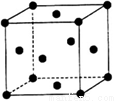
(5)單質Z的警報結構如圖所示,已知兩個最近的Z原子距離為a,Z的相對原子質量用Mr表示,則該晶體密度為_______________(只列計算式)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com