
分析 (1)根據N=$\frac{m}{M}$×NA進行計算;
(2)等溫等壓下,氣體摩爾體積相等,相同體積的氧氣和臭氧其物質的量相等,根據N=nNA計算;
(3)2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合價降低,Cl元素的化合價升高,結合方程式計算電子轉移;
(4)先計算濃硫酸的物質的量濃度,再根據溶液稀釋前后溶質的物質的量不變計算所需濃鹽酸的體積.
解答 解:(1)根據N=$\frac{m}{M}$×NA知,相同質量時其分子數與摩爾質量成反比,所以二者分子數之比=48g/mol:32g/mol=3:2,
故答案為:3:2;
(2)等溫等壓下,氣體摩爾體積相等,相同體積的氧氣和臭氧其物質的量相等,根據N=nNA知,分子數之比等于物質的量之比=1:1,
故答案為:1:1;
(3)2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合價降低,則氧化劑為KMnO4,Cl元素的化合價升高,Cl2為氧化產物,氧化產物與還原產物的物質的量之比為5:2;被氧化與未被氧化的HCl的質量之比為5:3;若有73g HCl被氧化,即2molHCl被氧化轉移2mol電子,則電子轉移的總數為2NA;
故答案為:KMnO4;Cl2;5:2;5:3;2NA;
(4)濃硫酸的物質的量濃度為$\frac{1000×1.84×98%}{98}$=18.4mol/L,設需要濃硫酸的體積為V,根據溶液稀釋前后溶質的物質的量不變得:0.2mol/L×0.5L=18.4mol/L×V,V=0.0054L=5.4mL,
故答案為:5.4.
點評 本題考查物質的量有關計算和氧化還原反應,側重考查學生計算能力和分析能力,明確各個物理量之間關系是解本題關鍵,題目難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | CO和SO2 | B. | 甲醛和苯等有機物 | ||
| C. | SO2和NO2 | D. | O3和Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下$\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| B. | 滴加石蕊試劑顯紅色的溶液中:Na+、Fe2+、Cl-、NO3- | |
| C. | 常溫下由水電離出來的c(H+)=1×10-13mol•L-1的溶液中:K+、CO32-、Cl-、NO3- | |
| D. | 常溫下,$\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
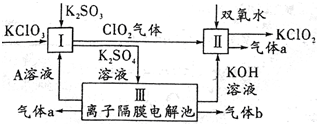 氯酸鉀(KC1O3)和亞氯酸鉀(KClO2)可以相互轉化,KClO2在堿性環境中能穩定存在,生產KClO2的主要流程如圖所示.
氯酸鉀(KC1O3)和亞氯酸鉀(KClO2)可以相互轉化,KClO2在堿性環境中能穩定存在,生產KClO2的主要流程如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在反應①中,生成3mol汞,轉移3mol電子 | |
| B. | 在反應②中,硫化汞既是氧化產物,又是還原產物 | |
| C. | 在反應③中,產生11.2L氧氣,轉移2mol電子 | |
| D. | 由反應③知,汞在空氣中加強熱會生成氧化汞 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
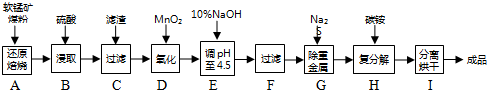
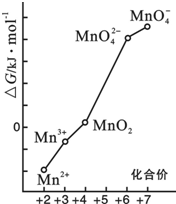
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com