
【題目】某溫度下,在2 L的密閉容器中,加入4 mol A和2 mol B進行如下反應:3A(g)+2B(g) ![]() 4C(s)+2D(g),反應一段時間后達到平衡,測得生成1.6 mol C,下列說法正確的是
4C(s)+2D(g),反應一段時間后達到平衡,測得生成1.6 mol C,下列說法正確的是
A.該反應的化學平衡常數表達式是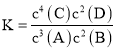
B.增加B,平衡向右移動,B的平衡轉化率增大
C.增大該體系的壓強,平衡向右移動,化學平衡常數增大
D.此時,B的平衡轉化率是40%
科目:高中化學 來源: 題型:
【題目】某有機物結構簡式為![]() ,下列敘述不正確的是( )
,下列敘述不正確的是( )
A.1mol該有機物在加熱和催化劑作用下,最多能和4molH2反應
B.該有機物能使溴水褪色,也能使酸性KMnO4溶液褪色
C.該有機物在一定條件下能發生消去反應或取代反應
D.該有機物遇硝酸銀溶液產生白色沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學方程式或離子方程式正確的是( )
A.用醋酸去除水垢:CaCO3+2H+=Ca2++H2O+CO2↑
B.甲醛與足量新制Cu(OH)2濁液反應:HCHO+2Cu(OH)2![]() HCOOH+Cu2O↓+2H2O
HCOOH+Cu2O↓+2H2O
C.實驗室用液溴和苯在催化劑作用下制溴苯:![]() +Br2
+Br2![]()
![]() +HBr
+HBr
D.將CO2通入苯酚鈉溶液:2![]() +CO2+H2O→2
+CO2+H2O→2![]() +Na2CO3
+Na2CO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯氧化銅[xCuO·yCuCl2·zH2O]在農業上用作殺菌劑。工業上用銅礦粉(主要含Cu2(OH)2CO3、Fe3O4等)為原料制取氯氧化銅的流程如下:
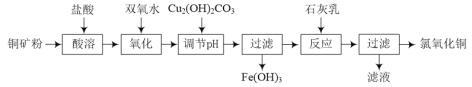
⑴“調節pH”并生成Fe(OH)3時反應的離子方程式為______。
⑵調節pH,要使常溫溶液中c(Cu2+)≥0.022mol·L-1,而c(Fe3+)≤1×10-6mol·L-1,則應調節pH的范圍為______。{已知Ksp[Cu(OH)2=2.2×10-20],Ksp[Fe(OH)3=1×10-36]}
⑶為測定氯氧化銅的組成,現進行如下實驗:
步驟Ⅰ:稱取0.4470 g氯氧化銅,放入錐形瓶,加入一定量30%的硝酸使固體完全溶解。滴加K2CrO4溶液作指示劑,用0.1000mol·L-1 AgNO3標準溶液滴定溶液中的Cl-,滴定至終點時消耗AgNO3標準溶液20.00 mL;
步驟Ⅱ:稱取0.4470g氯氧化銅,放入錐形瓶,加入一定量硫酸使固體完全溶解。向溶液中加入過量的KI固體,充分反應后向溶液中滴入數滴淀粉溶液,用0.2000mol·L-1Na2S2O3標準溶液滴定,滴定至終點時消耗Na2S2O3標準溶液20.00mL。
已知步驟Ⅱ中所發生的反應如下:
2Cu2++4I-=2CuI↓+I2 2Na2S2O3+I2=2NaI+Na2S4O6
①已知Ag2CrO4為磚紅色沉淀,步驟Ⅰ滴定終點時的實驗現象是_______。
②通過計算確定氯氧化銅的化學式________________(寫出計算過程)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種光化學電池的結構如圖所示,電池總反應為AgCl(s)+ Cu+(aq) = Ag(s)+Cu2+(aq)+Cl-(aq),下列關于該電池在工作時的說法中不正確的是
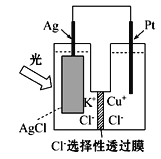
A.電子的運動方向:Pt→外電路→Ag→內電路→PtB.生成108 g銀,轉移的電子為1 mol
C.Cu+在負極發生氧化反應D.Cl-由正極遷移到負極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據報道,科學家已成功合成了少量N4,有關N4的說法正確的是( )
A.N4與N2化學性質相似
B.N4與N2互為同位素
C.相同質量的N4和N2含原子個數比為1:1
D.N4的摩爾質量是56g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉(Na2S2O3)可以除去自來水中的氯氣,在水產養殖上被廣泛應用。用純堿和硫化堿(主要成分Na2S,含少量Na2SO4、Na2CO3等)為原料制備Na2S2O3·5H2O的實驗流程如下:
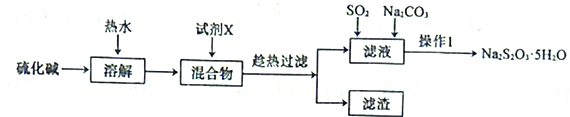
回答下列問題:
(1)試劑X是一種二元化合物的鋇鹽,它與Na2SO4反應的化學方程式為___________________。
(2)用熱水溶解并趁熱過濾的目的是______________________。
(3)利用SO2與Na2CO3、Na2S的混合溶液反應制備Na2S2O3,所需儀器如下圖:
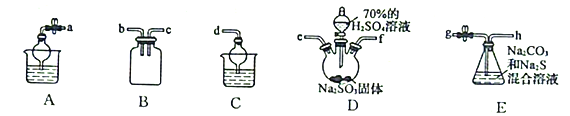
①從左到右連接各儀器,導管的接口順序為:___________接e、f接___________、___________接___________、___________接d。___________
②E中發生反應的離子方程式為______________________。
③裝置B的作用是______________________。
(4)操作1包括蒸發濃縮、______________________、___________、洗滌、干燥
(5)為測定產品Na2S2O3·5H2O的純度,準確稱取12.4gNa2S2O3·5H2O產品,配制成100mL溶液,取25.00mL溶液,以淀粉溶液作指示劑,用0.2500mol·L-1碘的標準溶液滴定,發生反應2S2O32-+I2= S4O62-+2I-,消耗碘的標準溶液20.00mL,則該產品的純度為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇來源豐富、價格低廉、運輸貯存方便,是一種重要的化工原料,有著重要的用途和應用前景,可以用多種方法合成。
Ⅰ.用CO2生產甲醇
(1)已知:H2的燃燒熱為-285.8 kJ/mol,CH3OH(l)的燃燒熱為-725.8kJ/mol,CH3OH(g)= CH3OH(l)△H=-37.3 kJ/mol,則CO2(g)+3H2(g)![]() CH3OH(g)+H2O(l)△H=_______kJ/mol。
CH3OH(g)+H2O(l)△H=_______kJ/mol。
(2)將CO2和H2按物質的量之比1:3充入體積為2.0 L的恒容密閉容器中反應,如圖兩條曲線分別表示壓強為0.1 M Pa和5.0 MPa下CO2轉化率隨溫度的變化關系。
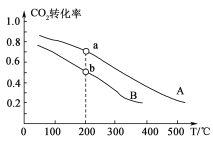
①其中a點的平衡常數表達式為:_________________。
②a,b兩點化學反應速率分別用va、vb表示,則va________vb (填“大于”、“小于”或“等于”)。
(3)在1.0 L恒容密閉容器中投入1 mol CO2和2.75 mol H2發生反應:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),實驗測得不同溫度及壓強下,平衡時甲醇的物質的量變化如圖所示,下列說法正確的是___________。
CH3OH(g)+H2O(g),實驗測得不同溫度及壓強下,平衡時甲醇的物質的量變化如圖所示,下列說法正確的是___________。
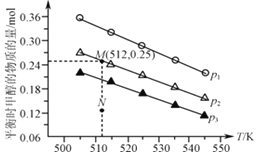
A. 該反應的正反應為放熱反應
B. 壓強大小關系為p1<p2<p3
C. M點對應的平衡常數K的值約為1.04×10-2
D. 在p2及512K時,圖中N點v(正)<v(逆)
Ⅱ.用![]() 生產甲醇
生產甲醇
(4)已知:CO(g)+2H2(g)![]() CH3OH(g),如圖是該反應在不同溫度下CO的轉化率隨時間變化的曲線。
CH3OH(g),如圖是該反應在不同溫度下CO的轉化率隨時間變化的曲線。
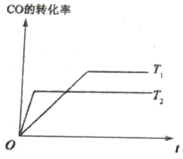
①該反應的焓變△H ______0(填“>”、“<”或“=”)。
②T1和T2溫度下的平衡常數大小關系是K1_________K2(填“>”“<”或“=”)。
Ⅲ.甲醇的應用
(5)以甲醇為主要原料,電化學合成碳酸二甲酯的工作原理如圖所示。陽極的電極反應式為___________。
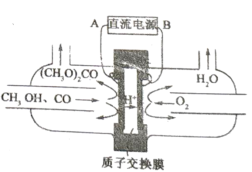
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A.激素類藥物乙烯雌酚的結構簡式為: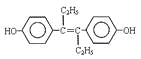 ,它的分子式是:C18H20O2
,它的分子式是:C18H20O2
B.等質量的甲烷、乙烯、乙醇分別充分燃燒,所耗用氧氣的量依次減少
C.聚乳酸(![]() )是由單體之間通過加聚反應合成的
)是由單體之間通過加聚反應合成的
D.實驗證實![]() 可使溴的四氯化碳溶液褪色,說明該分子中存在碳碳雙鍵
可使溴的四氯化碳溶液褪色,說明該分子中存在碳碳雙鍵
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com