
A是有機羧酸鹽,B、C、D是常見化合物; A、B、C、D焰色反應呈黃色,水溶液均呈堿性,其中B的堿性最強。X、Y是最常見的氧化物且與人體、生命息息相關,它們的晶體類型相同。A與B等物質的量反應生成D和一種氣體單質;C受熱分解得到Y、D和X;B與C反應生成D和X。E由兩種元素組成,式量為83,將E投入X中得到B和氣體Z,Z在標準狀況下的密度為0.76g·L-1。
(1)A的化學式是 。Y的電子式是 。
(2)X的沸點比同主族同類型物質要高,原因是 。
(3)寫出E與足量鹽酸反應的化學方程式
(4)寫出在D的飽和溶液中不斷通Y析出C的離子方程式 。
(5)A的一個重要應用是根據2A →P +H2↑得到P,P溶液中的陰離子通常用CaCl2使之沉淀,當它完全沉淀時,溶液中Ca2+的物質的量濃度至少為 。
(沉淀Ksp=2.3×10-9,當溶液中離子濃度≤10-5mol·L-1,即可認為完全沉淀)
(6)實驗室常用P與足量HCl反應所得的有機物在濃硫酸條件下共熱分解制某還原性氣體,設計實驗證明分解產物中還原性氣體的存在 。
(1)HCOONa(2分) 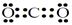 (2分)
(2分)
(2)水分子間存在氫鍵(2分)
(3)Na3N+4HCl=3NaCl+NH4Cl(2分)
(4)2Na++CO32-+H2O+CO2==2NaHCO3↓(2分)
(5)2.3×10-4mol·L-1(2分)
(6)將所得氣體先通過足量NaOH溶液,再通過澄清石灰水,無現象,點燃剩余氣體,將事先用澄清石灰水潤濕過的燒杯倒置在火焰上方,燒杯內壁變渾濁,說明有還原性氣體CO的存在。(3分)(其它合理答案也給分)
解析試題分析:① 已知A是有機羧酸鹽,B、C、D是常見化合物; A、B、C、D焰色反應呈黃色,水溶液均呈堿性。則可推知化合物A、B、C、D均為含有Na元素的堿或強堿弱酸鹽,B的堿性最強,則B為NaOH。② X、Y是最常見的氧化物且與人體、生命息息相關,它們的晶體類型相同,則X、Y應為H2O和CO2。③ 由C受熱分解得到Y、D和X;B與C反應生成D和X,可推知C為NaHCO3,D為Na2CO3;即2 NaHCO3 Na2CO3 +CO2↑+H2O; NaHCO3 +NaOH =Na2CO3 +H2O; 由此可確定X為H2O,Y為CO2。④ 由有機羧酸鹽A與NaOH等物質的量反應生成Na2CO3和一種氣體單質,可聯想到由無水醋酸鈉與NaOH加熱反應制取甲烷的脫羧反應:
Na2CO3 +CO2↑+H2O; NaHCO3 +NaOH =Na2CO3 +H2O; 由此可確定X為H2O,Y為CO2。④ 由有機羧酸鹽A與NaOH等物質的量反應生成Na2CO3和一種氣體單質,可聯想到由無水醋酸鈉與NaOH加熱反應制取甲烷的脫羧反應: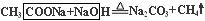 ,由此遷移可知,A為甲酸鈉(HCOONa),與等物質的量NaOH進行脫羧反應生成Na2CO3和氫氣:
,由此遷移可知,A為甲酸鈉(HCOONa),與等物質的量NaOH進行脫羧反應生成Na2CO3和氫氣: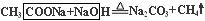 。⑤ E由兩種元素組成,式量為83,將E投入H2O中得到NaOH和氣體Z,Z在標準狀況下的密度為0.76g·L-1。由計算可知氣體Z的相對分子質量是17,則Z為NH3,由該反應:E + H2O → NaOH + NH3↑,可推知E由Na和N兩種元素組成,再根據元素化合價可確定E是Na3N。
。⑤ E由兩種元素組成,式量為83,將E投入H2O中得到NaOH和氣體Z,Z在標準狀況下的密度為0.76g·L-1。由計算可知氣體Z的相對分子質量是17,則Z為NH3,由該反應:E + H2O → NaOH + NH3↑,可推知E由Na和N兩種元素組成,再根據元素化合價可確定E是Na3N。
由此可解答:
(1)A的化學式是 HCOONa ;Y的電子式是 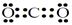
(2)X的沸點比同主族同類型物質要高的原因是:水分子間存在氫鍵,從而使分子間作用力增加,因此有較高的沸點。
(3)E與足量鹽酸反應的化學方程式:Na3N + 4HCl =" 3NaOH" + NH4Cl 。
(4)D的飽和溶液中不斷通入通Y析出C的離子方程式為:
2Na++CO32-+H2O+CO2 = 2NaHCO3↓
(5)根據2A →P +H2↑得到P,可知,2HCOONa →Na2C2O4 + H2↑,P為Na2C2O4,C2O42- + Ca2+ = CaC2O4↓,依據Ksp(CaC2O4) = c(Ca2+)?c(C2O42-) = 2.3×10-9,可計算出當CaC2O4完全沉淀時,溶液中Ca2+的物質的量濃度至少為:c(Ca2+) =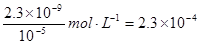 mol?L-1
mol?L-1
(6)實驗室Na2C2O4與足量HCl反應可得到H2C2O4 ,H2C2O4在濃硫酸條件下共熱分解生成CO、CO2、H2O ( 即 H2C2O4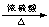 CO↑ + CO2↑+ H2O )。設計證明分解產物中存在還原性氣體CO的實驗為:將所得氣體先通過足量NaOH溶液(或通過盛有固體NaOH的干燥管),再通過澄清石灰水,若無現象,點燃剩余氣體,將事先用澄清石灰水潤濕過的燒杯倒置在火焰上方,燒杯內壁變渾濁,說明有還原性氣體CO的存在。
CO↑ + CO2↑+ H2O )。設計證明分解產物中存在還原性氣體CO的實驗為:將所得氣體先通過足量NaOH溶液(或通過盛有固體NaOH的干燥管),再通過澄清石灰水,若無現象,點燃剩余氣體,將事先用澄清石灰水潤濕過的燒杯倒置在火焰上方,燒杯內壁變渾濁,說明有還原性氣體CO的存在。
考點:物質結構、元素推斷、元素及化合物等知識


科目:高中化學 來源: 題型:填空題
(10分)Q、W、X、Y、Z是原子序數依次增大的短周期元素,X、Y是金屬元素,Q、W、Z是非金屬元素。五種元素核電荷數之和為55,對應原子最外層電子數之和為21。W、Z最外層電子數相同,但Z的核電荷數是W的2倍。
(1)Q在周期表中位于第 周期 族。
(2)X、Y各自的最高價氧化物對應的水化物可以發生反應生成鹽和水,請寫出該反應的離子方程式: 。
(3)X單質能在W單質中燃燒可生成化合物R,R的電子式 ___,該物質所含有的化學鍵的類型為 。
(4)Z的氫化物與W的氫化物發生反應生成Z單質和水,寫出其化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下表是元素周期表的一部分, 針對表中的①~⑨種元素,填寫下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ① | ② | ③ | | |
| 3 | ④ | | ⑤ | | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E五種短周期元素,已知:
①原子半徑遞增順序為:A、D、C、B、E
②短周期(除稀有氣體元素外)所有元素中A的原子半徑與E的原子半徑之比為最小
③B、C、D三種元素電子層相同,三者原子序數之和為21,且D原子次外層電子數為最外層電子數的,
請回答下列問題:
(1)寫出E單質在D單質中燃燒產物的電子式: 。(2)C2A4·H2O與NH3·H2O相似,水溶液也呈弱堿性,用電離方程式表示其水溶液呈弱堿性的原因: 。(3)B、D、E三種元素可組成常見化合物X,A、B、D、E可組成常見化合物Y,X、Y均是生活中常見的化學試劑,它們在一定條件下可互相轉化。當a mol Y轉化成amol X時:(溶液中進行)
①若加入a mol純凈物Z就可實現轉化,則加入Z為 (填一種Z物質化學式)。②若加入0.5a mol純凈物Z就可實現轉化,則加入Z為 (填一種Z物質化學式)。(4)C2A4可用作高能燃料電池的燃料,生成物之一為C的單質,惰性材料作電極,KOH作電解質溶液構成原電池,寫出負極的電極反應: ;用該電池電解過量CuSO4溶液,共收集到3.36 L(標準狀況)的氣體,電池消耗6.4 g C2A4,則該燃料的利用率為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
將下列物質按照要求由高到低的順序排列
(1)NaF、NaCl、冰醋酸、SiC四種物質的熔沸點順序: 。
(2)C、N、O三種元素的第一電離能: 。
(3)H2O的相對分子質量比H2S小,但沸點卻高的原因 。
(4)某氣態團簇分子的分子結構如圖所示,其晶體的晶胞與CO2晶體的晶胞類型相同,則該團簇分子的分子式為 。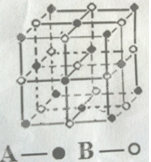
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下表是元素周期表主族元素的一部分,短周期元素X的最高正化合價是+5,Y的單質
可在空氣中燃燒。
| W | X | Y |
| | | Z |
| 編號 | 性質推測 | 化學方程式 |
| 示例 | 氧化性 | H2ZO3+4HI=Z↓+2I2+3H2O |
| 1 | | |
| 2 | | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
四種短周期元素W、X、Y、Z,原子序數依次增大,請結合表中信息回答下列問題。
| | W | X | Y | Z |
| 結構或性質 | 最高價氧化物對應的水化物與其氣態氫化物反應得到離子化合物 | 焰色反應呈黃色 | 在同周期主族元素形成的簡單離子中,離子半徑最小 | 最高正價與最低負價之和為零 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下表是元素周期表的一部分,請回答有關問題:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ① | ② | | ③ | |
| 3 | | ④ | ⑤ | | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | ⑩ | |
| 實驗步驟 | 實驗現象與結論 |
| | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C為短周期元素,在周期表中所處的位置如圖所示。A、C兩元素的原子核外電子數之和等于B原子的質子數。B原子核內質子數和中子數相等。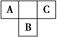
(1)A、B、C三種元素的名稱分別為________、________、________。
(2)B位于元素周期表中第______周期,第________族。
(3)C的原子結構示意圖為________,C的單質與H2反應的化學方程式為_________________________________________________________________。
(4)寫出A的氣態氫化物與B的最高價氧化物對應水化物反應的化學方程式_______________________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com