
【題目】根據碘與氫氣反應的熱化學方程式:
①I2(g)+H2(g)![]() 2HI(g) △H=-9.48kJmol-1
2HI(g) △H=-9.48kJmol-1
②I2(s)+H2(g)![]() 2HI(g)△H=+26.48kJmol-1,下列判斷正確的是
2HI(g)△H=+26.48kJmol-1,下列判斷正確的是
A.反應①的產物比反應②的產物穩定
B.254g I2(g)中通入2g H2(g),反應放熱9.48kJ
C.反應②的反應物總能量比反應①的反應物總能量低
D.1 mol固態碘與1 mol氣態碘所含的能量相差17.00 kJ
【答案】C
【解析】
A.反應①的產物與反應②的產物都是在相同狀態下的同種氣體物質,二者的穩定性相同,由于I2(g)比I2(s)能量高,所以反應①放出熱量,而②吸收熱量,A錯誤;
B.254g I2(g)的物質的量為1mol,n(H2)=1mol,由于該反應為可逆反應,則放出的熱量小于9.48kJ,B錯誤;
C.①-②,整理可得I2(g)=I2(s) △H=-35.96kJ/mol,可知I2(g)能量大于I2(s),則反應②的反應物總能量比反應①的反應物總能量低,C正確;
D.①-②,整理可得I2(g)=I2(s) △H=-35.96kJ/mol,可知I2(g)能量大于I2(s),可知1mol固態碘與1mol氣態碘所含的能量相差35.96kJ,D錯誤;
故合理選項是C。


科目:高中化學 來源: 題型:
【題目】有A、B、C、D、E 5種元素,它們的核電荷數依次增大,且都小于20。其中C、E是金屬元素;A和E屬同一族,它們原子的最外層電子排布為ns1。B和D也屬同一族,它們原子最外層的p能級電子數是s能級電子數的兩倍,C原子最外層上電子數等于D原子最外層上電子數的一半。請回答下列問題:
(1)A是________,B是________,E是_________。
(2) 寫出C元素基態原子的電子排布式_________________________。
(3)寫出D元素原子的價電子排布圖____________________。
(4) 元素B與D的電負性的大小關系是___________,C與E的第一電離能的大小關系是___________。(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家最近研究出一種環保、安全的儲氫方法,其原理可表示為:
NaHCO3+H2![]() HCOONa+H2O下列有關說法正確的是
HCOONa+H2O下列有關說法正確的是
A. 儲氫、釋氫過程均無能量變化
B. NaHCO3、HCOONa均含有離子鍵和共價鍵
C. 儲氫過程中,NaHCO3被氧化
D. 釋氫過程中,每消耗0.1molH2O放出2.24L的H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化合物G是一種治療胃及十二指腸潰瘍、反流性或糜爛性食管炎等的藥物,G 的一種合成路線如下:
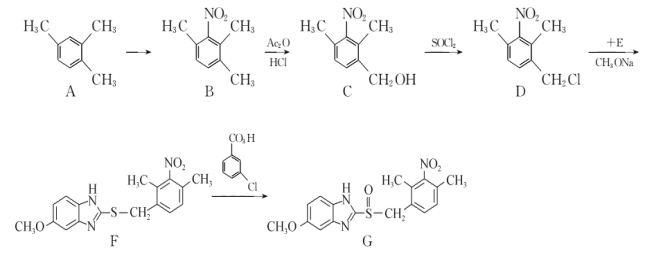
回答下列問題:
(1)A的化學名稱為____________,C中所含官能團名稱為____________。
(2)C生成D的反應類型為____________,F生成G的反應類型為____________。
(3)由A生成B的化學方程為____________。
(4)E的分子式為C8H8ON2S,其結構簡式為____________。
(5)芳香化合物W是C的同分異構體。滿足下列條件的W共有_________種(不含立體異構)。
①W分子中含氨基、羧基和羥基三種官能團
②苯環上只有兩個取代基
③能與FeCl3溶液發生顯色反應
其中核磁共振氫譜顯示有6種不同化學環境的氫的結構簡式為_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物N是制備抗抑郁藥物的重要中間體,其一種合成方法如下:

已知:i. ![]() ;
;
ii.  ;
;
iii.R—COOH![]() RCH2OH(R表示烴基)。
RCH2OH(R表示烴基)。
回答下列問題:
(1)A的化學名稱為____________,D 中含氧官能團的名稱為____________。
(2)C生成D、M生成N的反應類型分別為____________、____________。
(3)B、M的結構簡式分別為____________、____________。
(4)寫出G生成H的化學方程式:_________________。
(5)芳香族化合物X是E的同分異構體,X能與FeCl3溶液發生顯色反應,其核磁共振氫譜顯示有4種不同化學環境的氫,且峰面積比為6∶3∶2∶1,寫出1種符合要求的X的結構簡式:____________。
(6)寫出以A和![]() 為原料制備
為原料制備 的合成路線:___________(其他無機試劑任選)。
的合成路線:___________(其他無機試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】400 ℃時,將一定量的SO2和14 mol O2壓入一個盛有催化劑的10 L密閉容器中進行反應:2SO2+O2![]() 2SO3,已知2 min后,容器中剩余2 mol SO2和12 mol O2。試計算:
2SO3,已知2 min后,容器中剩余2 mol SO2和12 mol O2。試計算:
(1)生成SO3的物質的量__________________。
(2)SO2的起始物質的量濃度____________________。
(3)2 min內SO2和SO3的反應速率______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.已知:反應aA(g)+bB(g)cC(g),某溫度下,在2L的密閉容器中投入一定量的A、B,兩種氣體的物質的量濃度隨時間變化的曲線如圖所示。
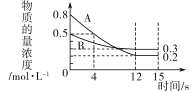
(1)經測4s時間,v(C)=0.05mol·L-1·s-1,則4s時物質C的物質的量為___________________,該反應的化學方程式為______________________。
(2)經12s時間,v(A)=___________,v(C)=___________,該反應12s時___________達到化學平衡(“是”或“否”)。
Ⅱ.(3)下列說法可以證明H2(g)+I2(g)2HI(g)已達平衡狀態的是________(填序號)。
A.單位時間內生成nmolH2的同時,生成nmolHI
B.一個H—H鍵斷裂的同時有兩個H—I鍵斷裂
C.溫度和體積一定時,混合氣體顏色不再變化
D.反應速率v(H2)=v(I2)=![]() v(HI)
v(HI)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組模擬工業生產制取HNO3設計下圖所示裝置,其中a為一個可持續鼓入空氣的橡皮球。請回答下列問題。
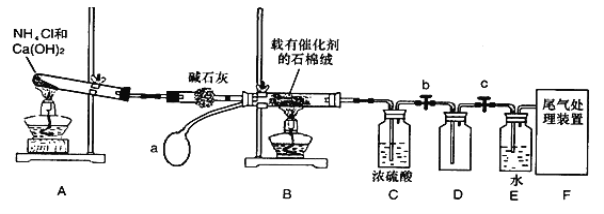
(1)寫出裝置B中主要反應的化學方程式 ________________________。
(2)裝置E中主要反應的化學方程式______________________________。
(3)裝置C中濃硫酸的作用是________________________________。
(4)請你幫助該化學小組設計實驗室制取NH3的另一方案_________________________。
(5)裝置D中的主要作用是 _______________________。
(6)干燥管中的堿石灰用于干燥NH3,某同學思考是否可用無水氯化鈣代替堿石灰,并設計下圖所示裝置(儀器固定裝置省略,擠出氣體的氣球緊套在玻璃管一端,玻璃管插在單孔橡膠塞上)進行驗證。實驗步驟如下:

①用燒瓶收集滿干燥的氨氣,立即塞上如圖所示的橡膠塞。
②正立燒瓶,使無水氯化鈣固體滑入燒瓶底部,搖動,可以觀察到的現象是______,由此,該同學得出結論:不能用CaCl2代替堿石灰。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com