
【題目】【2016宜春校級模擬】在一定溫度下,一定體積的密閉容器中有如下平衡:H2(g)+I2(g)2HI(g).已知H2和I2的起始濃度均為0.10molL﹣1時,達平衡時HI的濃度為0.16molL﹣1.若H2和I2的起始濃度均變為0.20molL﹣1,則平衡時H2的濃度(molL﹣1)是( )
A.0.16 B.0.08 C.0.04 D.0.02
【答案】C
【解析】 H2(g)+I2(g)![]() 2HI(g)
2HI(g)
起始濃度0.10molL﹣1 0.10molL﹣1 0
反應濃度0.08molL﹣1 0.08molL﹣1.16molL﹣1
平衡濃度0.02molL﹣1 0.02molL﹣1 0.16molL﹣1
化學平衡常數K=![]() =
=![]() =64
=64
當H2和I2的起始濃度均變為0.20molL﹣1時,設則平衡時H2的濃度為x(molL﹣1),
則氫氣的反應濃度為( 0.20﹣x)molL﹣1.
H2(g)+I2(g)![]() 2HI(g)
2HI(g)
起始濃度 0.20molL﹣1 0.20molL﹣1 0
反應濃度 ( 0.20﹣x)molL﹣1 ( 0.20﹣x)molL﹣1 2(0.20﹣x)molL﹣1
平衡濃度 x x 2(0.20﹣x)molL﹣1
化學平衡常數K=![]() =64, x=0.04 molL﹣1; 故選C。
=64, x=0.04 molL﹣1; 故選C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】(1)在恒溫恒壓密閉容器中充入1mol N2和3 mol H2在tl時刻達到平衡狀態后,繼續充入2 mol NH3,在t2時刻達到平衡狀態。畫出v(正)和v(逆)隨時間t的變化關系__________________

(2)恒溫恒容時,下列不能說明合成氨反應達到平衡狀態的是__________________
a.容器內N2、H2、NH3的濃度之比為1 : 3 : 2 b.v(N2)(正)=3v(H2)(逆)
c.容器內壓強保持不變 d.混合氣體的密度保持不變
e.單位時間內斷裂6mol N-H鍵的同時,有3mol H-H形成
(3)將上述制得的的氨氣溶于水配成溶液,25℃時,將amol/L的氨水與bmol/L鹽酸等體積混合,反應后溶液恰好顯中性,用a、b表示NH3·H2O的電離平衡常數Kb__________________(寫出詳細計算過程)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【2017海淀區模擬】某溫度下,將6mol CO2和8mol H2 充入2L密閉容器中發生反應CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,容器中H2的物質的量隨時間的變化關系如右圖中的實線所示.圖中虛線表示僅改變某一反應條件時,H2的物質的量隨時間的變化關系.下列說法正確的是( )

A.曲線Ⅰ對應的條件改變可能降低溫度
B.曲線Ⅱ對應的條件改變可能是充入氦氣
C.該溫度下,此反應的化學平衡常數的數值為0.5
D.從反應開始至a 點,ν(CO2)=0.6 molL﹣1min﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列能用勒夏特列原理解釋的是
A.H2、I2、HI平衡混合氣加壓后顏色變深
B.工業上由氫氣和氮氣合成氨是在較高溫度下進行的
C.Fe(SCN)3溶液中加入固體KSCN后顏色變深
D.SO2催化氧化成SO3的反應,往往需要使用催化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將純水加熱到較高溫度時,下列敘述正確的是
A.水的離子積變大、pH變小、呈酸性
B.水的離子積不變、pH變大、呈中性
C.水的離子積變小、pH變小、呈堿性
D.水的離子積變大,pH變小、呈中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應A(g)B(g)+C(g)在容積為1.0L的密閉容器中進行,A的初始濃度為0.050mol/L.溫度T1和T2下A的濃度與時間關系如右圖所示.回答下列問題:
(1)上述反應的溫度T1T2 , 平衡常數K(T1) K(T2).(填“大于”、“小于”或“等于”)
(2)若溫度T2時,5min后反應達到平衡,A的轉化率為70%,則:
①平衡時體系總的物質的量為 .
②反應的平衡常數K= .
③反應在0~5min區間的平均反應速率v(A)= .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列液體中,滴入水中會出現分層現象,但在滴入熱的氫氧化鈉溶液中時分層現象會逐漸消失的是(不考慮有機物的揮發)( )
A. 溴乙烷 B. 乙醇 C. 苯 D. 苯乙烯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【2016·西安一模】某化學興趣學習小組設計實驗探究金屬M與濃硫酸反應的氣體產物。
[提出假設] 假設1:氣體產物只有SO2; 假設2:_______________。
[實驗設計]為了探究金屬M與濃硫酸反應產物,設計如圖實驗裝置:一定量的濃硫酸與金屬M反應。
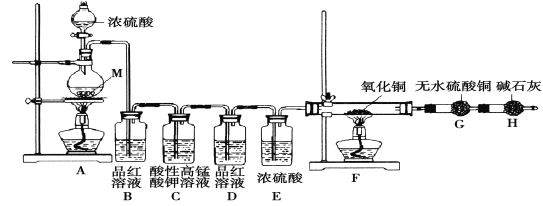
(1) 檢查上述裝置氣密性的一種方法是:關閉分液漏斗的活塞,在H裝置后面連上一根導管,然后 ,則證明裝置的氣密性良好。
(2)若B瓶里品紅溶液褪色,E、F和G中都無明顯現象。反應后硫酸鹽中金屬顯+2價。寫A中發生反應的化學方程式: ;
(3)若假設2正確,則可觀察到:F管中 ;G干燥管里 。
[實驗反思] 為了進一步探究金屬M成分和氣體組分,進行如下實驗:
稱取11.2g金屬M放入裝置A中,加入一定量的濃硫酸,反應結束后,B瓶里品紅溶液褪色,金屬沒有剩余,拆下G并稱重,G增重0.9g。
(4)為了觀察溶液顏色,實驗完畢后,需要稀釋燒瓶里溶液。稀釋燒瓶里溶液的操作方法: 。
(5)將稀釋后的溶液分裝甲、乙試管,向甲試管里滴加KSCN溶液,溶液變紅色;向乙試管里滴加酸性高錳酸鉀溶液,振蕩,溶液紫色褪去。如果燒瓶溶液中金屬離子濃度相等,則氣體成分及物質的量為 。試寫出燒瓶里發生反應的總化學方程式 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com