
【題目】下列反應不屬于四種基本反應類型,但屬于氧化還原反應的是
A.Fe+CuSO4=FeSO4+CuB.AgNO3+NaCl=AgCl↓+NaNO3
C.Fe2O3+3CO![]() 2Fe+3CO2D.MgCl2(熔融)
2Fe+3CO2D.MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
科目:高中化學 來源: 題型:
【題目】(1)用電子式表示H2O和MgBr2的形成過程:
H2O__;MgBr2__;
(2)寫出CO2、Na2O2、H2O2的電子式:
CO2_;Na2O2__;H2O2___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】同周期的X、Y、Z三種元素的最高價氧化物對應水化物的酸性由強到弱的順序是:HZO4![]() H2YO4
H2YO4 ![]() H3XO4,下列判斷正確的是 ( )
H3XO4,下列判斷正確的是 ( )
①陰離子的還原性按X、Y、Z順序減弱
②單質的氧化性按X、Y、Z順序增強
③元素的原子半徑按X、Y、Z順序減小
④氣態氫化物的穩定性按X、Y、Z順序減弱
①②A. ②③ B. ①②③ C. ①②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在120℃的條件下,將體積比為1:1總質量為7.2g的CO與H2的混合氣體在足量的O2中充分燃燒,然后將產生的氣體通過足量的Na2O2固體中充分反應,反應后固體增加的質量為( )
A.4.5 gB.7.2 gC.9.3 gD.無法計算
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C是中學化學常見的三種物質,它們之間的相互轉化關系如圖所示(部分反應條件及產物略去)。
![]()
(1)若A是一種活潑金屬,C是淡黃色固體,則C的名稱為________________,C可用在礦山、坑道、潛水或宇宙飛船等缺氧的場合,將人們呼出的CO2再轉換成O2,以供呼吸之用,請用化學方程式表示該反應原理______________________。
(2)若A是一種黃色單質固體,則B→C的化學方程式為________________。
(3)若A為能使濕潤的紅色石蕊試紙變藍的氣體,C是紅棕色氣體,且B和C易在空氣形成光化學煙霧。
①則A為________________(填寫化學式,下同),C為___________________;實驗室用熟石灰與氯化銨固體共熱制取A,寫出此化學方程式:_____________________________。
②寫出C與水反應的化學方程式:____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是常見四種有機物的比例模型示意圖。下列說法不正確的是( )
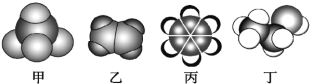
A. 甲不能使酸性高錳酸鉀溶液和溴水均褪色
B. 乙可使酸性高錳酸鉀溶液和溴水均褪色,且反應類型也相同.
C. 丙不能使酸性高錳酸鉀溶液和溴水反應而褪色
D. 丁能使酸性高錳酸鉀溶液褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬鉬在工業和國防建設中有重要的作用。鉬(Mo)的常見化合價為+6、+5、+4。由鉬精礦(主要成分是MoS2)可制備單質鉬和鉬酸鈉晶體(Na2MoO4·2H2O),部分流程如圖1所示:
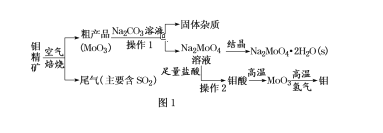
已知:鉬酸微溶于水,可溶于液堿和氨水。回答下列問題:
(1)鉬精礦焙燒時,每有1molMoS2反應,轉移電子的物質的量為______。
(2)鉬精礦焙燒時排放的尾氣對環境的主要危害是________,請你設計工業上除去該尾氣的方法(寫出兩種“變廢為寶”的方法和離子方程式):___________;___________。
(3)由鉬酸得到MoO3所用到的硅酸鹽材料儀器的名稱是_______。
(4)操作1中,加入碳酸鈉溶液充分反應后,堿浸液中c(MoO42-)=0.80mol/L,c(SO42-)=0.04mol/L,在結晶前需加入Ba(OH)2固體以除去溶液中的SO42-。當BaMoO4開始沉淀時,SO42-的去除率是_____。[Ksp(BaSO4)=1.1×1010、Ksp(BaMoO4)=4.0×108,溶液體積變化可忽略不計]
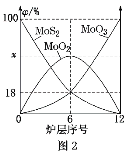
(5)焙燒鉬精礦所用的裝置是多層焙燒爐,圖2為各爐層固體物料的物質的量的百分數(φ)。
①x=_____。
②焙燒爐中也會發生MoS2與MoO3反應生成MoO2和SO2的反應,若該反應轉移6mol電子,則消耗的氧化劑的物質的量為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溴酸鎘[Cd(BrO3)2]常用于生產顏料和熒光粉。以鎘鐵礦(成分為CdO2、Fe2O3、FeO及少量的Al2O3和SiO2)為原料制備[Cd(BrO3)2]的流程如下:
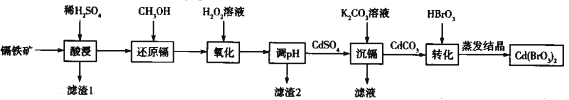
已知:Cd(SO4)2溶于水。
(1)Cd(BrO3)2中Cd的化合價為__________
(2)酸浸時,為了提高鎘的浸取率可以采取的指施有__________(寫出兩種即可)。
(3)還原鎘時,產生能使澄清石灰水變渾濁的氣體,其發生反應的離于方程式為__________
(4)用H2O2溶液氧化時,氧化劑與還原劑的物質的量之比為__________
(5)已知幾種金屬離子的氫氧化物開始沉淀和完全沉淀的pH如下表,調pH時,應調整的pH范為____,濾渣2的主要成分為_____(填化學式)。
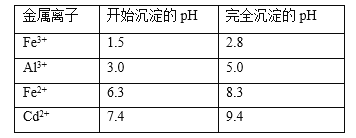
(6)實際工業生產中,有時還采用陽離子交換樹脂法來測定沉鎘后溶液中Cd2+的含量,其原理是: Cd2++2NaR=2Na++CdR2,其中NaR為陽離子交換樹脂。常溫下,將沉鎘后的溶液(此時溶液pH=6)經過陽離子交換樹脂后,測得溶液中的Na+比交換前增加了0.046g/L,則該條件下Cd(OH)2的Ksp值為____
(7)已知鎘鐵礦中CdO2的含量為72%,整個流程中鎘元素的損耗率為8%,則2t該鎘鐵礦可制得Cd(BrO3)2(相對分子質量為368)_____Kg。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某種電鍍污泥主要含有碲化亞銅(Cu2Te)、三氧化二鉻(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金屬銅和粗碲等,以實現有害廢料的資源化利用,工藝流程如下:
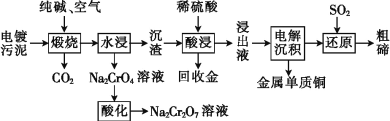
已知:煅燒時,Cu2Te發生的反應為Cu2Te+2O2![]() 2CuO+TeO2。
2CuO+TeO2。
(1)煅燒時,Cr2O3發生反應的化學方程式為__________________。
(2)浸出液中除了含有TeOSO4(在電解過程中不反應)外,還可能含有____(填化學式)。
(3)工業上用重鉻酸鈉(Na2Cr2O7)母液生產重鉻酸鉀(K2Cr2O7)的工藝流程如圖所示:
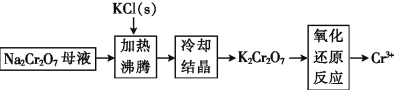
通過冷卻結晶能析出大量K2Cr2O7的原因是__________________。
(4)測定產品中K2Cr2O7含量的方法如下:稱取產品試樣2.50 g配成250 mL溶液,用移液管取出25.00 mL于錐形瓶中,加入足量稀硫酸酸化后,再加入幾滴指示劑,用0.1000 mol·L-1硫酸亞鐵銨(NH4)2Fe(SO4)2標準液進行滴定,重復進行二次實驗。(已知Cr2![]() 被還原為Cr3+)
被還原為Cr3+)
①氧化還原滴定過程中的離子方程式為________________。
②若三次實驗消耗(NH4)2Fe(SO4)2標準液的平均體積為25.00 mL,則所得產品中K2Cr2O7的純度為_____%。[已知M(K2Cr2O7)=294 g·mol-1,計算結果保留三位有效數字]。
(5)上述流程中K2Cr2O7發生氧化還原反應后所得溶液中除含有Cr3+外,還含有一定濃度的Fe3+雜質,可通過加堿調pH的方法使兩者轉化為沉淀。已知c(Cr3+)=3×10-5 mol·L-1,則當溶液中開始析出Cr(OH)3沉淀時Fe3+是否沉淀完全?____(填“是”或“否”)。{已知:Ksp[Fe(OH)3]=4.0×10-38, Ksp[Cr(OH)3]=6.0×10-31}
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com