
【題目】實驗室需要0.1 mol/L NaOH溶液450 mL和0.5mol/L硫酸溶液480 mL。根據這兩種溶液的配制情況回答下列問題:
(1)如圖所示的儀器中,配制溶液需要的是_________________(填字母),配制上述溶液還需用到的玻璃儀器是__________________________(填儀器名稱)。

(2)根據計算用托盤天平稱取NaOH的質量為_______________g。在實驗中其他操作均正確,若定容時俯視刻度線,則所得溶液濃度_____________(填“大于”“等于”或“小于”)0.1 mol/L。 若NaOH溶液在轉移至容量瓶時,灑落了少許,則需要如何操作:_______。
(3)根據計算得知,所需質量分數為98%、密度為l.84 g/cm3的濃硫酸的體積為________mL。如果實驗室有10 mL,15 mL,20 mL量筒,應選用__________mL的量筒最好。配制過程中需先在燒杯中將濃硫酸進行稀釋,稀釋時操作方法是______________。
(4)下列操作會使配制的NaOH溶液濃度偏低的是___________。
A.用濾紙稱量NaOH B.選用的容量瓶內有少量蒸餾水
C.定容搖勻后,液面下降,又加水至刻度線 D.整個配制過程中,容量瓶不振蕩
【答案】BDE 燒杯和玻璃棒 2.0 大于 重新配制 13.6 15 將濃硫酸沿燒杯內壁緩緩倒入水中,并用玻璃棒不斷攪拌 AC
【解析】
(1)配制溶液需要五種玻璃儀器:量筒、燒杯、玻璃棒、膠頭滴管、500mL容量瓶,所以如圖所示的儀器中配制溶液肯定不需要的是A、C;配制上述溶液還需用到的玻璃儀器是燒杯、玻璃棒,故答案為:BDE、燒杯和玻璃棒;
(2)因無450 mL的容量瓶,配制NaOH溶液用500 mL的容量瓶,m(NaOH)=c·V·M=0.1 mol·L-1×0.5 L×40 g·mol-1=2.0 g;若定容時俯視刻度線,溶液的體積偏小,則所得溶液濃度偏大;若NaOH溶液在轉移至容量瓶時,灑落了少許,導致溶質減少,則所得溶液濃度偏小,需要重新配制;故答案為:2.0、大于、重新配制;
(3)c(濃)·V(濃)=c(稀)·V(稀),[(1000×1.84 ×98%)÷98]×V(濃)=0.5×0.5,解得V(濃)≈0.013 6 L=13.6 mL;選用量筒的原則是比計算出來的體積稍大,誤差小,則選用15 mL量筒最好;濃硫酸的密度比水大且溶于水放出大量的熱,所以稀釋時注意三點:酸入水、沿器壁、棒攪拌,則稀釋時操作方法是將濃硫酸沿器壁緩緩倒入水中,并用玻璃棒不斷攪拌;故答案為:13.6、15、將濃硫酸沿燒杯內壁緩緩倒入水中,并用玻璃棒不斷攪拌;
(4)A.用濾紙稱量NaOH,則由于氫氧化鈉易吸水和二氧化碳,則實際稱量的質量偏少,測定結果偏低,故A符合題意;B.選用的容量瓶內有少量蒸餾水,對溶質的物質的量及溶液的體積都沒有影響,所以不影響配制結果,故B不符合題意;C.定容搖勻后,液面下降,又加水至刻度線,則測定結果偏低,故C符合題意;D.先加入的是密度較大的NaOH溶液,后加入的洗滌燒杯和玻璃棒的溶液密度較小,造成溶液密度不均勻,如果搖均勻密度大的和密度小的相溶體積會比二者原體積之和小,所配制溶液濃度偏大,故D與題意不符;故答案為:AC。


科目:高中化學 來源: 題型:
【題目】硫酸亞鐵銨[(NH4)2Fe(SO4)2·6H2O]較硫酸亞鐵不易被氧氣氧化,是分析化學中重要的試劑,常用于代替硫酸亞鐵。硫酸亞鐵銨在 500 ℃時隔絕空氣加熱完全分解,發生了氧化還原反應,固體產物可能有FeO和Fe2O3,氣體產物可能有NH3、SO3、H2O、N2和SO2。
(1)為檢驗分解產物的成分,設計如下實驗裝置進行實驗,加熱A中的硫酸亞鐵銨至分解完全。

①A中固體充分加熱較長時間后,通入氮氣,目的是__________________________。
②為驗證A中殘留物是否含有FeO,需要選用的試劑有____________(填字母)。
A.KSCN溶液 B.稀硫酸 C.濃鹽酸 D.KMnO4溶液
③裝置B中BaCl2溶液的作用是為了檢驗分解產物中是否有________氣體生成,若含有該氣體,觀察到的現象為_______________________________________。
④若A中分解產物有N2,固體殘留物只有Fe2O3,Fe2O3的物質的量為b mol,C中沉淀物質的量為a mol,則b________________a(填“大于”“小于”或“等于”)。
⑤實驗中,觀察到C中有白色沉淀生成,則C中發生的反應的離子方程式為______________________
(2)為測定某固體樣品中(NH4)2Fe(SO4)2·6H2O的含量,某實驗小組做了如下實驗:
步驟一:準確稱量20.00 g硫酸亞鐵銨晶體,配制成100 mL溶液。
步驟二:取所配溶液25.00 mL于錐形瓶中,加稀H2SO4酸化,實驗測定其與16.00mL 0.1000 mol/L KMnO4溶液恰好完全反應。已知(NH4)2Fe(SO4)2·6H2O的摩爾質量是392g/mol,則產品中(NH4)2Fe(SO4)2·6H2O的質量分數為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氰化氫(HCN)是形成生物重要化合物的重要源或中間體,其水溶液稱氫氰酸,是一種非常弱的酸。工業上以甲烷和氨氣為原料在高溫和催化劑的作用下按下列反應制備HCN:
2CH4(g)+3O2(g)+2NH3(g)![]() 2HCN(g)+6H2O(g) △H1=-475kJ/mol①
2HCN(g)+6H2O(g) △H1=-475kJ/mol①
CH4(g)+NH3(g)![]() HCN(g)+3H2(g) △H2=+240kJ/mol②
HCN(g)+3H2(g) △H2=+240kJ/mol②
(1)該條件下1mol水蒸氣分解為氫氣和氧氣的熱化學方程式為________________________(數值保留三位有效數字)。根據題中信息_______________(填“能”或“不能”)計算出氫氣的燃燒熱。
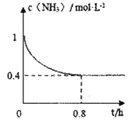
(2)在恒溫恒容的密閉容器中按照體積比6:5的比例充入甲烷和氨氣發生反應②,氨氣的物質的量濃度與時間關系如圖所示,從開始到0.8h達平衡狀態的過程中v(H2)=____________________;甲烷的平衡轉化率為____________;該溫度下反應②的平衡常數K=________________________。
(3)工業生產中反應②常用鉑作催化劑,甲、乙兩名同學在討論催化劑的選擇,甲同學認為用鉑作催化劑會提高生產成本,應研究出更廉價的催化劑;乙同學認為使用鉑不會明顯提高生產成本。你認為觀點更合理的是___________(填“甲”或“乙”),原因是______________________________。
(4)HCN及其鹽均有劇毒,因此含CN-的工業廢水必須經過處理才能排放,處理方法之一是電解氧化法;以石墨為陽極、鐵板為陰極電解含CN-的堿性廢水,將CN-轉化為N2和CO2。該方法的陽極反應式為___________________________。為確保CN-被完全處理掉,電解一段時間后通常會加入適量氯化鈉固體,其作用可能是_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的離子方程式正確的是:
A. 將銅絲插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. 向Fe2(SO4)3溶液中加入過量鐵粉:Fe3++Fe===2Fe2+
C. 向Al2(SO4)3溶液中加入過量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
D. 向Na2SiO3溶液中滴加稀鹽酸:Na2SiO3+2H+===H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X2﹣與Y+離子都與Ar原子具有相同的核外電子排布,則下列敘述中正確的是( )
A.原子序數X>Y
B.離子半徑X>Y
C.X和Y一定在同一周期
D.X是第IIA族元素,Y是第VIIA族元素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】最近我國科研人員成功攻克了5G通信芯片制造中關鍵材料—氮化鎵的研制難題。已知元素鎵(Ga)與Al同主族,氮化鎵中鎵顯最高正價,氮顯最低負價。則氮化鎵的化學式為( )
A.Ga2N3B.GaN2C.GaND.Ga3N2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎳廢料中主要含有Ni,還有少量的Cu、Fe、Pb等。現從中制取Ni2O3,可用于制造人造衛星、宇宙飛船的高能電池,也可用于制成鎳鎘堿性電池。生產流程見下:

已知0.010mol/L金屬離子在不同pH下的沉淀情況如下:
Fe3+ | Cu2+ | Ni2+ | Fe2+ | |
開始沉淀pH | 3.0 | 5.0 | 7.4 | 9.7 |
完全沉淀pH | 4.0 | 6.5 | 9.0 | 11 |
回答下列問題:
(1)加入碳酸鈣調pH的目的是____________________________________________,“沉渣2”的主要成分是____________,必須先過濾“沉渣1”后再進行“除Cu”的原因是______________________________________________________________________。
(2)用離子方程式解釋加入NH4F“除Ca”的過程_________________。
(3)“酸浸”時參與反應的H2SO4與HNO3物質的量比保持為3∶2,此時Ni單質所發生的化學方程式為___________________________________________。
(4)“操作X”是__________、__________,煅燒時產生兩種氣體的成分是________。
(5)向NiO中加入鹽酸溶解,待完全溶解后,加入足量NaOH溶液,再加入NaClO溶液,寫出其中和NaClO相關的反應的離子方程式為_________________________________。
(6)根據上表數據,計算當0.010mol/LNiSO4溶液中Ni2+完全沉淀時的c(Ni2+)=______mol/L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com