
| A. | 反應中,每生成1molH2轉移的電子數均為2mol | |
| B. | 參加反應的金屬Na、Mg、Al的物質的量之比為1:2:3 | |
| C. | 鎂的物質的量為0.1mol | |
| D. | V=2.24 |
分析 Na、Mg、Al均與鹽酸反應生成氫氣,鹽酸不足時,Mg、Al不能與水反應,而Na能與水反應生成氫氣,根據氫元素守恒,可知Mg、Al與鹽酸反應最多生成氫氣為0.1L×2mol/L×$\frac{1}{2}$=0.1mol,其體積為0.1mol×22.4L/mol=2.24L,由關系式:2Na~H2,Mg~H2,2Al~3H2,可得生成氣體與金屬的物質的量關系圖為: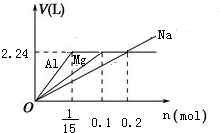 ,據此解答.
,據此解答.
解答 解:A、反應中,每生成1molH2需2mol氫離子得電子,所以轉移的電子數均為2mol,故A正確;
B、Na、Mg、Al均與鹽酸反應生成氫氣,鹽酸不足時,Mg、Al不能與水反應,而Na能與水反應生成氫氣,根據氫元素守恒,可知Mg、Al與鹽酸反應最多生成氫氣為0.1L×2mol/L×$\frac{1}{2}$=0.1mol,其體積為0.1mol×22.4L/mol=2.24L,由關系式:2Na~H2,Mg~H2,2Al~3H2,可得生成氣體與金屬的物質的量關系圖為: ,
,
反應生成氣體的體積均為VL(標準狀況下),說明反應生成氫氣為2.24L,金屬Al、Mg過量,Na恰好完全反應,參加反應的金屬Na、Mg、Al的物質的量分別為0.2mol、0.1mol、$\frac{1}{15}$mol,參加反應的金屬Na、Mg、Al的物質的量之比為0.2mol:0.1mol:$\frac{1}{15}$mol=6:3:2,綜上分析可知,故B錯誤;
C、由B可知,鎂的物質的量為0.1mol,故C正確;
D、Na、Mg、Al均與鹽酸反應生成氫氣,鹽酸不足時,Mg、Al不能與水反應,而Na能與水反應生成氫氣,根據氫元素守恒,可知Mg、Al與鹽酸反應最多生成氫氣為0.1L×2mol/L×$\frac{1}{2}$=0.1mol,其體積為0.1mol×22.4L/mol=2.24L,故D正確;
故選ACD.
點評 本題考查化學方程式的有關計算,屬于討論型計算,題目采取圖象法便于判斷金屬與鹽酸反應情況,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | c(H+)•c(OH-)=KW | B. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)+c(OH-) | D. | c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{a}{576V}$ mol•L-1 | B. | $\frac{a}{125}$ mol•L-1 | C. | $\frac{250a}{36V}$mol•L-1 | D. | $\frac{250a}{48V}$mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 密閉、低溫是存放氨水的必要條件 | |
| B. | 實驗室常用排飽和食鹽水法收集氯氣 | |
| C. | 打開汽水瓶時,有大量氣泡冒出 | |
| D. | 已知合成氨的反應為N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol,工業上采用較高溫度和使用催化劑以提高氨氣的產率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH(CH3)CH2CH3 2-甲基丁烷 | B. | 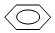 間二甲苯 間二甲苯 | ||
| C. | CH3CH2CH2CH2OH 1-羥基丁烷 | D. | 2-甲基-2-丙烯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 霧是氣溶膠,在陽光下可觀察到丁達爾效應 | |
| B. | 預制備Fe(OH)3膠體,向盛有沸水的燒杯中加入FeCl3飽和溶液煮沸得紅褐色沉淀 | |
| C. | 用石膏或鹵水點制豆腐利用了膠體的性質 | |
| D. | 用雞蛋殼膜和蒸餾水除去淀粉膠體中的食鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Cu2+、Cl-、SO42- | B. | Fe3+、K+、SO42-、NO3- | ||
| C. | H+、Mg2+、OH-、NO3- | D. | Na+、Ca2+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com