
| A. | Cu$\stackrel{{H}_{2}S{O}_{4}}{→}$CuSO4$\stackrel{Ba(N{O}_{3})_{2}}{→}$Cu(NO3)2 | |
| B. | Cu$\stackrel{{O}_{2}}{→}$CuO$\stackrel{HN{O}_{3}}{→}$Cu(NO3)2 | |
| C. | Cu$\stackrel{{O}_{2}}{→}$CuO$\stackrel{{H}_{2}O}{→}$Cu(OH)2$\stackrel{HN{O}_{3}}{→}$Cu(NO3)2 | |
| D. | Cu$\stackrel{HN{O}_{3}}{→}$Cu(NO3)2 |
分析 綠色化學要求盡可能地利用原料并保證生產過程無污染,且在經濟、環保和技術上有設計可行性,據此解答.
A、銅與硫酸反應生成二氧化硫,會有污染物生成;
B、Cu生成CuO,再生成硝酸銅,整個過程中無污染物的生成;
C、將CuO轉化為Cu(OH)2,在技術上難以實現;
D、銅與硝酸反應生成一氧化氮或者二氧化氮,都會有污染物生成;
解答 解:A、銅與硫酸反應生成二氧化硫,會有污染物生成,不符合“綠色化學”的思想,故A錯誤;
B、Cu生成CuO,再生成硝酸銅,整個過程中無污染物的生成,符合“綠色化學”的思想,故B正確;
C、將CuO轉化為Cu(OH)2,在技術上難以實現,且增加了步驟,不符合“綠色化學”中經濟性的要求,故C錯誤;
D、銅與硝酸反應生成一氧化氮或者二氧化氮,都會有污染物生成,不符合“綠色化學”的思想,故D錯誤;
故選:B.
點評 本題通過生活環境污染及治理的綠色化學問題考查了硝酸、硫酸和銅反應的實質問題,本題難度不大,注意反應的產物即可.


 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:解答題
| 元素 | 相 關 信 息 |
| X | X的基態原子核外3個能級上有電子,且每個能級上的電子數相等 |
| Y | Y元素的激發態原子的電子排布式為1s22s22p63s23p34s1 |
| Z | Z和Y同周期,Z的電負性大于Y |
| W | W的一種核素的質量數為63,中子數為34 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1L水中含有1molH2SO4 | B. | 1L溶液中含有1molH+ | ||
| C. | 1LH2SO4溶液中含98g H2SO4 | D. | 將98g H2SO4溶于1L水配成溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 一定含有Al,其質量為4.5g | |
| B. | 一定含有(NH4)2SO4和MgCl2,且物質的量相等 | |
| C. | 一定含有MgCl2和FeCl2 | |
| D. | 一定不含FeCl2,可能含有MgCl2和AlCl3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .某探究小組在實驗室探究阿司匹林的合成,主要原料是水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O],制備基本實驗流程如下:
.某探究小組在實驗室探究阿司匹林的合成,主要原料是水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O],制備基本實驗流程如下:
| 名稱 | 相對分子質量 | 熔點或沸點(℃) | 水溶性 |
| 水楊酸 | 132 | 158(熔點) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸點) | 與水反應 |
| 乙酰水楊酸 | 180 | 135(熔點) | 微溶 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
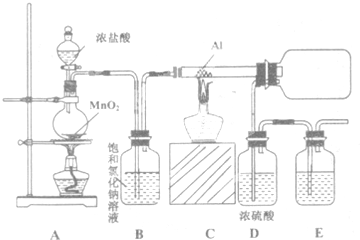
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
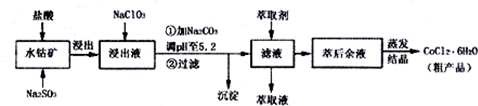
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)2 | Mn(OH)2 |
| 開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
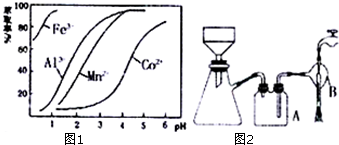
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 溫度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常數 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
| A. | 該反應的正反應是吸熱反應 | |
| B. | 100℃時,向體積為V1L的恒容密閉容器中充入2mol CO和4mol H2,達到平衡時,CO的轉化率為40%,則V1=12 | |
| C. | 250℃時,向體積為V2L的恒容密閉容器中充入3mol CO和3mol H2,達到平衡時,混合氣體中CO的體積分數為50% | |
| D. | 250℃時,向體積為V2L的恒容密閉容器中充入3mol CO和3mol H2,達到平衡時,混合氣體中CH3OH(g)的體積分數為62.5% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高一定的溫度 | |
| B. | 加入100 mL 0.1 mol•L-1的醋酸溶液 | |
| C. | 加入少量的0.5 mol•L-1的硫酸 | |
| D. | 加入少量的1 mol•L-1的NaOH溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com