
【題目】A、B、C、D、E、F是元素周期表中前四周期元素,且原子序數依次增大,其相關信息如下:
①A的周期序數等于其主族序數;
②B、D原子的L層中都有兩個未成對電子;
③E元素原子最外層電子排布式為(n+1)Sn(n+1)Pn-1;
④F原子有四個能層,K、L、M全充滿,最外層只有一個電子。
試回答下列問題:
(1)基態E原子中,電子占據的最高能層符號為_____,F的價層電子排布式為_________________。
(2)B、C、D的電負性由大到小的順序為_________(用元素符號填寫),C與A形成的分子CA3的VSEPR模型為__________。
(3)B和D分別與A形成的化合物的穩定性:BA4小于A2D,原因是______________________________。
(4)以E、F的單質為電極,組成如圖所示的裝置,E極的電極反應式為_____________________________。

(5)向盛有F的硫酸鹽FSO4的試管里逐滴加入氨水,首先出現藍色沉淀,繼續滴加氨水,藍色沉淀溶解,得到深藍色溶液,再向深藍色透明溶液中加入乙醇,析出深藍色晶體。藍色沉淀溶解的離子方程式為___________________________。
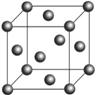
(6)F的晶胞結構(面心立方)如右圖所示:已知兩個最近的F的距離為acm,F的密度為__________g/cm3(阿伏加德羅常數用NA表示,F的相對原子質量用M表示)
【答案】 M 3d104s1 O>N>C 四面體 H2O中共價鍵的鍵能高于CH4中共價鍵的鍵能或非金屬性O大于C,氣態氫化物的穩定性H2O大于CH4 Al-3e-+4OH-=AlO2-+2H2O Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-或 Cu(OH)2+4NH3H2O=[Cu(NH3) 4]2++2OH-+4H2O, ![]()
【解析】A的周期序數等于其主族序數,結合A、B、C、D、E、F是元素周期表中前四周期元素,可知A為H;B、D原子的L層中都有兩個未成對電子,即2p2或2p4,則B為碳、D為O,根據核電荷數遞增,可知C為N;E元素原子最外層電子排布式為(n+1)Sn(n+1)Pn-1,則n=2,E為Al;F原子有四個能層,K、L、M全充滿,最外層只有一個電子,則其電子排布式為[Ar]4s1,核電荷數為29,應為Cu;
(1)Al為第三周期ⅢA元素,則基態Al原子中,電子占據的最高能層符號為M,Cu的核電荷數為29,其電子排布式為[Ar]3d104s1,則價層電子排布式為3d104s1;
(2)非金屬性越強,電負性越大,則C、N、O的電負性由大到小的順序為O>N>C;氨氣分子中氮價層電子對個數=σ鍵個數+孤電子對個數=3+![]() (5-3×1)=4,VSEPR模型為正四面體結構,含有一個孤電子對,所以其空間構型為三角錐形;
(5-3×1)=4,VSEPR模型為正四面體結構,含有一個孤電子對,所以其空間構型為三角錐形;
(3)非金屬性越強,氫化物越穩定,O的非金屬性比碳強,則CH4穩定性小于H2O;
(4)以Al、Cu和NaOH溶液組成原電池,因Al與NaOH之間存在自發的氧化還原反應,反應方程式為2Al+2H2O+2NaOH=2NaAlO2+3H2↑,可知Al為原電池的負極,電極反應式為Al-3e-+4OH-=AlO2-+2H2O;
(5)氨水和硫酸銅反應生成氫氧化銅藍色沉淀,當氨水過量時,氨水和氫氧化銅反應生成可溶性的銅氨絡合物,所以難溶物溶解得到深藍色的透明溶液,涉及的離子方程式為:Cu2++2NH3H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;
(6)該晶胞為面心立方,晶胞中含有數目為8×![]() +6×
+6×![]() =4,則晶胞質量為
=4,則晶胞質量為![]() g,已知兩個最近的Cu的距離為acm,可知晶胞的邊長為
g,已知兩個最近的Cu的距離為acm,可知晶胞的邊長為![]() acm,該晶胞體積為(
acm,該晶胞體積為(![]() a)3cm3,則密度ρ=
a)3cm3,則密度ρ=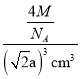 =
=![]() g/cm3。
g/cm3。


科目:高中化學 來源: 題型:
【題目】下列敘述不正確的是( )
A.過氧化氫中既含有極性鍵又含有非極性鍵
B.18O原子中含有18個中子
C.含有相同電子數的H2O和NH3的分子數相同
D.苯分子中所有原子共處在同一平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液中各微粒的濃度關系不正確的是 ( )
A. pH=2的HA溶液與pH=12的MOH溶液任意比混合:c(H+) + c(M+) == c(OH-) + c(A-)
B. 1 L 0.1 mol·L-1 (NH4)2Fe(SO4)2的溶液中:c(SO![]() )>c(NH
)>c(NH![]() )>c(Fe 2+)>c(H+)>c(OH-)
)>c(Fe 2+)>c(H+)>c(OH-)
C. 0.1 mol·L-1 NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO![]() )+c(OH-)
)+c(OH-)
D. 0.1mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探索工業含鋁、鐵、銅合金廢料的再利用,甲同學設計的實驗方案如下:

回答下列問題:
(1)操作①的名稱為__________,沉淀C的化學式為______________。
(2)在濾渣B中滴加稀硫酸時,發現反應速率比同濃度硫酸與純鐵粉反應要快,原因是_______________________。
(3)在濾渣B中滴加的硫酸可用SO2制取,可按以下三步進行:
已知25℃、101kPa時:
2SO2(g)+O2(g)2SO3(g) △H1=-197kJ/mol
H2O(g)=H2O(l) △H2=-44kJ/mol
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=-545kJ/mol
則SO3(g)與H2O(l)反應的熱化學方程式是_________________。
(4)設計實驗方案,檢測濾液D中含有的金屬離子(試劑自選)________________________。
(5)常溫下,乙同學將綠礬配成約0.1molL-1FeSO4溶液,測得溶液的pH=3,請用離子方程式解釋其原因_______,該溶液中c(SO42-)-c(Fe2+)=______molL-1(填近似數值)。
(6)在濾渣E中加入稀硫酸和試劑Y制膽礬晶體是一種綠色化學工藝,試劑Y為無色液體,則反應④的總反應化學方程式為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】藥物阿司匹林可由水楊酸制得,它們的結構如圖所示。有關說法正確的是( )
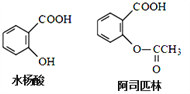
A. 1 mol阿司匹林最多可消耗3 molH2
B. 水楊酸分子中所有原子不可能共面
C. 水楊酸可以發生取代、加成、氧化、加聚反應
D. 1 mol阿司匹林最多可消耗2 molNaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“綠色、高效”概括了2005年諾貝爾化學獎的特點。換位合成法在化學工業中每天都在應用,主要用于研制新型藥物和合成先進的塑料材料。在“綠色化學工藝”中,理想狀態是反應物中的原子全部轉化為欲制得的產物,即原子利用率為100%。①置換反應 ②化合反應 ③分解反應 ④取代反應 ⑤加成反應⑥消去反應 ⑦加聚反應 ⑧縮聚反應等反應類型中能體現這一原子最經濟原則的是( )
A.①②⑤ B.②⑤⑦C.⑦⑧D.⑦
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在日常生活中,下列解決問題的方法不可行的是( )
A. 為加快漂白精的漂白速率,使用時可滴加幾滴醋酸 B. 為防止海鮮腐爛,可將海鮮產品浸泡在硫酸銅溶液中
C. 為增強治療缺鐵性貧血效寒,可在口服硫酸亞鐵片時同服維生素![]() D. 為使水果保鮮,可在水果箱內放入高錳酸鉀溶液?浸泡過的硅藻土
D. 為使水果保鮮,可在水果箱內放入高錳酸鉀溶液?浸泡過的硅藻土
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com