
分析 (1)在陽離子中,質量數=質子數+中子數;核電荷數=質子數=核外電子數+所帶電荷數;
(2)根據元素的種類由質子數決定分析,根據質子數、中子數和核數、同位素的概念判斷,同位素最外層電子數相同;
(3)距離原子核越遠,能層能量越高能量越高,Mg原子核外電子排到M層.
解答 解:(1)因2311Na+的質子數為11,質量數為23,中子數=質量數-質子數=23-11=12,核外電子數=質子數-所帶電荷數=11-1=10,故答案為:11;12;10;
(2)元素就是具有相同的核電荷數(即核內質子數)的一類原子的總稱,不同種元素最本質的區別是質子數不同,元素的種類由質子數決定,11H、12H、13H的質子數都是1,所以3種不同粒子${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H表示同一種元素氫元素;
核素是指具有一定數目質子和一定數目中子的一種原子;11H、12H、13H的質子數都是1,中子數分別為0、1、2,屬于三種核數;
具有相同質子數,不同中子數同一元素的不同核素互為同位素;11H、12H、13H的質子數都是1,中子數分別為0、1、2,屬于同位素;
同位素最外層電子數相同,化學性質相同,故答案為:1;3;同位素;相同;
(3)2412Mg的電子數為12,核外電子排布為1s22s22p63s2,距離原子核越遠,能層能量越高,因此能量最高的為M層,故答案為:M.
點評 本題考查原子的表示式、核素、同位素、質量數A=質子數Z+中子數N的計算和核外電子排布規律,解答此類題,除了解核組成符號外,還要記住兩個關系:A═Z+N,質子數═核外電子數═原子序數═質量數-中子數.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③⑤ | B. | ①③⑤ | C. | ①④⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | υD=0.4mol/(L•s) | B. | υC=0.5mol/(L•s) | C. | υB=0.6mol/(L•s) | D. | υA=0.22mol/(L•s) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
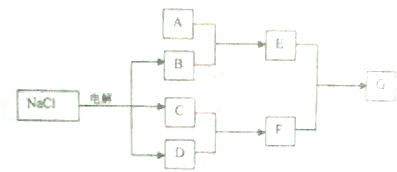
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

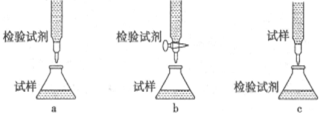
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com