
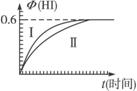
(1)達平衡時,I2(g)的物質的量濃度為______________mol·L-1。
(2)若改變反應條件,在某條件下Φ(HI)的變化如曲線(Ⅰ)所示,則該條件可能是_________________(填入下列條件的序號)。
①恒容條件下,升高溫度
②恒容條件下,降低溫度
③恒溫條件下,縮小反應容器體積
④恒溫條件下,擴大反應容器體積
⑤恒溫、恒容條件下,加入適當催化劑
(3)若保持溫度不變,在另一相同的2 L密閉容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),發生反應達平衡時,HI的體積分數仍為0.60,則a、b、c的關系為______________(用一個含a、b、c的代數式表示)。
(4)室溫時將0.01 mol HI氣體溶于水配成100 ml 溶液,則該溶液中由水電離產生的氫離子的物質的量濃度為____________mol·L-1;若降低溫度該溶液的pH將____________(填增大、減小或不變)。
(1)0.05 (2)③⑤ (3)2b-4a=c (4)1×10-13 不變
解析:(1)平衡時,HI的體積分數為0.60,而平衡前后的總體積不變,即為3 mol,n(HI)=0.6×3 mol=1.8 mol,通過三段式計算:
I2(g)+H2(g)![]() 2HI(g)
2HI(g)
起始:1 2 0
轉化:0.9 0.9 1.8
平衡:0.1 1.1 1.8
達平衡時,I2(g)的物質的量濃度為![]() mol·L-1=0.05 mol·L-1;
mol·L-1=0.05 mol·L-1;
(2)從圖中可知,平衡狀態沒有改變,只是反應速率增大,改變溫度時平衡狀態一定改變,①和②不行,該反應的氣體的計量數不變,所以增大壓強,反應速率增大,平衡不移動,此外加入催化劑也符合題意;(3)因為氣體的計量數不變,所以是等溫等壓條件下的等效平衡問題。利用極限轉化思想,將HI的量轉化,得到(a+2/c)∶(b+2/c)=1∶2,得2b-4a=c;(4)將0.01 mol HI氣體溶于水配成100 mL溶液,此時c(H+)=0.1 mol·L-1,則由水電離出的氫離子的物質的量濃度為![]() mol·L-1=1×10-13 mol·L-1,降低溫度時,KW減小,但是氫離子的物質的量濃度仍然為0.1 mol·L-1,pH將不變。
mol·L-1=1×10-13 mol·L-1,降低溫度時,KW減小,但是氫離子的物質的量濃度仍然為0.1 mol·L-1,pH將不變。


科目:高中化學 來源: 題型:
將1 mol I2(g)和2 mol H2置于某![]() 2HI(g)ΔH<0,并達到平衡。HI的體積分數w(HI)隨時間t變化如圖曲線(Ⅰ)所示。
2HI(g)ΔH<0,并達到平衡。HI的體積分數w(HI)隨時間t變化如圖曲線(Ⅰ)所示。

(1)達到平衡時,I2(g)的物質的量濃度為______________mol·L-1。
(2)若改變反應條件,在甲條件下w(HI)的變化如圖曲線(Ⅱ)所示,在乙條件下w(HI)的變化如圖曲線(Ⅲ)所示。則甲條件可能是______________,乙條件可能是______________。(填入下列條件的序號)
①恒容條件下,升高溫度 ②恒容條件下,降低溫度 ③恒溫條件下,縮小反應容器體積 ④恒溫條件下,擴大反應容器體積 ⑤恒溫恒容條件下,加入適當催化劑
(3)若保持溫度不變,在另一相同的
查看答案和解析>>
科目:高中化學 來源: 題型:
I2(g)+H2(g) ![]() 2HI(g);ΔH<0,并達到平衡。HI的體積分數φ(HI)隨時間變化如下圖中曲線(Ⅱ)所示:
2HI(g);ΔH<0,并達到平衡。HI的體積分數φ(HI)隨時間變化如下圖中曲線(Ⅱ)所示:

(1)達平衡時,I2(g)的物質的量濃度為_______ mol·L -1。
(2)若改變反應條件,在某條件下φ(HI)的變化如曲線(Ⅰ)所示,則該條件可能是______(填下列條件的序號)。?
①恒容條件下,升高溫度?
②恒容條件下,降低溫度?
③恒溫條件下,縮小反應容器體積?
④恒溫條件下,擴大反應容器體積?
⑤恒溫、恒容條件下,加入適當催化劑?
(3)若保持溫度不變,在另一相同的2 L密閉容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),發生反應,達平衡時,HI的體積分數仍為0.60,則a、b、c應滿足的關系為_______(用一個含a、b、c的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
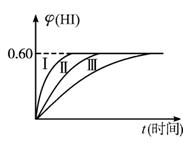
圖1-2-9
(1)達到平衡時,I2(g)的物質的量濃度為___________mol·L-1。
(2)若改變反應條件,在甲條件下φ(HI)的變化如圖中曲線(Ⅰ)所示,在乙條件下φ(HI)的變化如圖中曲線(Ⅲ)所示,則甲條件可能是___________,乙條件可能是___________ (填入下列條件的序號)。
①恒容條件下,升高溫度
②恒容條件下降低溫度
③恒溫條件下,縮小反應容器的體積
④恒溫條件下,擴大反應容器的體積
⑤恒溫、恒容條件下,加入適當催化劑
(3)若保持溫度不變,在另一相同的2 L密閉容器中加a mol I2(g),b mol H2和c mol HI(a,b,c均大于0),發生反應達到平衡時,HI的體積分數仍為0.60,則a,b,c的關系是___________。
查看答案和解析>>
科目:高中化學 來源:2012年滬科版高中化學6.1提示化學反應速率和平衡之謎練習卷(解析版) 題型:填空題
將1 mol I2(g) 和2 mol H2置于2L密閉容器中,在一定溫度下發生反應:
I2(g) + H2(g) 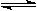 2HI(g);△H<0,并達平衡。HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示
2HI(g);△H<0,并達平衡。HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示
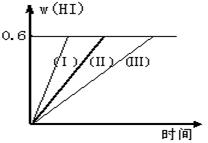
(1)達平衡時,I2(g)的物質的量濃度為 寫出該反應的平衡常數表達式 _____________________________________。
(2)若改變反應條件,在甲條件下w(HI)的變化如曲線(Ⅰ) 所示,在乙條件下w(HI)的變化如曲線(Ⅲ) 所示。則甲條件可能是 ,則乙條件可能是 。
(填入下列條件的序號)
①恒容條件下,升高溫度; ②恒容條件下,降低溫度;③恒溫條件下,縮小反應容器體積; ④恒溫條件下,擴大反應容器體積; ⑤恒溫恒容條件下,加入適當催化劑。
查看答案和解析>>
科目:高中化學 來源:2012屆云南省高二下學期期中考試化學試卷 題型:填空題
(12分)將1 mol I2(g) 和2 mol H2置于2L密閉容器中,在一定溫度下發生反應: H2(g) + I2(g)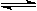 2HI(g);△H<0,并達平衡。HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:
2HI(g);△H<0,并達平衡。HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:

(1)達平衡時,I2(g)的物質的量濃度為 。
(2)若改變反應條件,在甲條件下w(HI)的變化如曲線(Ⅰ) 所示,在乙條件下w(HI)的變化如曲線(Ⅲ) 所示。則甲條件可能是 ,則乙條件可能是 。
(填入下列條件的序號)[來源:學#科#網Z#X#X#K]
①恒容條件下,升高溫度;②恒容條件下,降低溫度;③恒溫條件下,縮小反應容器體積;④恒溫條件下,擴大反應容器體積;⑤恒溫恒容條件下,加入適當催化劑。
(3)若保持溫度不變,在另一個相同的2L密閉容器中加入a mol I2(g)、b mol H2(g)和c mol HI(a、b、c均大于0),發生反應,達平衡時,HI的體積分數仍為0.6,則a、b、c的關系是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com