
【題目】金屬元素Fe、Ni、Pt均為周期表中同族元素,該族元素的化合物在研究和生產中有許多重要用途。
(1)Fe是常見的金屬,生活中用途廣泛。請回答下列問題:
①Fe在元素周期表中的位置為________________________。
②Fe的一種晶胞結構如圖所示,測得晶胞邊長為 a pm,則Fe原子半徑為__________。
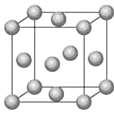
③已知:FeO晶體晶胞結構為NaCl型,與O2-距離最近且等距離的亞鐵離子圍成的空間構型為________。
(2)鉑可與不同的配體形成多種配合物,分子式為[Pt(NH3)2Cl4]的配合物的配體是_________;該配合物有兩種不同的顏色,其中橙黃色比較不穩定,在水中的溶解度大;呈亮黃色的物質在水中的溶解度小,如下圖所示的結構示意圖中呈亮黃色的是_____(填“A”或“B”),理由是___________。
A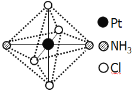 B
B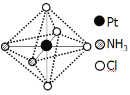
(3)金屬鎳與鑭(La)形成的合金是一種良好的儲氫材料,其晶胞結構示意圖如圖。
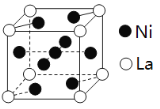
①測知鑭鎳合金晶胞體積為9.0×10-23cm3,則鑭鎳合金的晶體密度為____________ (不必計算結果) 。
②儲氫原理為:鑭鎳合金吸附H2,H2解離為原子,H原子儲存在其中形成化合物。若儲氫后,氫原子占據晶胞中上下底面的棱和面心,則形成的儲氫化合物的化學式為____________。
(4)已知:多原子分子中,若原子都在同一平面上且這些原子有相互平行的p軌道,則p電子可在多個原子間運動,形成“離域π鍵”(或大π鍵)。大π鍵可用![]() 表示,其中m、n分別代表參與形成大π鍵的電子數和原子個數,如苯分子中大π鍵表示為
表示,其中m、n分別代表參與形成大π鍵的電子數和原子個數,如苯分子中大π鍵表示為![]() 。 下列微粒中存在“離域Π鍵”的是__________。
。 下列微粒中存在“離域Π鍵”的是__________。
a.O3 b.SO42- c.H2S d.NO3-
【答案】第4周期第Ⅷ族 ![]() pm 正八面體形 NH3、Cl- A B和水均為極性分子,相似相溶,A為非極性分子在水中的溶解度小
pm 正八面體形 NH3、Cl- A B和水均為極性分子,相似相溶,A為非極性分子在水中的溶解度小 ![]() gcm-3 LaNi5H3 ad
gcm-3 LaNi5H3 ad
【解析】
(1)①鐵是26號元素,據此判斷在周期表中的位置;②根據晶胞結構知,面對角線為鐵原子半徑的4倍,據此計算鐵原子半徑;③FeO晶體晶胞結構為NaCl型,與O2-距離最近且等距離的亞鐵離子為六個面的面心上的離子,據此判斷;
(2)關鍵圖示判斷Pt(NH3)2Cl4的配合物的配體;根據相似相溶原理分析判斷;
(3)①根據晶胞結構圖,利用均攤法計算La和Ni的個數,結合密度=![]() 計算;②根據氫原子占據晶胞中上下底面的棱和面心,計算利用均攤法H的個數,結合①判斷化學式;
計算;②根據氫原子占據晶胞中上下底面的棱和面心,計算利用均攤法H的個數,結合①判斷化學式;
(4)根據形成離域π鍵的形成條件是“原子都在同一平面上且這些原子有相互平行的p軌道”的條件分析判斷。
(1)①鐵是26號元素,位于第四周期第VIII族,故答案為:第四周期第VIII族;
②根據晶胞結構知,面對角線為鐵原子半徑的4倍,面對角線長度=![]() a pm,則Fe原子半徑=
a pm,則Fe原子半徑=![]() pm=
pm=![]() pm,故答案為:
pm,故答案為:![]() pm;
pm;
③FeO晶體晶胞結構為NaCl型,與O2-距離最近且等距離的亞鐵離子為六個面的面心上的離子,與O2-等距離且最近的Fe2+圍成的空間構型為正八面體,故答案為:正八面體;
(2)根據結構圖,[Pt(NH3)2Cl4]的配體為NH3和Cl-;橙黃色在水中的溶解度較大,水為極性分子,根據相似相溶,橙黃色也為極性分子,A為對稱結構,屬于非極性分子,B為非對稱結構,屬于極性分子,則橙黃色的配合物為B;亮黃色的為A,故答案為:NH3、Cl-;A;B和水均為極性分子,相似相溶,A為非極性分子在水中的溶解度小;
(3)①根據晶胞結構圖,La的個數為8×![]() =1,Ni的個數為8×
=1,Ni的個數為8×![]() +1=5,晶胞的質量為
+1=5,晶胞的質量為![]() g,密度=
g,密度=![]() =
= gcm-3=
gcm-3=![]() gcm-3,故答案為:
gcm-3,故答案為:![]() gcm-3;
gcm-3;
②根據晶胞結構圖,La的個數為8×![]() =1,Ni的個數為8×
=1,Ni的個數為8×![]() +1=5,氫原子占據晶胞中上下底面的棱和面心,則H的個數為8×
+1=5,氫原子占據晶胞中上下底面的棱和面心,則H的個數為8×![]() +2×
+2×![]() =3,其化學式為LaNi5H3,故答案為:LaNi5H3;
=3,其化學式為LaNi5H3,故答案為:LaNi5H3;
(4)形成離域π鍵的形成條件是“原子都在同一平面上且這些原子有相互平行的p軌道” ,O3為V形結構,有相互平行的p軌道,可以形成離域π鍵;硫酸根離子是正四面體結構,原子不處于同一平面內,不能形成離域π鍵;硫化氫中H原子和S原子沒有平行的p軌道,不能形成離域π鍵;NO3-為平面三角形,有相互平行的p軌道,可以形成離域π鍵,故答案為:ad。


 學練快車道口算心算速算天天練系列答案
學練快車道口算心算速算天天練系列答案科目:高中化學 來源: 題型:
【題目】下列說法中正確的是
A. NO2、BF3、NCl3分子中沒有一個分子中原子的最外層電子都滿足了8電子穩定結構
B. P4和CH4都是正四面體形分子且鍵角都為109°28′
C. NH4+的電子式為 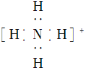 ,離子呈平面正方形結構
,離子呈平面正方形結構
D. NH3分子中有一對未成鍵的孤電子對,它對成鍵電子的排斥作用較強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組同學設計實驗,探究中和反應的發生。
(實驗過程)
編號 | 實驗操作 |
實驗I | 向滴有酚酞的氫氧化鈉溶液中滴加稀鹽酸,觀察現象
|
實驗II | 按如圖進行實驗,對比①、②中的實驗現象
|
(分析與解釋)
(1)中和反應的實質是______(用離子方程式表示)。
(2)實驗I中,中和反應發生的現象是______。
(3)實驗II中,能判斷中和反應發生的依據是______。
a.反應結束消耗鎂條的量②>①
b.鎂條表面產生氣泡的速率①>②
(4)實驗II中,如果提供溫度計、氣球(收集氣體)等輔助儀器,還能獲取證明中和反應發生的實驗證據是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖中是部分短周期元素化合價與原子序數的關系圖,下列說法正確的是( )
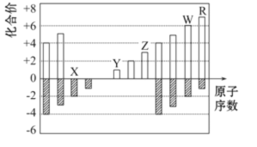
A.原子半徑:Z>Y>X
B.氣態氫化物穩定性:R<W
C.WX3和水反應生成的化合物是離子化合物
D.Y和Z兩者最高價氧化物對應的水化物能相互反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉晶體(Na2S2O3·5H2O)又稱海波,呈無色透明狀,易溶于水,不溶于乙醇,常用作棉織物漂白后的脫氯劑、定量分析中的還原劑。
Ⅰ. Na2S2O3·5H2O的制備
Na2S2O3·5H2O的制備方法有多種,其中亞硫酸鈉法是工業和實驗室中的主要方法:Na2SO3 + S + 5H2O ![]() Na2S2O3·5H2O
Na2S2O3·5H2O
制備過程如下:
①稱取12.6g Na2SO3于100mL燒杯中,加50 mL去離子水攪拌溶解。
②另取4.0 g硫粉于200mL燒杯中,加6 mL乙醇充分攪拌均勻將其潤濕,再加入Na2SO3溶液,隔石棉小火加熱煮沸,不斷攪拌至硫粉幾乎全部反應。
③停止加熱,待溶液稍冷卻后加2 g活性炭,加熱煮沸2分鐘(脫色)。
④趁熱過濾,得濾液至蒸發皿中, ______________、____________________。
⑤過濾、洗滌,用濾紙吸干后,稱重,計算產率。
(1)加入的硫粉用乙醇潤濕的目的是____________________________。
(2)步驟④趁熱過濾的原因_____________________,空格處應采取的操作是_________________、____________________。
(3)步驟⑤洗滌過程中,為防止有部分產品損失,應選用的試劑為___________。
(4)濾液中除Na2S2O3和未反應完全的Na2SO3外,最可能存在的無機雜質是________________,生成該雜質的原因可能是____________________________。
Ⅱ.產品純度的測定
準確稱取1.00 g產品(硫代硫酸鈉晶體的摩爾質量為248 g/mol),用適量蒸餾水溶解,以淀粉作指示劑,用0.1000 mol/L碘標準溶液滴定至終點,消耗21.00 mL。反應的離子方程式為:2S2O32-+I2=S4O62-+2I-。
(5)計算所得產品的純度為___________(保留三位有效數字),該數據的合理解釋可能是__________(不考慮實驗操作引起的誤差)。
Ⅲ.產品的應用
(6)Na2S2O3常用于脫氯劑,在溶液中易被Cl2氧化為SO42-,該反應的離子方程式為 ____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】全釩氧化還原電池是一種新型可充電電池,不同價態的含釩離子作為正極和負極的活性物質,分別儲存在各自的酸性電解液儲罐中。其結構原理如圖所示,該電池放電時,右槽中的電極反應為:V2+- e-=V3+,下列說法正確的是( )

A.放電時,右槽發生還原反應
B.放電時,左槽的電極反應式:VO2++2H++e-=VO2++H2O
C.充電時,每轉移1mol電子,1 mol H+從右槽遷移向左槽
D.充電時,陰極電解液pH升高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學工程師為了變廢為寶,從某工業廢液(含有大量CuCl2、FeCl2和FeCl3,任意排放將導致環境污染及資源的浪費)中回收銅,并將鐵的化合物全部轉化為化工原料FeCl3晶體,主要流程如下:
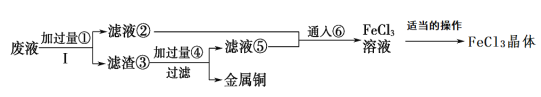
(1)步驟Ⅰ的操作名稱:__________;
(2)檢驗濾液中②是否含有Fe3+所需試劑化學式:_____________,
(3)向②中加入NaOH溶液并長時間暴露在空氣中,此過程的現象:________。
(4)濾渣③加入過量的④發生的離子方程式____________,
(5)通入⑥的目的:_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣(含CO、SO2、NO等)是城市空氣的污染源之一,治理方法之一是在汽車的排氣管上裝一個“催化轉化器”(用鉑、鈀合金作催化劑),它能使一氧化碳跟一氧化氮反應生成可參與大氣循環的無毒氣體。
(1)汽車尾氣中導致酸雨形成的主要物質是________(填化學式)。
(2)在汽車排氣管上加裝“催化轉化器”,可使CO和NO反應產生可參與大氣循環的無毒氣體,請寫出該反應的化學方程式:__________。該反應的還原劑為:______氮元素的化合價_______(填“升高”或“降低”)。
(3)請寫出汽車尾氣形成硝酸型酸雨的主要反應的化學方程式:__________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在某密閉容器中發生反應:2HI(g)H2(g)+I2(g),若 15 s 內 c(HI)由 0.1 mol·L-1 降到 0.07 mol·L-1,則下列說法正確的是
A.0~15 s 內用 I2 表示的平均反應速率為 v(I2)=0.015 mol·L-1·s-1
B.c(HI)由 0.07 mol ·L-1 降到 0.05 mol·L-1 所需的反應時間小于 10 s
C.升高溫度,正反應速率加快,逆反應速率減慢
D.減小容器的體積,反應速率加快
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com