
【題目】用NA表示阿伏加德羅常數的值。下列敘述正確的是( )
A. 常溫常壓下,11.2L二氧化硫所含的氧原子數等于NA
B. 0.5molH2O所含的電子數為9NA
C. 8.0gCu2S和CuO的混合物中含有銅原子數為0.1NA
D. 300mL2mol·L-1蔗糖溶液中所含分子數為0.6NA
科目:高中化學 來源: 題型:
【題目】氮的固定對工農業及人類生存具有重大意義。
合成氨是最重要的人工固氮:N2(g)+3H2(g) ![]() 2NH3(g) △H<0。
2NH3(g) △H<0。
(1)下列關于該反應的說法中,正確的是___________(填正確選項字母編號)。
A.反應達到平衡狀態時,N2、H2、NH3的體積比為1∶3∶2
B.加催化劑可以加快正反應速率,減慢逆反應速率
C.高溫既有利于加快反應速率也有利于提高氨氣的產率
D.高壓既有利于加快反應速率也有利于提高氨氣的產率
(2)一定溫度下,在容積為1L的密閉容器中,加入lmolN2和3mol H2,反應達到平衡時H2的轉化率為60%,此時反應消耗N2物質的量為___________mol;保持容器體積不變,再向容器中加入1molN2,3mol H2,反應再次達到平衡時,氫氣的轉化率將___________(填“增大”或“減小”或“不變”)。
(3)標準狀況下,將22.4 mL的氨氣通入100 mL 0.01 mol·L-1的鹽酸中,充分反應后,溶液中各離子濃度由大到小的順序是________________________。
(4)將氨氣通入盛有CaSO4懸濁液的沉淀池中,再通入適量的CO2氣體,充分反應后,過濾所得濾液為(NH4)2SO4溶液,該過程的化學反應方程式為____________________。
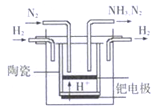
(5)20世紀末,科學家采用高質子導電性的SCY陶瓷(能傳遞 H+)為介質,用吸附在它內外表面上的金屬鈀多晶薄膜做電極,實現常壓、570℃高溫的電解法合成氨,提高了反應物的轉化率,其實驗簡圖如圖所示,寫出陰極的電極反應式____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,有下列四種溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。下列有關說法正確的是
A.四種溶液的KW相同,由水電離的c(H+):①=③>②=④
B.向等體積的四種溶液中分別加入100 mL水后,溶液的pH:③>④>②>①
C.①、②、④溶液分別與足量鋁粉反應,生成H2的量:①最大
D.將②、③兩種溶液混合后,若pH=7,消耗溶液的體積為:③>②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A的結構簡式為![]() ,它可通過不間化學反應分別制得B、C、D和E四種物質。
,它可通過不間化學反應分別制得B、C、D和E四種物質。

回答下列問題:
(1)A中含有官能團的名稱是_____________。 A生成B的反應類型為______________。
(2)在AE五種物質中,互為同分異構體的是(填標號)_____________。
(3)關于B的性質,下列說法正確的是________________(填標號)
a.1 mol B最多可與5mol H2發生加成反應
b.能與新制Cu(OH)2反應生成紅色沉淀
c.在催化劑作用下,可被空氣中的氧氣氧化
d.該分子中所有的原子在同一平面上
(4) C能形成高聚物,該高聚物的結構簡式為_____________。
(5)寫出下列反應的化學力程式(需注明反應條件)。
①A生成C:_________________。
②D與NaOH溶液共熱:__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列屬于固氮反應的是( )
A. 2NO+O2→2NO2 B. 3NO2+H2O→2HNO3+NO
C. NH3+HCl→NH4Cl D. N2+3Mg→Mg3N2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗是研究化學的基礎。化學實驗的基本操作、氣體的制備、離子的檢驗、物質性質的探究等內容是化學實驗中的重要內容。請回答下列問題:
(1)下列實驗操作的裝置正確的是____(填標號)。指出不正確裝置中的一處錯誤____。

A B C D
(2)實驗室常用濃鹽酸制取Cl2,制取時,需要加入具有___________性的物質(填:氧化性、還原性、酸性、堿性)。若制取氯氣反應為6HCl(濃)+KClO3=3Cl2↑+KCl+3H2O,該反應中的還原產物為____;還原產物與氧化產物的物質的量之比為_____。
(3)氯氣溶于水可制得氯水,氯水的成份比較復雜。
①取新制的氯水加入硝酸酸化的AgNO3溶液出現白色沉淀,證明有Cl-存在,反應的離子方程式為________。
②取新制的氯水加入試劑______,現象為___________,證明溶液中含有H+;
③取新制的氯水,加入幾滴紫色的石蕊試液,溶液先變紅后褪色,原因是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】70年代開始發現氯氣應用水消毒會產生具有致癌作用的鹵代甲烷類化合物。氧化氯(ClO2)是目前國際上公認的第四代高效、無毒的廣泛消毒劑,是一種黃綠色的氣體,易溶于水。我國從2000年起已逐步用消毒劑ClO2代替氯氣對飲用水進行消毒。
(1)ClO2消毒水時,可將Fe2+、Mn2+轉化成Fe(OH)3、MnO2難溶物除去,用ClO2處理過的飲用水(pH為5.5~6.5)常含有一定量對人體不利的亞氯酸根離子ClO2-。2001年我國衛生部規定,飲用水的ClO-2含量應不超過0.2mg/L。若飲用水中ClO2-的含量超標,可向其中加入適量的某還原劑,該反應的氧化產物是_____________(填化學式)。
ClO2在殺菌消毒的同時,可將劇毒氰化物中碳、氮元素氧化成無毒氣體而除去,寫出用ClO2氧化除去NaCN的化學方程式___________________________________。
(2)①工業上制備ClO2,可以通過NaClO3在H2SO4存在的條件下與Na2SO3反應制得。
請寫出該反應的離子方程式:_________________________________________。
②實驗室制備ClO2,可以用NH4Cl、鹽酸、NaClO2(亞氯酸鈉)為原料在一定條件下制得,只是制得的ClO2中混有NH3除去ClO2中的NH3可選用的試劑是____;(填序號)
A.濃硫酸 B.飽和食鹽水
C.堿石灰 D.水
(3)測定ClO2(如圖)的過程如下:在錐形瓶中加入足量的碘化鉀,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;將生成的ClO2氣體通過導管在錐形瓶中被吸收;將玻璃封管中的水封液倒入錐形瓶中,加入幾滴淀粉溶液,用cmol/L硫代硫酸鈉標準溶液滴定(I2+2S2O32-===2I—+S4O62—),共用去V ml硫代硫酸鈉溶液。

①裝置中玻璃液封管的作用是__________________;
②滴定終點的現象是:_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[2016·浙江節選]催化還原CO2是解決溫室效應及能源問題的重要手段之一。研究表明,在Cu/ZnO催化劑存在下,CO2和H2可發生兩個平行反應,分別生成CH3OH和CO。反應的熱化學方程式如下:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH1=53.7 kJ·mol1 I
CH3OH(g)+H2O(g)ΔH1=53.7 kJ·mol1 I
CO2(g)+ H2(g)![]() CO(g)+H2O(g) ΔH2 II
CO(g)+H2O(g) ΔH2 II
某實驗室控制CO2和H2初始投料比為1:2.2,在相同壓強下,經過相同反應時間測得如下實驗數據:

【備注】Cat.1:Cu/ZnO納米棒;Cat.2:Cu/ZnO納米片;甲醇選擇性:轉化的CO2中生成甲醇的百分比
已知:①CO和H2的標準燃燒熱分別為283.0 kJ·mol1和285.8 kJ·mol1
②H2O(l)![]() H2O(g) ΔH3=44.0 kJ·mol1
H2O(g) ΔH3=44.0 kJ·mol1
請回答(不考慮溫度對ΔH的影響):
(1)反應I的平衡常數表達式K= ;反應II的ΔH2= kJ·mol1。
(2)有利于提高CO2轉化為CH3OH平衡轉化率的措施有 。
A.使用催化劑Cat.1
B.使用催化劑Cat.2
C.降低反應溫度
D.投料比不變,增加反應物的濃度
E.增大CO2和H2的初始投料比
(3)表中實驗數據表明,在相同溫度下不同的催化劑對CO2轉化成CH3OH的選擇性有顯著的影響,其原因是 。
(4)在圖中分別畫出反應I在無催化劑、有Cat.1和有Cat.2三種情況下“反應過程~能量”示意圖。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com