隨著人類對溫室效應和資源短缺等問題的重視,如何降低大氣中CO
2的含量及有效地開發利用CO
2,引起了各國的普遍重視.目前工業上有一種方法是用CO
2來生產燃料甲醇.一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu
2O/ZnO):
CO(g)+2H
2(g)
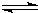
CH
3OH(g)
根據題意完成下列各題:反應達到平衡時,
(1)平衡常數表達式K=
,升高溫度,K值
減小
減小
(填“增大”、“減小”或“不變”).
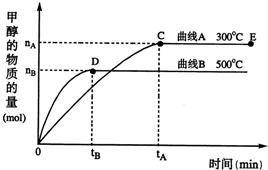
(2)在500℃,從反應開始到平衡,氫氣的平均反應速率v(H
2)=
(用 n
B t
B 表示)
(3)在其他條件不變的情況下,對處于E點的體系體積壓縮到原來的
,下列有關該體系的說法正確的是
bc
bc
a.氫氣的濃度減少
b.正反應速率加快,逆反應速率也加快
c.甲醇的物質的量增加
d.重新平衡時
增大
(4)據研究,反應過程中起催化作用的為Cu
2O,反應體系中含少量CO
2有利于維持催化劑Cu
2O的量不變,原因是:
Cu
2O+CO
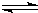
2Cu+CO
2Cu
2O+CO
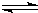
2Cu+CO
2(用化學方程式表示).
(5)使用燃料電池是節能減排的重要手段之一.CO和H
2(俗稱水煤氣)燃料電池就是其中的一種,該電池的兩極分別通入燃料氣(水煤氣)和氧氣.電解質是摻雜了Y
2O
3的ZrO
2晶體,它在高溫下能傳導O
2-.水煤氣在一定條件下可以合成二甲醚,同時還產生一種可以參與大氣循環的無機化合物,3CO+3H
2=CH
3OCH
3+CO
2 或 2CO+4H
2=CH
3OCH
3+H
2O.上述水煤氣燃料電池的負極反應方程式:(寫1個)
CO+O2--2e-=CO2 H2+O2--2e-=2H2O
CO+O2--2e-=CO2 H2+O2--2e-=2H2O
.
(6)如圖是丙烷、二甲醚燃燒過程中能量變化圖,其中x為各自反應中對應的系數.根據該圖寫出二甲醚燃燒的熱化學方程式:
CH
3OCH
3(g)+3O
2(g)
2CO
2(g)+3H
2O(l)△H=-1455kJ?mol
-1CH
3OCH
3(g)+3O
2(g)
2CO
2(g)+3H
2O(l)△H=-1455kJ?mol
-1



 課課練江蘇系列答案
課課練江蘇系列答案 名牌中學課時作業系列答案
名牌中學課時作業系列答案 明天教育課時特訓系列答案
明天教育課時特訓系列答案 浙江新課程三維目標測評課時特訓系列答案
浙江新課程三維目標測評課時特訓系列答案 9、一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g)
9、一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)
CH3OH(g) 2Cu+CO2
2Cu+CO2 2Cu+CO2
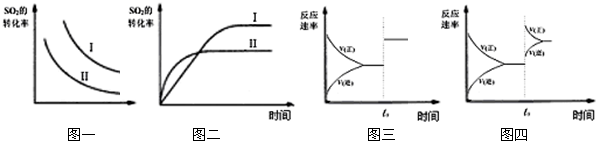
2Cu+CO2 (4)反應過程中CO(g)、H2(g)、CH3OH(g)物質的量變化如圖所示,分別用A、B、C表示CO、H2、CH3OH,根據圖中所示判斷下列說法正確的是
(4)反應過程中CO(g)、H2(g)、CH3OH(g)物質的量變化如圖所示,分別用A、B、C表示CO、H2、CH3OH,根據圖中所示判斷下列說法正確的是 一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g)根據題意完成下列各題:
一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g)根據題意完成下列各題: 隨著人類對溫室效應和資源短缺等問題的重視,如何降低大氣中CO2的含量及有效地開發利用CO2,引起了各國的普遍重視.目前工業上有一種方法是用CO2來生產燃料甲醇.一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):
隨著人類對溫室效應和資源短缺等問題的重視,如何降低大氣中CO2的含量及有效地開發利用CO2,引起了各國的普遍重視.目前工業上有一種方法是用CO2來生產燃料甲醇.一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):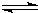 CH3OH(g)
CH3OH(g)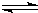 2Cu+CO2
2Cu+CO2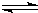 2Cu+CO2
2Cu+CO2
 一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO).根據題意完成下列各題:
一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO).根據題意完成下列各題: