短周期元素A、B、C、D、E、F,原子序數依次增大.已知:①A與E同主族,E的單質與D
2反應可生成E
2D和E
2D
2兩種固體;②F的單質在D
2中燃燒的產物可使品紅溶液褪色;B的單質在D
2中燃燒可生成BD和BD
2兩種氣體;③CA
4++DA
-=CA
3↑+A
2D,各種反應和生成物的電子數都與E
+相等.請回答下列問題:
(1)BD
2的結構式為
O=C=O
O=C=O
,F的離子結構示意圖為
,CA
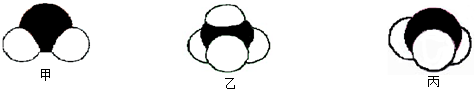
3分子的空間構型為
三角錐型
三角錐型
.
(2)廢舊印刷電路板上含有銅,以往回收的方法是將其灼燒使用銅轉化為氧化銅,再用稀硫酸來溶解.現改用A
2D
2和稀硫酸浸泡即達目的,又保護了環境,其反應的化學方程式為
Cu+H2O2+H2SO4=CuSO4+2H2O
Cu+H2O2+H2SO4=CuSO4+2H2O
;
(3)在火箭推進器中裝有強還原劑C
2A
4和強氧化劑A
2D
2,已知0.5mol液態C
2A
4和足量液態A
2D
2反應,生成一種無色無味無毒的氣體和水蒸氣,放出320kJ熱量,寫出該反應的熱化學方程式
N2H4(1)+2H2O2(1)=N2(g)+4H2O(g);△H=-640kJ?mol-1
N2H4(1)+2H2O2(1)=N2(g)+4H2O(g);△H=-640kJ?mol-1
.
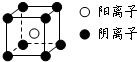
(4)離子化合物CA
5的電子式為
,其晶體的最小結構單元如圖所示經實驗測得CA
5晶體的密度為dg/cm
3,阿伏加德羅常數用N
A表示,則該晶體中陰離子與陽離子之間的最短距離為
cm.

 短周期元素A、B、C、D、E、F,原子序數依次增大.已知:①A與E同主族,E的單質與D2反應可生成E2D和E2D2兩種固體;②F的單質在D2中燃燒的產物可使品紅溶液褪色;B的單質在D2中燃燒可生成BD和BD2兩種氣體;③CA4++DA-=CA3↑+A2D,各種反應和生成物的電子數都與E+相等.請回答下列問題:
短周期元素A、B、C、D、E、F,原子序數依次增大.已知:①A與E同主族,E的單質與D2反應可生成E2D和E2D2兩種固體;②F的單質在D2中燃燒的產物可使品紅溶液褪色;B的單質在D2中燃燒可生成BD和BD2兩種氣體;③CA4++DA-=CA3↑+A2D,各種反應和生成物的電子數都與E+相等.請回答下列問題:



 ,氨氣是三角錐型結構,
,氨氣是三角錐型結構, ;三角錐型;
;三角錐型; ;
; ;
;

 活力課時同步練習冊系列答案
活力課時同步練習冊系列答案