
I.短周期元素X、Y、Z、W在元素周期表中相對位置如圖所示,其中Y所處的周期序數與族序數相等。按要求回答下列問題:
(1)寫出X的原子結構示意圖_______________。
(2)列舉一個事實說明W非金屬性強于Z: _______________(用化學方程式表示)。
(3)含Y的某種鹽常用作凈水劑,其凈水原理是__________(用離子方程式表示)。
II.運用所學化學原理,解決下列問題:
(4)已知:Si+2NaOH+H2O=Na2SiO3+2H2。某同學利用單質硅和鐵為電極材料設計原電池(NaOH為電解質溶液),該原電池負極的電極反應式為_________________。
(5)已知:①C(s)+ O2(g)=CO2(g) 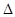 H=a kJ· mol-1;②CO2(g) +C(s)=2CO(g)
H=a kJ· mol-1;②CO2(g) +C(s)=2CO(g) 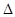 H=b kJ· mol-1;③Si(s)+ O2(g)=SiO2(s)
H=b kJ· mol-1;③Si(s)+ O2(g)=SiO2(s) 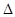 H=c kJ· mol-1。工業上生產粗硅的熱化學方程式為____________。
H=c kJ· mol-1。工業上生產粗硅的熱化學方程式為____________。
(6)已知:CO(g)+H2O(g) H2(g) + CO2(g)。右表為該反應在不同溫度時的平衡常數。則:該反應的
H2(g) + CO2(g)。右表為該反應在不同溫度時的平衡常數。則:該反應的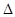 H________0(填“<”或“>”);500℃時進行該反應,且CO和H2O起始濃度相等,CO平衡轉化率為_________。
H________0(填“<”或“>”);500℃時進行該反應,且CO和H2O起始濃度相等,CO平衡轉化率為_________。
(1)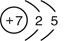 (2分)(2)2HClO4+Na2SiO3=2NaClO4+H2SiO3↓(3分)
(2分)(2)2HClO4+Na2SiO3=2NaClO4+H2SiO3↓(3分)
(3)Al3++3H2O Al(OH)3+3H+(2分)(4)Si-4e-+6OH-=SiO32-+3H2O(3分)
Al(OH)3+3H+(2分)(4)Si-4e-+6OH-=SiO32-+3H2O(3分)
(5)2C(s)+SiO2(s)=Si(s)+2CO(g) △H=(a+b-c)kJ·mol-1(3分) (6)<(1分) 75%(3分)
解析試題分析:根據短周期元素X、Y、Z、W在元素周期表中相對位置可知,X位于第二周期,Y、Z、W位于第三周期。其中Y所處的周期序數與族序數相等,所以Y是第三周期第ⅢA族元素,即Y是鋁,則Z是Si,X是N,W是Cl。
(1)氮元素的原子序數是7,則氮元素的原子結構示意圖為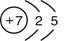 。
。
(2)判斷非金屬性強弱的一般規律是:①由元素原子的氧化性判斷:一般情況下,氧化性越強,對應非金屬性越強。②由單質和酸或者和水的反應程度判斷:反應越劇烈,非金屬性越強。③由對應氫化物的穩定性判斷:氫化物越穩定,非金屬性越強。④由和氫氣化合的難易程度判斷:化合越容易,非金屬性越強。⑤由最高價氧化物對應水化物的酸性來判斷:酸性越強,非金屬越強。(除氟元素之外)。⑥由對應陰離子的還原性判斷:還原性越強,對應非金屬性越弱。⑦由置換反應判斷:強置弱。〔若依據置換反應來說明元素的非金屬性強弱,則非金屬單質應做氧化劑,非金屬單質做還原劑的置換反應不能作為比較非金屬性強弱的依據〕。⑧按元素周期律,同周期元素由左到右,隨核電荷數的增加,非金屬性增強;同主族元素由上到下,隨核電荷數的增加,非金屬性減弱。⑨非金屬單質與具有可變價金屬的反應。能生成高價金屬化合物的,其非金屬性強。因此可以根據高氯酸能制備硅酸來驗證W非金屬性強于Z,反應的化學方程式為2HClO4+Na2SiO3=2NaClO4+H2SiO3↓。
(3)明礬溶于水電離出的鋁離子水解生成氫氧化鋁膠體,膠體具有吸附性,因此明礬可以作凈水劑,反應的離子方程式為Al3++3H2O Al(OH)3+3H+。
Al(OH)3+3H+。
(4)原電池中負極失去電子,發生氧化反應。所以根據反應式Si+2NaOH+H2O=Na2SiO3+2H2可知,如果利用單質硅和鐵為電極材料設計原電池(NaOH為電解質溶液),則硅是負極,因此該原電池負極的電極反應式為Si-4e-+6OH-=SiO32-+3H2O。
(5)已知:①C(s)+ O2(g)=CO2(g) △H=a kJ· mol-1;②CO2(g) +C(s)=2CO(g) △H=b kJ· mol-1;③Si(s)+ O2(g)=SiO2(s) △H=c kJ· mol-1,則根據蓋斯定律可知①+②-③即得到工業上生產粗硅的熱化學方程式,即為2C(s)+SiO2(s)=Si(s)+2CO(g) △H=(a+b-c)kJ·mol-1。
(6)根據表中數據可知,隨著溫度的升高,平衡常數逐漸減小。這說明升高溫度平衡向逆反應方向移動,因此正方應是放熱反應,即△H<0;設CO和H2O起始濃度分別為a,則
CO(g)+H2O(g) H2(g) + CO2(g)
H2(g) + CO2(g)
起始濃度 a a 0 0
轉化濃度 b b b b
平衡濃度 a-b a-b b b
所以根據平衡常數表達式可知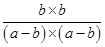 =9
=9
解得b=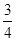 a
a
所以CO平衡轉化率為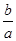 ×100%=75%
×100%=75%
考點:考查元素推斷、非金屬性強弱比較、蓋斯定律應用、原電池應用以及可逆反應的有關判斷與計算


科目:高中化學 來源: 題型:填空題
主族元素W、X、Y、Z的原子序數依次增大,W的原子最外層電子數是次外層電子數的3倍。X、Y和Z分屬不同的周期,它們的原子序數之和是W原子序數的5倍。在由元素W、X、Y、Z組成的所有可能的二組分化合物中,由元素W與Y形成的化合物M的熔點最高。請回答下列問題:
(1)W元素原子的L層軌道表示式為________,W3分子的空間構型為________;
(2)化合物M的晶體結構與NaCl相同,而熔點高于NaCl。M熔點較高的原因是____________________。將一定量的化合物ZX負載在M上可制得ZX/M催化劑,用于催化碳酸二甲酯與月桂醇酯交換合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的雜化方式有________,O—C—O的鍵角約為________;
(3)X、Y、Z可形成立方晶體結構的化合物,其晶胞中X占據所有棱的中心,Y位于頂角,Z處于體心位置,則該晶體的組成為X∶Y∶Z=________;
(4)含有元素Z的鹽的焰色反應為紫色。許多金屬鹽都可以發生焰色反應,其原因是__________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
甲元素的原子序數是19,乙元素原子核外有兩個電子層,最外電子層上有6個電子;丙是元素周期表第ⅠA族中金屬性最弱的堿金屬元素。由此推斷:
(1)甲元素在周期表中位于第________周期;乙元素在周期表中位于第________族;丙元素的名稱為________。
(2)甲的單質與水反應的離子方程式為____________________________;
乙單質與丙單質反應的化學方程式為______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(8分)X、Y、Z是短周期三種元素,它們在周期表中的位置如圖所示。試回答:
| | | X |
| | Y | |
| Z | | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F是原子序數依次增大的同周期元素,已知A、C、F的原子最外層電子數之和為11,且這三種元素的最高價氧化物的水化物之間兩兩皆能反應,均生成鹽和水,D元素原子的次外層電子數比最外層電子數多4個,E元素原子最外層與最內層電子數的差是3,試回答:
(1)寫出下列元素的元素符號:A__________,C________,D__________,E__________。
(2)用電子式表示B和F形成化合物的過程:__________。
(3)寫出A、C、F三種元素最高價氧化物的水化物相互反應的化學方程式__________________,__________________,________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
元素周期表是學習化學的重要工具,它隱含許多信息和規律。下表所列是五種短周期的原子半徑及主要化合價(已知鈹的原子半徑為0.089 nm)。
| 元素代號 | A | B | C | D | E |
| 原子半徑/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合價 | +2 | +3 | +6,-2 | -1 | -2 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
有X、Y、Z、W四種含14個電子的粒子,其結構特點如下:
(1)A原子核外比X原子多3個電子,A的原子結構示意圖是________;含1 mol X的氧化物晶體中含有共價鍵數目為________。
(2)Z與鈣離子組成的化合物的電子式為________________。
(3)14 g Y完全燃燒放出的熱量是141.5 kJ,寫出Y燃燒的熱化學方程式:______________________________。
(4)組成W的元素最高價氧化物對應的水化物甲有下圖所示轉化關系(反應條件和其他物質已略):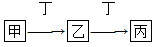
①寫出丁在高溫下與水反應的化學方程式:__________________;
②組成W的元素的簡單氫化物極易溶于水的主要原因是________________________
該氫化物與空氣可以構成一種燃料電池,電解質溶液是KOH,其負極的電極反應式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某銨態氮肥由W、X、Y、Z 4種短周期元素組成,其中W的原子半徑最小。
Ⅰ.若Y、Z同主族,ZY2是形成酸雨的主要物質之一。
(1)將X、Y、Z的元素符號填在如圖所示元素周期表(局部)中的相應位置上。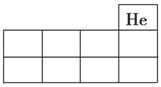
(2)X的最高價氧化物對應水化物的稀溶液與銅反應的化學方程式為 。
(3)一定條件下,1 mol XW3氣體與O2完全反應生成X元素的單質和液態水,放出382.8 kJ熱量。該反應的熱化學方程式為 __。
Ⅱ.若Z是形成化合物種類最多的元素。
(4)該氮肥的名稱是 __(填一種)。
(5)HR是含Z元素的一元酸。室溫時,用0.250 mol·L-1NaOH溶液滴定25.0 mL HR溶液時,溶液的pH變化情況如圖所示。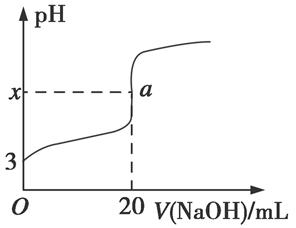
其中,a點表示兩種物質恰好完全反應。
①圖中x (填“>”“<”或“=”)7。
②室溫時,HR的電離常數Ka= (填數值)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
部分中學化學常見元素原子結構及性質如表所示:
| 序號 | 元素 | 結構及性質 |
| ① | A | A單質是生活中常見金屬,它有兩種氯化物,相對分子質量相差35.5 |
| ② | B | B原子最外層電子數是內層電子總數的 |
| ③ | C | C是常見化肥的主要元素,單質常溫下呈氣態 |
| ④ | D | D單質被譽為“信息革命的催化劑”,是常用的半導體材料 |
| ⑤ | E | 通常情況下,E沒有正化合價,A、B、C、D、F都能與E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com