
【題目】【加試題】鐵在工業和生活中都具有非常重要的應用。某含鐵化合物W,為探究其成分,化學興趣小組的同學取化合物W粉末進行試驗。經組成分析,該粉末除Fe外還有O和另一未知元素共三種元素。另取2.22g化合物W的粉末溶于適量稀硫酸,向反應后的溶液中加入含有3.20gNaOH的溶液,恰好完全反應。過濾,將洗滌后的沉淀充分灼燒,得到紅棕色粉末1.60g;將所得濾液在一定條件下蒸發灼燒可得到一種純凈的不含結晶水的鹽7.10g。請回答:
(1)則另一未知元素為________(填化學式)。
(2)①該化合物W的化學式為________________。
②該化合物W與適量稀硫酸反應的化學方程式___________________。
(3)草酸鈷是廣泛應用于磁性材料、電池材料、及超硬材料等領域。某研究小組在實驗室探究CoC2O4分解反應的平衡常數。將一定量純凈的CoC2O4粉末置于特制的密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解的平衡:
CoC2O4(S)![]() CoO(S)+CO(g)+CO2(g)
CoO(S)+CO(g)+CO2(g)
實驗測得不同溫度下的平衡數據列于下表:
溫度/℃ | 240 | 250 | 260 | 270 |
平衡總壓強/kp | 5.7 | 8.3 | 12.0 | 17.1 |
平衡總濃度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 |
由表中數據,列式計算250℃時CoC2O4分解平衡常數 。 該反應的焓變△H 0(填“>”、“=”或“<”)。
(4)溫度加熱至350℃,CO2的體積分數開始發生變化,體積分數和溫度的關系如下:試畫出CO的體積分數隨溫度升高的曲線
【答案】(1)Na (2)NaFeO2 ;2NaFeO2+4H2SO4=Na2SO4+Fe2(SO4)3+4H2O
(3) 2.89×10—6 > (4)見右圖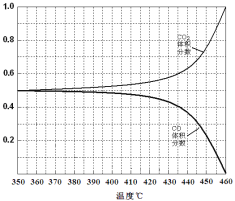
【解析】
試題分析:另取2.22g化合物W的粉末溶于適量稀硫酸,向反應后的溶液中加入含有3.20gNaOH的溶液,恰好完全反應。過濾,將洗滌后的沉淀充分灼燒,得到紅棕色粉末1.60g,這說明氧化鐵是1.60g,物質的量是0.01mol;將所得濾液在一定條件下蒸發灼燒可得到一種純凈的不含結晶水的鹽7.10g,由于加入氫氧化鈉,這說明原化合物中含有鈉元素,因此7.10g物質是硫酸鈉,物質的量是7.10g÷142g/mol=0.05mol。加入的氫氧化鈉是3.20g÷40g/mol=0.08mol,因此原化合物中鈉離子的物質的量是0.05mol×2-0.08mol=0.02mol。氧元素的物質的量是
![]() =0.04mol。
=0.04mol。
(1)根據以上分析可知則另一未知元素為Na。
(2)①該化合物W中Na、O、Fe的原子個數之比為0.02:0.04:0.02=1:2:1,其化學式為NaFeO2。
②該化合物W與適量稀硫酸反應的化學方程式為2NaFeO2+4H2SO4=Na2SO4+Fe2(SO4)3+4H2O。
(3)根據方程式可知生成物CO和二氧化碳的物質的量相等,則250℃時二者的濃度均是3.4×10-3mol/L÷2=1.7×10-3mol/L,所以該溫度下的平衡常數K=c(C0)·c(CO2)=2.89×10—6;根據表中數據可知升高溫度壓強增大,說明升高溫度平衡向正反應方向進行,因此正反應是吸熱反應,則△H<;
(4)350℃以后二氧化碳的體積分數升高,這說明CO開始與CoO發生反應生成Co和二氧化碳,所以CO的體積分數降低。圖像為(見答案)。


科目:高中化學 來源: 題型:
【題目】50 mL 0.50 mol·L-1的鹽酸與50 mL 0.55 mol·L-1NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,完成下列問題:

(1)從實驗裝置上看,圖中尚缺少的一種玻璃用品是_____________。請指出裝置中的另外錯誤是 。
(2)燒杯間填滿碎紙條的作用是___________。
(3)大燒杯上如不蓋硬紙板,求得的中和熱數值___________(填“偏大”“偏小”“無影響”)。
(4)實驗中改用60mL0.50mol·L-1的鹽酸跟60mL0.55mol·L-1NaOH溶液進行上述實驗相比,所放出的熱量___________(填“相等”“不相等”),所求中和熱___________(填“相等”“不相等”)。
(5)用相同濃度體積的氨水代替NaOH溶液進行上述實驗,測得的中和熱的數值會_____;用50 mL 0.50 mol·L-1NaOH溶液進行上述實驗,測得的中和熱的數值會_____(均填“偏大”“偏小”“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】正在研制的一種“高容量、低成本”鋰—銅空氣燃料電池。該電池通過一種復雜的銅腐蝕現象產生電力,其中放電過程為2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列說法不正確的是( )

A.放電一段時間后右側水溶液pH升高
B.整個反應過程中,銅相當于催化劑
C.通空氣時,銅被腐蝕,表面產生CuO
D.放電時,正極的電極反應式為Cu2O+H2O+2e—=2Cu+2OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含氮化合物是化學與工業中運用廣泛的物質。

(1)該小組利用電解原理設計了如右圖裝置進行H2還原NO的實驗(高質子導電性的SCY陶瓷(能傳遞H+)為介質,金屬鈀薄膜做電極)。鉑電極B是____極,鈀電極A的電極反應式為_____________。
(2)若工業廢水中的NO2- 的濃度約為1.0×10-4 mol·L-1 ,取工業廢水5 mL 于試管中,滴加2滴0.1 mol·L-1 的硝酸銀溶液,能否看到沉淀現象?試通過計算說明。(注:1mL溶液以20滴計;Ksp(AgNO2)=2×10-8)
(3)已知鍵能數據,H-H 436,S=S 255,H-S 339,單位kJ/mol。請計算熱化學方程式2H2(g) + S2(g) = 2H2S(g)的ΔH=___________
(4)將一定量純凈的氨基甲酸銨置于特制的密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
實驗測得不同溫度下的平衡數據列于下表:
溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡氣體總濃度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
根據表中數據,列式計算25.0℃時的分解平衡常數:__________________________。
已知:NH2COONH4+2H2O![]() NH4HCO3+NH3·H2O。該研究小組分別用三份不同初始濃度的氨基甲酸銨溶液測定水解反應速率,得到c(NH2COO-)隨時間變化趨勢如圖所示。
NH4HCO3+NH3·H2O。該研究小組分別用三份不同初始濃度的氨基甲酸銨溶液測定水解反應速率,得到c(NH2COO-)隨時間變化趨勢如圖所示。

根據圖中信息,如何說明水解反應速率隨溫度升高而增大:_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氯化砜(SO2Cl2)是一種無色液體,主要用于有機物和無機物的氯化等。其熔點為-54.1℃.沸點為69.2℃;常溫下比較穩定,受熱易分解,遇水劇烈反應生成硫酸和鹽酸。
(1)制備。實驗室可利用SO2和Cl2按下列裝置制取少量SO2Cl2(丙中放有樟腦液,起催化作用)。已知SO2(g)+Cl2(g)![]() SO2Cl2(g) △H<0
SO2Cl2(g) △H<0
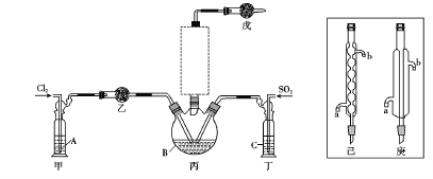
①可以用濃鹽酸和酸性高錳酸鉀制取氯氣,該反應的化學方程式為 ;溶液A為 。
②上圖實框中儀器己的名稱為 ;反應裝置圖的虛框中未畫出的儀器是 (填“己”或“庚”)。
③如果將丙裝置放入冰水中,會更有利于二氯化砜的生成,其原因是 。
④下列有關說法錯誤的是 (填編號)。
a.乙、戊裝置相同,在實驗中的作用也完全相同
b.甲、丁裝置為洗氣裝置,可用于氣體的除雜和干燥
c.組裝儀器后首先要進行的操作是檢查裝置的氣密性
d.為提高反應物的利用率,可控制甲、丁裝置中產生氣泡的速率相等
(2)提純。將收集到的產物進行減壓蒸餾,減壓蒸餾的目的是 。
(3)測定。取1.00g蒸餾后液體,小心地完全溶于水,向所得的溶液中加入足量氯化鋇溶液,測得生成沉淀的質量為1.60g,則所得蒸餾成分中二氯化砜的質量百分含量為 %。
(4)貯存。二氯化砜應儲存于陰涼、干燥、通風良好的庫房。但久置后微顯黃色,其原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】右圖為濃硫酸與銅片反應的裝置。請回答:
(1)濃硫酸與銅片反應的化學方程式為 。

(2)反應一段時間后,試管乙中品紅溶液的現象是 。
(3)下列有關該實驗的說法中,不正確的是 。
A.該反應中濃硫酸只體現酸性
B.試管乙中含有堿液的棉花,其作用是吸收過量的SO2,防止環境污染
C.反應一段時間后,將試管甲中的溶液緩慢倒入盛有水的燒杯,溶液顯藍色
D.含0.04mol溶質的濃硫酸與足量的銅片反應,能收集到448mL的SO2(標準狀況)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有X、Y、Z、T、U五種短周期元素。X、Y、Z三元素在周期表中的位置如下所示,三元素的原子序數之和是41。X和T的單質在不同條件下反應,可以生成T2X(白色固體)和T2X2(淡黃色固體)兩種化合物。U單質在Z單質中燃燒時產生蒼白色火焰,生成物的水溶液能使石蕊試液變紅。
X | |
Y | Z |
(1)各元素的符號是:Z________,T________
(2)Y原子的結構示意圖為____________________,U2X的電子式
(3)YX2和U2Y反應的化學方程式為____________________________,其中氧化劑是____________,被氧化的元素是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氣是清潔的能源,也是重要的化工原料,根據以下兩種制氫方法。完成下列問題:
(1)方法一:H2S熱分解法,反應式為:2H2S(g)![]() 2H2(g)+S2(g)△H
2H2(g)+S2(g)△H
在恒容密閉容器中,測定H2S分解的轉化率(H2S的起始濃度均為cmol/L),測定結果見右圖,圖中曲線a表示H2S的平衡轉化率與溫度關系,曲線表示不同溫度下反應經過相同時間未達到化學平衡時H2S的轉化率。

①△H______0,(“>”、“<”或“=”),
②若985℃時,反應經tmin達到平衡,此時H2S的轉化率為40%,則tmin內反應速率v(H2)=______(用含c、t的代數式表示)。
③請說明隨溫度的升高,曲線b向曲線a接近的原因:______。
(2)方法二:以CaO為吸收體,將生物材質(以C計)與水蒸氣反應制取H2.相關主要反應如下:
I:C(s)+H2O(g)═CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g) △H=-43kJ/mol
Ⅲ:CaO(s)+CO2(g)═CaCO3(s) △H=-178.3kJ/mol
①計算反應C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)的△H=______;
CaCO3(s)+2H2(g)的△H=______;
若K1、K2、K3分別為反應I、Ⅱ、Ⅲ的平衡常數,該平衡常數K=_____________(用K1、K2、K3表示)。
②對于可逆反應C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g),采取以下措施可以提高H2產率的是______。(填字母編號)
CaCO3(s)+2H2(g),采取以下措施可以提高H2產率的是______。(填字母編號)
A.降低體系的溫度
B.壓縮容器的體積
C.適當增加水蒸氣的通入量
D.增加CaO的量
③下圖為反應I在一定溫度下,平衡時各氣體體積百分含量隨壓強變化的關系圖。若反應達某一平衡狀態時,測得c(H2O)=2c(H2)=2c(CO)=2mol/L,試根據H2O的體積百分含量變化曲線,補充完整CO的變化曲線示意圖。
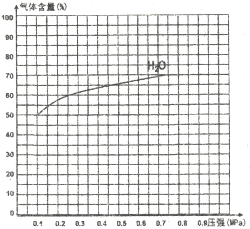
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高錳酸鉀是中學化學常用的強氧化劑,實驗室中可通過以下反應制得:
MnO2熔融氧化:3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
相關物質的溶解度數據見下表:
20℃ | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
s(g/100g水) | 111 | 33.7 | 11.1 | 6.34 |
已知K2MnO4溶液顯綠色,KMnO4溶液顯紫紅色。實驗流程如下:

請回答:
(1)步驟①應在 中熔化,并用鐵棒用力攪拌,以防結塊。
A.燒杯 B.蒸發皿 C.瓷坩堝 D.鐵坩堝
(2)①綜合相關物質的化學性質及溶解度,步驟③中可以替代CO2的試劑是 。
A.二氧化硫 B.稀醋酸 C.稀鹽酸 D.稀硫酸
②當溶液pH值達10~11時,停止通CO2;若CO2過多,造成的后果是 。
(3)烘干時,溫度控制在80℃為宜,理由是 。
(4)工業上采用電解K2MnO4水溶液的方法來生產KMnO4,其中隋性電極作陽極,鐵作陰極。請寫出陽極的電極反應式 ,與原方法相比,電解法的優勢為 。
(5)通過用草酸滴定KMnO4溶液的方法可測定KMnO4粗品的純度(質量分數)。
①量取KMnO4溶液應選用 (填“酸式”或“堿式”)滴定管;若量取KMnO4溶液的滴定管用蒸餾水洗凈后未潤洗,則最終測定結果將 (填“偏大”、“偏小”或“不變”)。
②滴定過程中反應的離子方程式為______。(已知:常溫下0.01 mol/L的H2C2O4溶液的pH為2.1)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com