
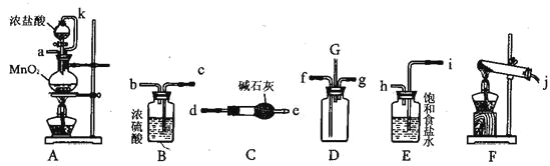
【題目】某化學興趣小組利用以下各裝置連接成一整套裝置,探究氯氣與氨氣之間的反應。其中D 為純凈干燥的氯氣與純凈干燥氨氣反應的裝置。
請回答下列問題:
(1)連接好裝置后,必需進行的一步實驗操作是_____
(2)裝置E 的作用是_____,橡膠管 k 的作用是_____
(3)裝置F 中試管內發生反應的化學方程式 _____
(4)裝置D 內出現濃厚的白煙并在容器內壁凝結,另一產物是空氣的主要成分之一,寫出該反應的化學方程式_____
(5)接入D 裝置的兩根導管左邊較長、右邊較短,目的是_____
(6)整套裝置從左向右的連接順序是(j)接______、______接(f) (g)接______ 、______接______ 、______接(a)
【答案】檢查裝置氣密性 除去氯氣中的氯化氫氣體 平衡氣壓,保證濃鹽酸順利滴下 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+ 2H2O 8NH3+3Cl2= 6NH4Cl+N2 使氨氣和氯氣充分接觸 d e b c h i
CaCl2+2NH3↑+ 2H2O 8NH3+3Cl2= 6NH4Cl+N2 使氨氣和氯氣充分接觸 d e b c h i
【解析】
A為制備氯氣的發生裝置,B干燥氯氣的裝置,C干燥氨氣的裝置,D氯氣與氨氣的發生裝置,E為除去氯氣中的氯化氫的除雜裝置,F為制備氨氣的發生裝置。
(1)連接好裝置后,必需進行的一步實驗操作是檢查裝置的氣密性,故答案為:檢查裝置氣密性;
(2)因為濃鹽酸有揮發性,所以制備出的氯氣中會混有少量的氯化氫,應用飽和的食鹽水進行除雜,則裝置E 的作用是除去氯氣中的氯化氫氣體;橡膠管 k 連接燒瓶和分液漏斗,組成恒壓裝置,作用是平衡氣壓,保證濃鹽酸順利滴下,故答案為:除去氯氣中的氯化氫氣體;平衡氣壓,保證濃鹽酸順利滴下;
(3)F為制備氨氣的發生裝置,其中的化學反應方程式為2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+ 2H2O,故答案為:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+ 2H2O,故答案為:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+ 2H2O;
CaCl2+2NH3↑+ 2H2O;
(4)根據現象和提示可知,氯氣和氨氣反應的產物為氯化銨和氮氣,其反應的化學方程式為8NH3+3Cl2= 6NH4Cl+N2,故答案為:8NH3+3Cl2= 6NH4Cl+N2;
(5)氯氣密度較大,從短管進入,氨氣的密度較小,從長管進入,這樣操作能夠使進入其中的氣體混合均勻,接觸更充分,故答案為:使氨氣和氯氣充分接觸;
(6)由分析可知,整套裝置從左向右的連接順序是(j)接d、e接(f) (g)接b、c接h、i接(a),故答案為:d;e;b;c;h;i。


 暑假接力賽新疆青少年出版社系列答案
暑假接力賽新疆青少年出版社系列答案科目:高中化學 來源: 題型:
【題目】工業上合成CH3OH的原理為:2H2(g)+CO![]() CH3OH(g),一定溫度下,向1L恒容密閉容器中充入H2和CO,反應達平衡時CH3OH的體積分數與反應物投料之比(n(H2)/n(CO))的關系如圖所示。下列說法錯誤的是
CH3OH(g),一定溫度下,向1L恒容密閉容器中充入H2和CO,反應達平衡時CH3OH的體積分數與反應物投料之比(n(H2)/n(CO))的關系如圖所示。下列說法錯誤的是
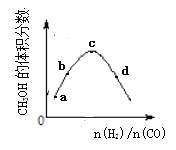
A. 相同條件下,達到平衡時混合氣體的密度與反應前相同
B. a、b、c、d四點中,c點CO的轉化率最大。
C. 若投料時n(CO)不變,a、b、c、d四點中d處CH3OH的物質的量最大
D. 圖像中 c點到d點,平衡向正反應方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究鋅與稀硫酸的反應速率(以v(H2)表示),向反應混合液中加入少量下列物質,下列判斷正確的是
A. 加入NH4HSO4固體,v(H2)不變 B. 加入KNO3固體,v(H2)不變
C. 加入CH3COONa固體,v(H2)減小 D. 滴加CuSO4溶液,v(H2)減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關電化學的敘述正確的是
A. 鍍鋅的鐵皮鍍層破損后,鐵更容易腐蝕
B. 把銅片插入三氯化鐵溶液中,在銅片表面出現一層鐵
C. 把鋅粒放入盛有鹽酸的試管中,加入幾滴氯化銅溶液,產生氣泡的速率增大
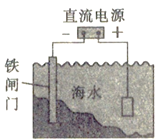
D. 如圖對海水中的鐵閘門進行電化學防護的方法是犧牲陽極的陰極保護法
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯酸是一種強酸,濃度超過40%時會發生分解,反應可表示為:aHClO3═bO2↑+cCl2↑+dHClO4+eH2O,用濕潤的淀粉碘化鉀試紙檢驗氣體產物時,試紙先變藍后褪色。下列說法不正確的是
A.由反應可推斷氧化性:HClO4<HClO3
B.變藍的淀粉碘化鉀試紙褪色是因為可能發生了:5Cl2+I2+6H2O═12H++10Cl-+2IO3-
C.若氯酸分解所得混合氣體,1 mol混合氣體質量為47.6 g,則反應方程式可表示為26HClO3 ═15O2↑+8Cl2↑+10HClO4+8H2O
D.若化學計量數a=8,b=3,則該反應轉移電子數為20e-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各項反應對應的圖像正確的是
A. 保持溫度不變,向BaSO4飽和溶液中加入硫酸鈉固體
保持溫度不變,向BaSO4飽和溶液中加入硫酸鈉固體
B. 向少量氯化鐵溶液中加入鐵粉
向少量氯化鐵溶液中加入鐵粉
C.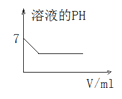 25℃時,向亞硫酸溶液中通入氯氣
25℃時,向亞硫酸溶液中通入氯氣
D.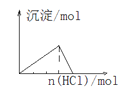 向NaAlO2溶液中通入HCl氣體
向NaAlO2溶液中通入HCl氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA 為阿伏加德羅常數的值,下列說法不正確的是( )
A.0.l mol Cl2與足量的鐵粉充分反應轉移的電子數為 0.2 NA
B.1.0 mol CH4 與Cl2 在光照下反應生成的 CH3Cl 分子數為 1.0 NA
C.標準狀況下,11.2 L甲烷和乙烯(C2H4)混合物中含氫原子數目為2 NA
D.0.1mol Cl2 通入水中,HClO、Cl-、ClO-粒子數之和小于 0.2 NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解質在水溶液中存在各種行為,如電離、水解、沉淀溶解,據所學知識回答下列問題:
(1)t℃時,純水中c(H+)=1×10-6 mol·L-1, 該溫度下,pH=10的Ba(OH)2溶液的物質的量濃度為_________ mol·L-1。
(2)25℃時,將 a mol·L-1 的醋酸和 b mol·L-1 的氫氧化鈉溶液等體積混合后,溶液的pH=7,則溶液中c(CH3COO-)+c(CH3COOH)=__________ mol·L-1,a_______ b(填“﹥”、“﹤”或“=”)。
(3)工業上采取用氨水除去SO2,已知25 ℃,NH3 H2O的Kb=1.8×10-5,H2SO3的 Ka1=1.3 × 10一2,Ka2=6.2 × 10一8。若氨水的濃度為2.0 mo1/ L,溶液中的c(OH-)=_____ mo1/ L;將SO2通入該氨水中,當c(OH-)降至2.0 × 10一6mo1/ L時,溶液中的![]() =_____________。
=_____________。
(4)將AgCl分別放入:①5 mL水 ②10 mL 0.1 mol·L-1 MgCl2溶液③40 mL 0.3mol·L-1 鹽酸溶液中溶解至溶液飽和 ④20 mL 0.5mol·L-1 NaCl溶液 ,各溶液中Ag+的濃度分別為a、b、 c、d,它們由大到小的排列順序是____________(用字母表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寶雞被譽為“青銅器之鄉”,出土了大盂鼎、毛公鼎、散氏盤等五萬余件青銅器。研究青銅器(含Cu、Sn等)在潮濕環境中發生的腐蝕對于文物保護和修復有重要意義。下圖為青銅器在潮濕環境中發生電化學腐蝕的原理示意圖,下列說法不正確的是( )

A. 青銅器發生電化學腐蝕,圖中c作負極
B. 潮濕環境中Cl-濃度大有利于多孔粉狀銹的生成
C. 若生成0.2 mol Cu2(OH)3Cl,則消耗的O2體積為4.48L
D. 環境中的Cl與正、負兩極反應的產物作用生成a的離子方程式為2Cu2++3OH+Cl===Cu2 (OH)3Cl↓
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com