
ij���W(xu��)�о�С�M̽�����l�������W(xu��)����(y��ng)mA(g)��nB(g) pC(g)�����ʺ�ƽ���Ӱ푈D�����£������Д����_����
pC(g)�����ʺ�ƽ���Ӱ푈D�����£������Д����_����

A���ɈD1��֪��T1��T2��ԓ����(y��ng)������(y��ng)�����ᷴ��(y��ng)
B���ɈD2��֪��ԓ����(y��ng)m��n��p
C���D3�У���ʾ����(y��ng)����v��>v�������c(di��n)3
D���D4�У���m��n��p���ta����һ��ʹ���˴���
C
��������
ԇ�}������A���ɈD1��֪���ض���T2�r�����_(d��)��ƽ�⡣�f��T1��T2�����ߜضȣ����W(xu��)����(y��ng)���ʼӿ죬�_(d��)��ƽ������Ҫ�ĕr�g�s�̡�����ڜضȞ�T2�rC%�pС���f�����ߜضȣ����W(xu��)ƽ�����淴��(y��ng)�����Ƅӡ��淴��(y��ng)��������ᷴ��(y��ng)������ԓ����(y��ng)������(y��ng)��şᷴ��(y��ng)���e�`��B���ɈD2��֪���ڜضȲ�׃�r������(qi��ng)��C%���ࡣ�f������(qi��ng)�����W(xu��)ƽ����������(y��ng)�����Ƅӡ�����(j��)ƽ���Ƅ�ԭ��������(qi��ng)�����W(xu��)ƽ������w�w�e�pС�ķ����Ƅӣ�������(y��ng)�������w�w�e�pС�ķ�������ԓ����(y��ng)m��n>p���e�`��C���D3��ʾ�����ڲ�ͬ�Ĝض��£���(d��ng)����(y��ng)�_(d��)��ƽ��r����(y��ng)��B���D(zhu��n)�����c�ضȵ��P(gu��n)ϵ�������ϵ��c(di��n)��ʾ����ƽ���B(t��i)��v��=v�����^3�@һ�c(di��n)���M����(bi��o)�Ĵ��£��������cһ�c(di��n)���@�c(di��n)��B���D(zhu��n)���ʸ���3�@һ�c(di��n)���f��3δ�_(d��)��ƽ�⣬����(y��ng)��������(y��ng)�����M(j��n)�У��˕r��ʾ�ķ���(y��ng)����v��>v�������c(di��n)3�����_��D���D4�У���m��n��p���ta�����_(d��)��ƽ������Ҫ�ĕr�g��b�̣����_(d��)��ƽ�⡣�t������ʹ���˴�����Ҳ�����������ˉ���(qi��ng)���sС���������ݷe���e�`��
���c(di��n)������D���ڱ�ʾ���l�������W(xu��)����(y��ng)���ʺͻ��W(xu��)ƽ���Ӱ푵�֪�R��


 ��x��܇ϵ�д�
��x��܇ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���x����
 I��С�����������~�r���~�ǃ�(n��i)ȡ�����B��Ҋ�D���a(ch��n)�����dȤ�����M����̽���B��(n��i)���w�w�e�ͳɷ֡������о��ԌW(xu��)��(x��)���n�}��С��ͨ�^������P(gu��n)�Y�ϫ@֪���@�N�~�B��(n��i)����sռ�ķ�֮һ������Ҫ�������̼�͵�?d��)⣮̽���փɲ��M(j��n)�У�
I��С�����������~�r���~�ǃ�(n��i)ȡ�����B��Ҋ�D���a(ch��n)�����dȤ�����M����̽���B��(n��i)���w�w�e�ͳɷ֡������о��ԌW(xu��)��(x��)���n�}��С��ͨ�^������P(gu��n)�Y�ϫ@֪���@�N�~�B��(n��i)����sռ�ķ�֮һ������Ҫ�������̼�͵�?d��)⣮̽���փɲ��M(j��n)�У�| ���?z��i)��?/TD> | ���� | ���F(xi��n)�� |
| ��C�B��(n��i)��O2 | ||
| ��C�B��(n��i)��CO2 |

�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���x����
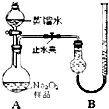 ��2011?����һģ��ij���W(xu��)�о�С�M��y��Na2O2��Ʒ���H��Na2O�s�|(zh��)���ļ��ȣ��O(sh��)Ӌ�˃ɷN�����M(j��n)��̽����
��2011?����һģ��ij���W(xu��)�о�С�M��y��Na2O2��Ʒ���H��Na2O�s�|(zh��)���ļ��ȣ��O(sh��)Ӌ�˃ɷN�����M(j��n)��̽����| ���Δ�(sh��) | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| ��(bi��o)��(zh��n)�}���w�e��mL�� | 23.00 | 24.98 | 25.00 | 25.02 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
̽���y�R����(y��ng)����ь��l��(����(sh��)��(j��)���±�)��
���׃�� �����̖ | �y����Һ����(mL) | ��ȩ����(��) | ˮԡ�ض�(��) | ����(y��ng)���Һ��pH | ���F(xi��n)�y�R�r�g(min) |
���1 | 1 | 3 | 65 | 11 | 5 |
���2 | 1 | 3 | 45 | 11 | 6.5 |
���3 | 1 | 5 | 65 | 11 | 4 |
���4 | 1 | 3 | 30 | 11 | 9 |
���5 | 1 | 3 | 50 | 11 | 6 |
���6 | 1 | 5 | 80 | 11 | 3 |
Ո�ش����І��}��
(1)��ֻ�M(j��n)�Ќ��1�͌��3����̽��Ŀ����____________________��
(2)��(d��ng)�y����Һ������1 mL����ȩ������3�Σ�ˮԡ�ضȞ�
(3)��߀Ҫ̽���y����Һ�����������F(xi��n)�y�R������Ӱ푣�����M(j��n)�Ќ�__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
ij���W(xu��)�о�С�M��y��Na2O2��Ʒ���H��Na2O�s�|(zh��)���ļ��ȣ��O(sh��)Ӌ�˃ɷN�����M(j��n)��̽����
[���һ] ȡ��Ʒ0. 100 g�����҈D��ʾ����b���M(j��n)�Мy����
���A���b��ʡ�ԣ�
��1���z���b��A�����Եķ����� ��
��2�����ڌ���^���й��a(ch��n)�����w11.20 mL��������ɘ�(bi��o)��(zh��n)
��r�����t��Ʒ��Na2O2�ļ��Ȟ� ��
[����] ��Ʒ����ˮ�����}��ζ�
��3��ȡһ������Ʒ����ˮ�����Ƴ�250 mL��Һ�����ƕr�����õ��IJ����x�����˟����Ͳ������⣬߀���õ� ��
��4��ȡ����������Һ��25.00 mL����һ����ȵĘ�(bi��o)��(zh��n)�}��ζ���ƽ�Ќ��ӛ����±���
| ���Δ�(sh��) | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| ��(bi��o)��(zh��n)�}���w�e��mL�� | 23.00 | 24.98 | 25.00 | 25.02 |
�ɱ��Д�(sh��)��(j��)��֪����(bi��o)��(zh��n)�}���w�e��ƽ��ֵ�� mL�����ζ�ǰ������������Һ��ϴ�F��ƿ�������y���Y(ji��)���a(ch��n)����Ӱ��� ���ƫ�ߡ�����ƫ�͡��oӰ푡�����
[������] ���Y(ji��)�����ȷ���
��5��С�Mͬ�W(xu��)���ȃɂ����l(f��)�F(xi��n)�����һ�y�õ�Na2O2��Ʒ�ļ��ȱ���Փֵ���@ƫС����(j��ng)�^������С�Mͬ�W(xu��)�J(r��n)�飬���@ƫ����ɲ���ʧ�`���b��ȱ������ģ������Ƿ���(y��ng)ԭ���ϵ�ԭ����Y�ϰl(f��)�F(xi��n)��Na2O2�cˮ����(y��ng)�a(ch��n)����H2O2δ��ȫ�ֽ⡣
�ٌ���Na2O2�cˮ����H2O2�Ļ��W(xu��)����ʽ ��
�����һ�ԼӸ��M(j��n)������ʹ�y���Y(ji��)���ӽ���Փֵ���������M(j��n)������
��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2011�ø���ʡ�����и�����ͨ���Ю��I(y��)���|(zh��)���z�飨���C�����W(xu��)���� �}�ͣ�����}
ij���W(xu��)�о�С�M��y��Na2O2��Ʒ���H��Na2O�s�|(zh��)���ļ��ȣ��O(sh��)Ӌ�˃ɷN�����M(j��n)��̽����
[���һ] ȡ��Ʒ0. 100 g�����҈D��ʾ����b���M(j��n)�Мy����
���A���b��ʡ�ԣ�
��1���z���b��A�����Եķ����� ��
��2�����ڌ���^���й��a(ch��n)�����w11.20 mL��������ɘ�(bi��o)��(zh��n)
��r�����t��Ʒ��Na2O2�ļ��Ȟ� ��
[����] �� Ʒ����ˮ�����}��ζ�
Ʒ����ˮ�����}��ζ�
��3��ȡһ������Ʒ����ˮ�����Ƴ�250 mL��Һ�����ƕr�����õ��IJ����x�����˟����Ͳ������⣬߀���õ� ��
��4��ȡ����������Һ��25.00 mL����һ����ȵĘ�(bi��o)��(zh��n)�}��ζ���ƽ�Ќ��ӛ����±���
| ���Δ�(sh��) | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| ��(bi��o)��(zh��n)�}���w�e��mL�� | 23.00 | 24.98 | 25.00 | 25.02 |
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com